
- •А.В. Юрьева аналитическая химия Учебное пособие
- •Предисловие
- •Глава 1. Аналитическая химия как наука
- •1.1. Предмет и методы аналитической химии. Качественный и количественный анализ
- •1.2. Значение аналитической химии
- •1.3. Краткий очерк развития аналитической химии
- •Глава 2. Качественный химический анализ
- •2.1. Особенности аналитических реакций и способы их выполнения
- •2.2. Требования к аналитическим реакциям. Чувствительность реакций. Селективные и специфические реакции
- •2.3. Дробный и систематический анализ
- •2.4. Классификации катионов
- •Сульфидная классификация катионов
- •Деление катионов на группы по кислотно-основной классификации
- •2.5. Классификация анионов
- •Классификация анионов
- •2.6. Анализ конкретных объектов
- •Изменения проб при нагревании на пластинке
- •2.7 Основы качественного анализа органических соединений
- •Практические работы
- •Групы по кислотно-основной классификации
- •Продукты некоторых аналитических реакций катионов третьей аналитической группы по кислотно-основной классификации
- •Растворимость в воде некоторых солей катионов I–III аналитических групп по кислотно-основной классификации
- •Продукты некоторых аналитических реакций катионов четвертой аналитической группы по кислотно-основной классификации
- •Продукты некоторых аналитических реакций катионов пятой аналитической группы по кислотно-основной классификации
- •Продукты некоторых аналитических реакций катионов шестой аналитической группы по кислотно-основной классификации
- •Вопросы и задачи
- •Глава 3. Метрологические основы химического анализа
- •3.1. Общая схема аналитического определения
- •Выбор метода анализа
- •Отбор и подготовка пробы к анализу
- •Проведение измерения
- •Расчет результатов анализа
- •Погрешности химического анализа
- •3.2.1. Систематические погрешности
- •3.2.2. Случайные погрешности
- •Значение t для различной доверительной вероятности
- •Вопросы и задачи
- •Глава 4. Количественный анализ. Химические методы
- •4.1. Гравиметрический анализ
- •4.1.1. Осаждение
- •4.1.2. Фильтрование и промывание осадка
- •4.1.3.Высушивание и прокаливание
- •4.1.4. Вычисления в гравиметрическом анализе
- •Практические работы
- •Вопросы и задачи
- •Глава 5. Титриметрический анализ
- •5.1. Сущность титриметрического анализа
- •5.2. Стандартизация раствора титранта
- •5.3. Основные приемы титриметрических определений
- •5.4. Расчеты в титриметрическом анализе
- •5.5. Кривые титрования
- •5.6. Основные методы титриметрического анализа
- •5.7. Техника работы
- •Вопросы и задачи
- •Глава 6. Реакции кислотно-основного взаимодействия
- •6.1. Протолитическая теория кислот и оснований Бренстеда-Лоури
- •6.2. Электронная теория Льюиса
- •6.3. Кислотно-основные и некоторые другие свойства растворителей
- •6.4. Равновесия в водных растворах кислот и оснований
- •6.5. Буферные растворы
- •6.6. Кислотно-основные индикаторы
- •Вопросы и задачи
- •Глава 7. Кислотно-основное титрование
- •7.1. Рабочие растворы
- •7.2. Кривые титрования и выбор индикатора
- •7.3. Практическое применение методов кислотно-основного титрования
- •Практические работы
- •Вопросы и задачи
- •Глава 8. Реакции окисления-восстановления. Окислительно-восстановительное титрование
- •Окислительно-восстановительное титрование
- •8.1. Требованиям к реакциям в методе окислительно-восстановительного титрования
- •8.2. Способы установления точки эквивалентности
- •8.3. Молярная масса эквивалента в реакциях окисления-восстановления
- •8.4. Кривые титрования
- •8.5. Индикаторы
- •8.6. Классификация методов окислительно-восстановительного титрования
- •8.7. Перманганатометрия
- •Практические работы
- •8.8. Иодометрия
- •Практические работы
- •8.9. Хроматометрия
- •Вопросы и задачи
- •Глава 9. Титрование по методу осаждения
- •9.1. Аргентометрия
- •9.2. Меркурометрия
- •Практические работы
- •Вопросы и задачи
- •Глава 10. Комплексометрическое титрование
- •10.1. Комплексонометрия
- •10.1.1. Рабочие растворы
- •10.1.2. Кривые титрования
- •10.1.3. Способы обнаружения конечной точки титрования
- •10.1.4. Применение комплексонометрии
- •Практические работы
- •Вопросы и задачи
- •Глава 11. Методы маскирования, разделения и концентрирования
- •11.1. Маскирование
- •11.2. Разделение и концентрирование
- •11.3. Краткая характеристика некоторых методов разделения и концентрирования
- •Вопросы и задачи
- •Глава 12. Биологические методы анализа
- •Вопросы
- •Библиографический список
- •Оглавление
- •Глава 1. Аналитическая химия как наука………………………….. ………… 4
- •Глава 2. Качественный химический анализ…………………………………….. 8
- •Глава 3. Метрологические основы химического анализа……………………. 50
- •Глава 4. Количественный анализ. Химические методы………………………. 63
- •Глава 5. Титриметрический анализ………………………………………………. 77
- •Глава 6. Реакции кислотно-основного взаимодействия ……………………… 89
- •Глава 7. Кислотно-основное титрование………………………………………… 100
- •Глава 8. Реакции окисления-восстановления. Окислительно-
6.4. Равновесия в водных растворах кислот и оснований
Кислотность раствора является одним из основных факторов, влияющих на протекание химических реакций, в связи с чем исследование и расчет равновесия в растворах кислот и оснований имеет большое практическое значение.
Удобной характеристикой кислотности раствора оказался водородный показатель, или pH, определяемый как отрицательный десятичный логарифм активности ионов водорода:
![]() .
.
При проведении приближенных расчетов можно вместо активности, в это уравнение вводить концентрацию:
![]() или
или
![]() .
.
Буква «p» часто используется как символ отрицательного логарифма, например
pOH = –lg[OH–], где [OH–] – концентрация гидроксильных групп; pKW = –lgKW, где KW – ионное произведение воды и т.д.
Учитывая, что при комнатной температуре в чистой воде [H+] = [OH–] = 1,0·10–7 моль/л, а KW = [H+]·[OH–] = 1,0·10-14, получим: pH + pOH = pKW =14.
Условие [H+] = 1,0·10–7 моль/л или pH = 7 соответствует нейтральной реакции раствора. В кислых растворах [H+] < 1·10–7 моль/л и pH < 7,0, в щелочных – [H+] < 1·10–7 моль/л и рН > 7,0.
С ростом температуры
pH
нейтрального раствора несколько
уменьшается вследствие увеличения
диссоциации воды и, например, при 80 оС
концентрация ионов водорода в нейтральном
растворе равна:
![]() т.е.
pH
= 6,3.
т.е.
pH
= 6,3.
Для решения многих аналитических задач необходимо уметь, в частности, рассчитывать концентрацию ионов водорода (или pH) и концентрацию аниона в растворах различных кислот и оснований, смесях кислот и т. д. С этой точки зрения обычно выделяют группу сильных кислот и оснований, практически нацело диссоциирующих в растворе при всех концентрациях, и группу слабых кислот и оснований, диссоциация которых невелика. Промежуточное положение занимают кислота и основания средней силы.
Одноосновные
кислоты и основания.
В водных растворах сильных
кислот
протолитическая реакции HA+H2O
= H3O++
A–
целиком сдвинута вправо. Вследствие
практически полной диссоциации
концентрация ионов водорода в растворах
сильных кислот равна концентрации
кислоты
![]() Например, в 0,1 М растворе HCl
Например, в 0,1 М растворе HCl
![]() М, т.е pH=-lg[H+]=-lgCHCl
= 1,0.
М, т.е pH=-lg[H+]=-lgCHCl
= 1,0.
Аналогично в растворе сильного основания СOH = CМOH, где М – щелочной металл.
Пример. Чему равен pH в 0,1 М растворе NaOH ?
Решение. Найдем концентрацию ионов водорода исходя из постоянства величины ионного произведения воды и [OH-] = CNaOH.
KW = [H+]·[OH-] = 1,0·10-14.
[H+] = KW/[OH-] = 1,0·10-14/0,1 = 1,0·10-13, а pH = 13.
Слабые кислоты и основания диссоциированы в водном растворе лишь частично. Для слабой кислоты HA состояние равновесия реакции
HA +H2O ↔ H3O+ + A– сдвинуто влево.
К слабому основанию B присоединяются протоны воды:
B + H2O ↔ BH+ + OH-.
Из уравнений видно, что в этих равновесиях участвуют сопряженные пары кислот и оснований: с кислотой HA сопряжено основание А–, а с основанием B – кислота BH+.
Установим связь
между константами диссоциации сопряженных
кислот и оснований. Для кислоты HA
константа диссоциации или константа
кислотности (Kk)
равна
![]() .
.
Для основания A–
константа диссоциации основания или
константа основности (Ko)
равна, следует из уравнения A–
+ H2O
= HA
+ OH–:
![]() .
.
Перемножив Kk
и Ko,
получим
![]() .
.
Таким образом, произведение констант кислотности и основности сопряженных кислот и оснований равно ионному произведению воды, т.е. если известна одна из констант (Kk или Ko), то можно из этой зависимости найти другую.
Вычислим pH в растворе слабой кислоты HA, используя упрощенное равновесие:
HA ↔ H+ + A–.
Ионы H+ образуются не только вследствие диссоциации кислоты, но и при диссоциации воды, однако для растворов не очень слабых кислот можно не принимать во внимание диссоциацию воды и считать, что [H+] = [A–].
Концентрация
недиссоциированных молекул кислоты
![]() .
Равновесие диссоциации характеризуется
константой:
.
Равновесие диссоциации характеризуется
константой:
![]() .
.
Обозначив
концентрацию [H+]
= [A–]
через x,
получим
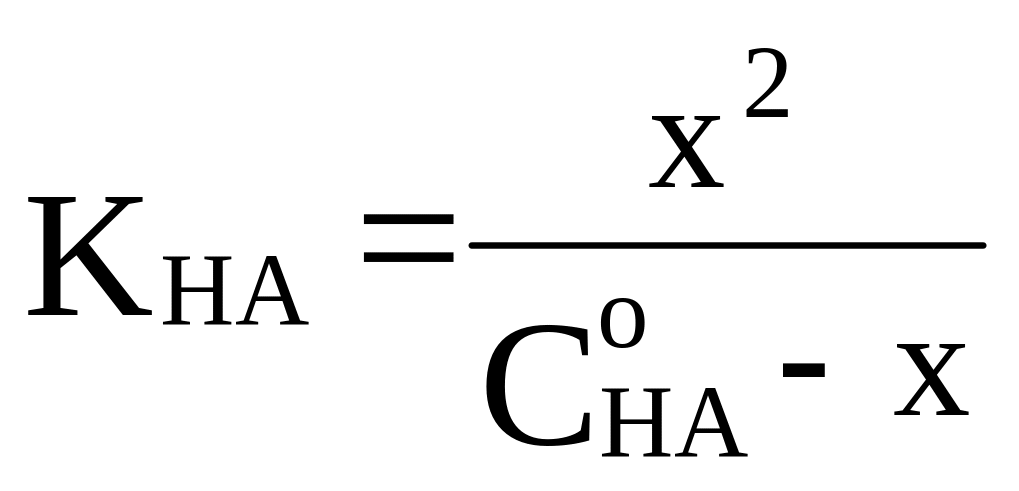 .
.
Решим квадратное
уравнение
![]() :
:
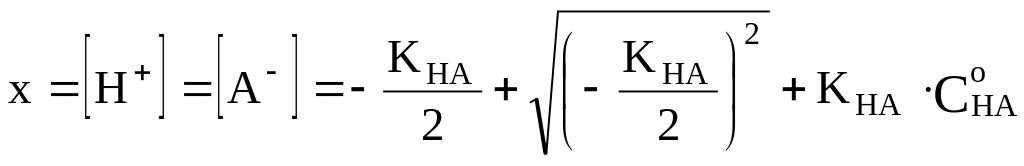 .
.
Если x
<<![]() кислота достаточно слабая, то С
кислота достаточно слабая, то С![]() – х ≈ С
и решение упрощается:
– х ≈ С
и решение упрощается:
![]() .
.
Прологарифмировав
и сменив знаки, получим приближенное
уравнение
![]() .
.
Пример. Чему равен pH 0,1 М раствора CH3COOH?
Решение. Вычислим pH по приближенному уравнению, взяв табличное значение
KHA = 1,74·10-5 (pK = 4,76): pH = 1/2 · 4,76 – 1/2 lg0,1=2,88.
Аналогично рассчитывается равновесие в растворах слабых оснований. В растворе слабого основания B существует равновесие: B + HOH ↔ BH+ + OH-.
Константа диссоциации
для него
![]() .
.
Проводя рассуждения
подобные рассмотренным для кислоты,
получим (с учетом того, что
![]() ):
):
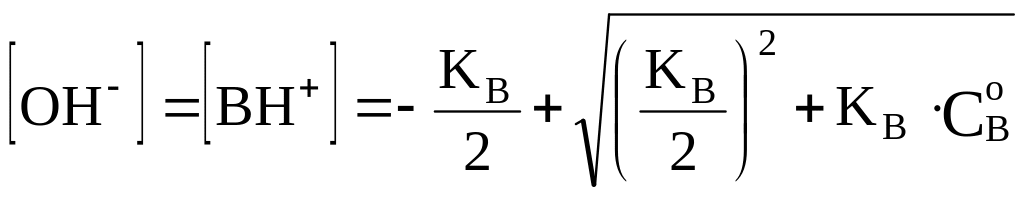 .
.
Если
![]() ,
то
,
то
![]() и
и
![]() ,
а
,
а
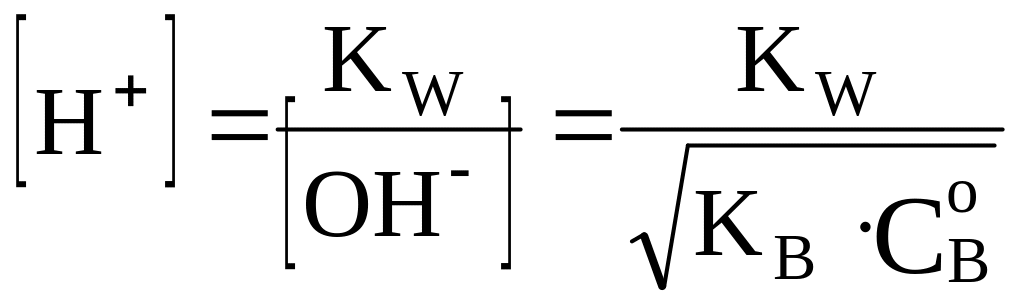 ,
или, учитывая, что
,
или, учитывая, что
![]() (BH+
– сопряженная с основанием B
кислота):
(BH+
– сопряженная с основанием B
кислота):
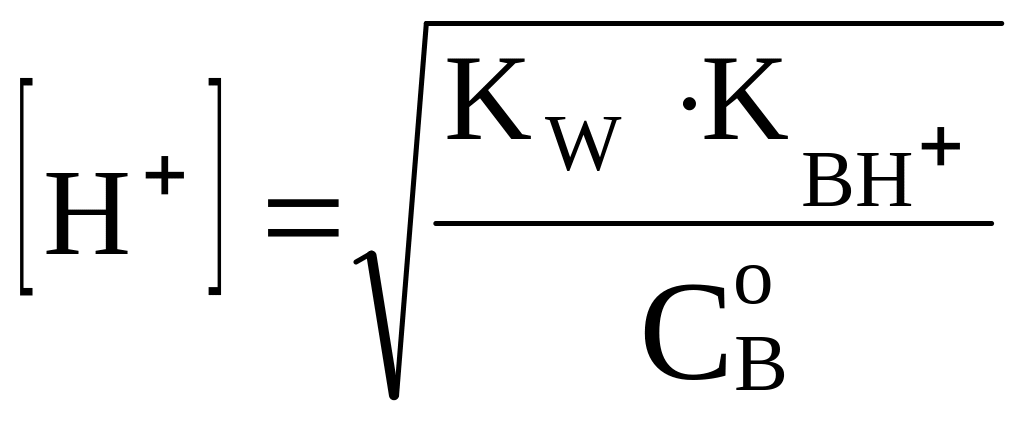 .
.
Пример. Чему равен pH 0,1 М раствора CH3COONa?
Решение. Ион CH3COO– является сопряженным с уксусной кислотой основанием
(CH3COOH ↔ CH3COO– + H+), поэтому с учетом того, что соль полностью диссоциирована и концентрация основания CH3COO– равна концентрации соли:
![]() и pH
≈ 9 (среда щелочная).
и pH
≈ 9 (среда щелочная).
Многоосновные кислоты и основания диссоциируют ступенчато, и каждая ступень диссоциации характеризуется своей константой. Например для сероводородной кислоты:
H2S ↔ H+ + HS– K1 = 1,0∙10-7;
HS– ↔ H+ + S2– K2 = 1,3∙10-13.
Разница в ступенчатых константах диссоциации H2S составляет 6 порядков. При таком соотношении констант можно ограничиться учетом диссоциации лишь для первой ступени и расчеты проводить как для одноосновных кислот и оснований.
