
- •1. Одноэлектронное приближение. Электронная конфигурация атома. Принципы заполнения одноэлектронных состояний.
- •2. Закон Рауля. Давление пара над идеальным раствором. Предельно разбавленные растворы. Закон Генри.
- •3. Гетерогенный катализ: основные стадии, энергетический профиль.
- •4. Расчёт электродных потенциалов по уравнению Нернста.
- •1. Электронное состояние атома как целого. Квантовые числа. Атомные
- •2. Энтропия и 2-й закон термодинамики. Термодинамическое и статистическое определения энтропии, их взаимосвязь.
- •3. Фотохимические реакции. Законы фотохимии. Квантовый выход. Примеры фотохимических реакций.
- •4. Анализ конкретной фазовой диаграммы двухкомпонентной системы.
- •Водородоподобные атомы. Уровни энергии и квантовые числа электрона.
- •2. Исходные постулаты термодинамики. Термические и калорические уравнения состояния.
- •3. Квазистационарное приближение в химической кинетике. Условия применимости, энергетические кривые.
- •4. Равновесный состав газовой смеси.
- •1. Электронные конфигурации переходных элементов 4-го периода и их ионов.
- •2. Коллигативные свойства растворов (электролиты и неэлектролиты).
- •3. Скорость химической реакции. Кинетическое уравнение. Закон действующих масс для элементарных реакций.
- •4. Энергии Гиббса химической реакции при различных температурах.
- •1. Электронные состояния двухатомных молекул. Характеристики кова-
- •2. Связь константы равновесия с изменением термодинамических функций в реакции. Зависимость константы равновесия от температуры. Принцип Ле Шателье.
- •3. Константа скорости. Порядок, псевдопорядок и молекулярность реакции. Экспериментальное определение порядка реакции и константы скорости.
- •1. Химическая связь и причины её образования. Кривые потенциальной энергии для двухатомной молекулы.
- •2. Электродные потенциалы, их зависимость от концентраций (активностей) ионов и температуры. Стандартные электродные потенциалы.
- •3. Тепловой эффект химической реакции. Закон Гесса. Энтальпия образования.
- •4. Порядок реакции по кинетическим данным.
- •1. Простейшие понятия теории молекулярных орбиталей. Метод молкао.
- •2. Электродвижущая сила (эдс), ее связь с термодинамическими функциями. Типы электрохимических ячеек.
- •3. Формальная кинетика реакций 1-го порядка. Решение прямой и обратной задачи.
- •4. Изменение энтропии в различных процессах (изменение температуры, объема, давления, фазовый переход, химическая реакция).
- •Теория мо. Электронные конфигурации молекул и молекулярных ионов водорода и гелия.
- •2. Сечения простейших фазовых диаграмм «температура – состав». Типичные диаграммы «жидкость – пар» (с азеотропом и без).
- •3. Энтальпия химической связи. Зависимость теплового эффекта реакции от температуры и давления.
- •4. Константы скорости в параллельных реакциях.
- •1. Межмолекулярные взаимодействия и их классификация. Сравнение межмолекулярных
- •2. Третий закон термодинамики. Абсолютная энтропия.
- •3. Влияние температуры на скорость реакции. Уравнение Аррениуса, его интегральная и дифференциальная формы. Опытная энергия активации.
- •4. Константа химического равновесия и равновесного состава смеси веществ.
- •Водородная связь и её характеристики. Примеры неорганических веществ с водородной связью.
- •2. Термодинамические системы и их классификация. Экстенсивные и интенсивные величины. Функции состояния и функции процесса. Термодинамические координаты и силы.
- •3. Механизмы реакций. Решение кинетических уравнений для последовательных реакций первого порядка.
- •4. Фазовые диаграммы одно- или двухкомпонентной системы на основе правила фаз Гиббса.
- •2. Фундаментальное уравнение Гиббса в переменных t, V. Критерии самопроизвольности процесса и равновесия.
- •2. Принцип независимости химических реакций. Составление и решение кинетических уравнений для обратимых реакций первого порядка.
- •4. Давления пара над чистым веществом и теплота фазового перехода.
- •1. Водородная связь и её характеристики. Влияние водородной связи на свойства органических веществ.
- •2. Химический потенциал, определение. Идеальные растворы. Термодинамика смешения. Активность и коэффициенты активности.
- •3. Механизм реакции. Составление и решение кинетических уравнений для параллельных реакций первого порядка.
- •4. Эмпирическая константа скорости и эффективная энергия активации сложной реакции.
- •1. Полиморфизм металлов (на примере железа или олова).
- •2. Внутренняя энергия и 1-й закон термодинамики в переменных t, V. Тепловой эффект процесса при постоянном объеме или давлении. Калорические коэффициенты.
- •3. Фотохимические реакции. Первичные процессы при возбуждении: фотофизические и фотохимические. Кинетика фотохимических реакций. Отличие фотохимических реакций от темновых.
- •4. Состав пара над идеальным раствором.
- •1. Основные типы кристаллических решёток металлов. Плотнейшие шаровые упаковки.
- •2. Фазовые диаграммы однокомпонентных систем. Уравнение Клапейрона-Клаузиуса.
- •3. Уравнения химических реакций. Стехиометрические соотношения. Химическая переменная. Энергетическая кривая химической реакции (элементарной и двухстадийной).
- •4. Квантовый выход фотохимической реакции.
- •1. Структура ионных кристаллов. Ионная модель.
- •2. Объединение 1-ого и 2-ого законов термодинамики. Фундаментальное уравнение Гиббса для закрытых и открытых систем.
- •4. Константа скорости для реакций целого порядка и определение энергии активации по температурной зависимости константы скорости.
- •1. Основные структурные типы ионных соединений: NaCl, CsCl, CaF2.
- •2. Химический потенциал компонента идеального раствора. Термодинамические функции образования идеального раствора.
- •3. Основные понятия катализа. Классификация каталитических реакций. Гомогенный катализ. Общий механизм катализа.
- •4. Анализ фазовой диаграммы одно- или двухкомпонентной системы на основе правила фаз Гиббса.
- •1. Энергия ионной кристаллической решётки. Цикл Борна-Габера.
- •2. Энтальпия и 1-ый закон термодинамики в переменных t, p. Тепловой эффект процесса при постоянном давлении. Изобарная теплоемкость.
- •3. Электроды и полуреакции. Основные типы электродов. Стандартные электродные потенциалы. Электродвижущая сила (эдс), ее связь с термодинамическими функциями.
- •4. Система кинетических уравнений по механизму реакции.
- •1. Радиусы атомов: ковалентные, металлические, ван-дер-ваальсовы. Радиусы ионов, способы их определения.
- •2. Стандартные состояния и термодинамические функции индивидуальных веществ. Оператор химической реакции. Изменение термодинамических функций в химических реакциях.
- •3. Параллельные обратимые реакции. Термодинамический и кинетический контроль.
- •4. Определение молярной массы растворенного вещества по коллигативным свойствам раствора.
- •1. Энергия ионной кристаллической решётки, её вычисление в рамках ионной модели.
- •2. Энтропия как функция состояния и как критерий направленности самопроизвольного процесса.
- •3. Условия химического равновесия. Закон действующих масс для идеально-газовой смеси. Константы равновесия и связь между ними.
- •3. Зависимость температуры кипения и плавления чистых веществ от давления. Уравнения Клапейрона и Клапейрона-Клаузиуса.
- •4. Расчёт плотности ионного кристалла по радиусам ионов и типу решётки.
3. Квазистационарное приближение в химической кинетике. Условия применимости, энергетические кривые.
Для большинства сложных реакций, включающих несколько элементарных стадий, кинетические уравнения обычно настолько сложны, что их можно точно решить только численным интегрированием. В то же время, разные константы скорости, входящие в эти уравнения, обычно отличаются друг от друга на много порядков, что позволяет при решении кинетических уравнений использовать приближенные методы.
Рассмотрим последовательность реакций первого порядка: A→k1 B →k2 D, для которой k2 >> k1. Точное решение системы кинетических уравнений можно привести к упрощенному виду:
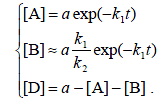
при k1 << k2 концентрация B в любой момент времени очень мала, следовательно мала и скорость ее изменения. В этих условиях концентрацию промежуточного вещества считают квазистационарной. Условие квазистационарности позволяет выражать концентрацию промежуточных веществ через концентрации реагентов и тем самым упрощать кинетические уравнения. Например, квазистационарное приближение позволяет исключить [B] из кинетических уравнений:
![]()
то есть суммарная реакция имеет первый порядок по реагенту.
Условия применимости: 1) скорости образования и расходования этих продуктов хотя и одинаковы, но изменяются со временем:

2) если сравнить концентрации промежуточных веществ и продуктов, рассчитанные в квазистационарном приближении, с точными значениями, видно, что приближение начинает хорошо работать лишь через небольшое время после начала реакции. Это время примерно соответствует четырем периодам полураспада вещества B. Именно это время является границей, за которой квазистационарное приближение имеет высокую точность.
Квазистационарное приближение применимо тогда, когда промежуточное вещество распадается быстро, а квазиравновесное – когда оно распадается медленно.
4. Равновесный состав газовой смеси.
Билет 4.
1. Электронные конфигурации переходных элементов 4-го периода и их ионов.
2. Коллигативные свойства растворов (электролиты и неэлектролиты).
Свойства разбавленных растворов, зависящие только от количества растворенного вещества, называют коллигативными свойствами. К ним относятся: понижение давления пара растворителя над раствором, повышение температуры кипения и понижение температуры замерзания раствора, а также осмотическое давление. Понижение температуры замерзания и повышение температуры кипения раствора по сравнению с чистым растворителем описывается формулами:

где m2 - молярность раствора, KК и KЭ – криоскопическая и эбуллиоскопическая постоянные растворителя, x2 – мольная доля растворенного вещества, ΔплH и ΔиспH – энтальпии плавления и испарения растворителя, Tпл и Tкип – температуры плавления и кипения растворителя, M1 – молярная масса растворителя.
Осмотическое давление π в разбавленных растворах можно рассчитать по уравнению
![]()
где a1 – активность растворителя (≈ x1), x2 – мольная доля растворенного вещества, V1 – мольный объем растворителя. В разбавленных растворах это выражение преобразуется в уравнение Вант–Гоффа:
![]()
где с – молярность раствора (молярная концентрация).
Поскольку при диссоциации число частиц в растворе возрастает, растворы электролитов обладают аномальными коллигативными свойствами. Уравнения, описывающие коллигативные свойства растворов неэлектролитов, можно применить и для описания свойств растворов электролитов, если ввести поправочный изотонический коэффициент Вант-Гоффа i, например:
![]()
Изотонический коэффициент связан со степенью диссоциации α электролита:
i = 1 + α(ν – 1),
где ν – количество ионов, образующихся при диссоциации одной молекулы.
