
- •Б 1. Взаимодействие электромагнитного излучения с веществом. Соотношение Эйнштейна
- •Поглощающие системы в фотометрии
- •Б 4. Результаты изменения спектральных свойств поглощающих систем (Эффекты и сдвиги).
- •Б 5. Основные фотометрические величины: а, т,ε (молярный кооф светопоглощения)
- •Б 6. Молярный коэффициент светопоглощения (погашения)
- •Б 7 Основные законы светопоглощения
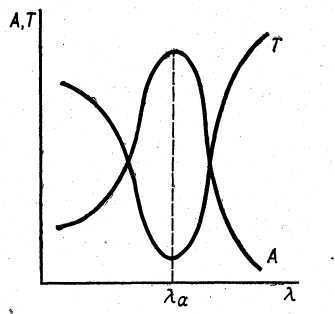
- •Зависимость а и т от λ
- •Б8. Представление о спектрах поглощения
- •Б 14. Монохроматор, светофильтры.Призмы, диф решётки
- •Б15. Кюветное отделение, материал кювет. Выбор материала и размера кювет. Выбор раствора сравнения при фотометр измерениях
- •Б 18. Дифференциальный метод определения концентраций
- •Б19. Анализ многокомпонентных систем
- •Б 21.Пламенная фотометрия
- •Преимущества пламенной фотометрии
- •Б22. Методы определения концентраций
- •Устранение помех
Поглощающие системы в фотометрии
Растворы аква-комплексов (ионов), обладающие поглощением в видимой области спектра; их молярный коэффициент поглощения (ε) не выше n·102.
Органические соединения.
Растворы солей элементов в высших степенях окисления (например,
 и т.д.).
и т.д.).Растворы комплексов металлов с неорганическими (ε~n·103) и органическими (ε~n·104) лигандами.
Б 4. Результаты изменения спектральных свойств поглощающих систем (Эффекты и сдвиги).
В результате протекания процессов вызывающих изменение строения вызывающих частиц или смещение равновесия растворов меняются спектральные свойства поглощаемых систем. Эти изменения в спектрах характеризуются либо увеличением поглощения - гиперхромный эффект, уменьшение поглощения - гипсохромный эффект. Батохромный сдвиг – смещение мах поглощения в сторону больших длин волн. Гипсохромный – в сторону меньших длин волн
Антрахинон α-оксиантрахинон ализарин
Б/ц жёлтый оранжевый
Б 5. Основные фотометрические величины: а, т,ε (молярный кооф светопоглощения)
Оптическая плотность (А или D) – аналитический сигнал, характеризующий способность раствора поглощать свет; величина безразмерная
Прозрачность или пропускание (Т) – отношение интенсивности монохроматического потока излучения, прошедшего через исследуемый объект, к интенсивности первоначального потока излучения. Величина Т характеризует способность раствора пропускать свет. Пропускание измеряется в процентах или в долях ( от 0 до 1).
Формулы рисунок
![]()
![]()
![]()
![]()
Молярный коэффициент светопоглощения (погашения) ε – является основной характеристикой поглощения любой системы при данной длине волны; отражает индивидуальные свойства окрашенных соединений и является их определяющей характеристикой.
Физический смысл – представляет собой оптическую плотность раствора с концентрацией 1 моль/л, помещённого в кювету с толщиной слоя 1 см; имеет размерность см2/моль
З
 ависит
от длины волны падающего света,
температуры раствора, природы
растворённого вещества
ависит
от длины волны падающего света,
температуры раствора, природы
растворённого вещества
Б 6. Молярный коэффициент светопоглощения (погашения)
Молярный коэффициент светопоглощения (ε) – является основной характеристикой поглощения любой системы при данной длине волны. Физический смысл: молярный коэффициент поглощения представляет собой оптическую плотность раствора с концентрацией 1 моль/л, помещенного в кювету с толщиной поглощающего слоя 1 см. ε – имеет размерность см2/моль, т.к. А – безразмерная величина. Однако принято приводить значение молярного коэффициента поглощения без обозначения его размерности. Молярный коэффициент поглощения зависит от длины волны падающего света, температуры раствора и природы растворенного вещества и не зависит от толщины поглощающего слоя и концентрации растворенного вещества. Молярный коэффициент светопоглощения (ε) отражает индивидуальные свойства окрашенных соединений и являются их определяющей характеристикой. Например:
ε индивидуальных веществ (растворов солей Cu, Co, Ni) достигает всего нескольких единиц.
 .
.Молярный коэффициент поглощения [Cu(NH3)4]2+ достигает – 500-600.
ε комплексов с органическими лигандами – десятки тысяч.
ε дитизоната цинка равен 94000
ε дитизоната меди равен 45000
ε сульфосалицилата железа равен 2000
Молярный коэффициент светопоглощения является мерой чувствительности данной фотометрической реакции. Т.е. чем больше ε, тем меньшую концентрацию вещества в растворе можно определить. Таким образом, повышение чувствительности может быть достигнуто в первую очередь выбором таких реакций, в результате которых образуются соединения, обладающие большими значениями ε. Обычно значения ε для реакций, используемых в спектрофотометрии, имеют порядок 102 – 105. Наибольшее экспериментально найденное значение ε имеет порядок 105.
Молярный коэффициент
светопоглощения бывает истинным и
кажущимся (средним). По градуировочному
графику вычисляют среднюю величину ε
по формуле
![]() (17). Также среднее значение ε можно найти
в справочнике. Для расчета истинного
значения
(17). Также среднее значение ε можно найти
в справочнике. Для расчета истинного
значения
![]() по формуле (17) необходимо выполнение
ряда условий:
по формуле (17) необходимо выполнение
ряда условий:
излучение, падающее на исследуемый объект, должно быть строго монохроматичным;
при данной длине волны должен поглощать только один тип частиц;
истинная концентрация данных поглощающих частиц в растворе должна быть известна;
данный индивидуальный тип частиц не должен взаимодействовать ни с какими посторонними компонентами раствора, в том числе и с растворителем;
на поглощение данных частиц не должна влиять ионная сила раствора.
Каждое из этих условий практически трудно выполнимо. Таким образом, истинное значение ε учитывает все химические равновесия, способные существовать в данном растворе. Значение ε характеризует два существенно важных свойства поглощающей системы:
Во-первых, постоянство значения ε говорит о соблюдении закона поглощения в определенном интервале концентраций. Если при изменении концентраций реагирующих веществ изменяется среднее значение ε, то это указывает на возможность возникновения побочных процессов (изменение степени диссоциации комплекса, полимеризация, ступенчатое образование комплексов и т.д.). Это позволяет спектрофотометрически исследовать состояние веществ в растворе.
Во-вторых, значение ε удобно использовать для сравнительной оценки чувствительности фотометрической реакции.
