
- •Глава 11 Специальные методы анализа состава и структуры веществ
- •11.1 Методы рентгеновского анализа
- •11.1.1 Рентгенофазовый анализ (метод рфа)
- •11.1.2 Условия возникновения дифракции на кристаллах
- •11.1.3 Дифракция на кристаллах. Понятие элементарной ячейки.
- •11.1.4 Рентгеноспектральный анализ (рса)
- •11.2 Масс-спектрометрия и ее применение в анализе
- •11.2.2 Техника проведения масс-спектрометрии.
- •11.2.2 Понятие массы в масс-спектрометрии
- •11.2.3 Типы дефрагментации молекул при воздействии эу
- •11.2.4 Примеры идентификации масс-спектров
- •11.3 Ядерный магнитный резонанс (метод ямр).
- •11.3.1 Техника получения спектров ямр
- •11.3.2 Основные характеристики спектра ямр
- •11.3.3 Основные правила анализа спектров ямр (пмр)
- •11.3.4 Химические сдвиги в отдельных классах органических соединений
- •11.3.4 Пример анализа спектра пмр
- •11.4 Гибридные методы анализа
- •11.4.1 Общее понятие «гибридных (комплексных) методов анализа»
- •11.4.2 Примеры применения гибридных установок.
11.1.4 Рентгеноспектральный анализ (рса)
Рентгеноспектральный анализ выполняется на установках, основной частью которых, как и в методе РФА, является рентгеновская трубка (рисунок 11.9).
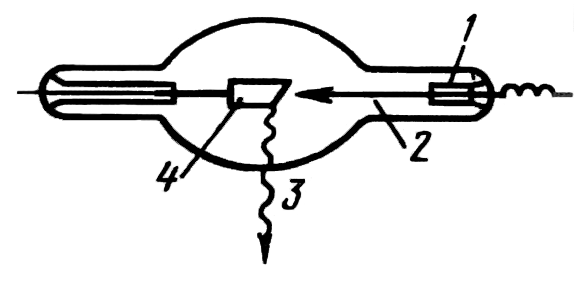
Рисунок 11.9. Строение рентгеновской трубки:
1 – катод (источник электронов); 2 – поток электронов высокой энергии;
3 – рентгеновское излучение; 4 – анод (антикатод).
Возникновение жесткого рентгеновского излучения происходит за счет квантовых переходов внутренних электронов в результате облучения вещества потоком электронов высокой энергии (см. выше описание механизма возникновения характеристического рентгеновского излучения). Поскольку квантовые переходы электронов в атомах различных элементов отличаются по энергии, то частота рентгеновского излучения будет зависеть от строения атома. Математически эту зависимость выражает закон Мозли: длина волны рентгеновского излучения атомов пропорциональна атомному номеру элемента Z (уравнение 11.3).
![]() (11.3)
(11.3)
где
– длина волны характеристического
рентгеновского излучения; а и b
– константы, одинаковые для линий данной
серии (![]() ,
,
![]() или
или
![]() ).
).
Электронные переходы, объясняющие возникновение различных серий рентгеновского излучения показаны на рисунке 11.10, а зависимость длины волны от атомного номера элемента – на рисунке 11.11
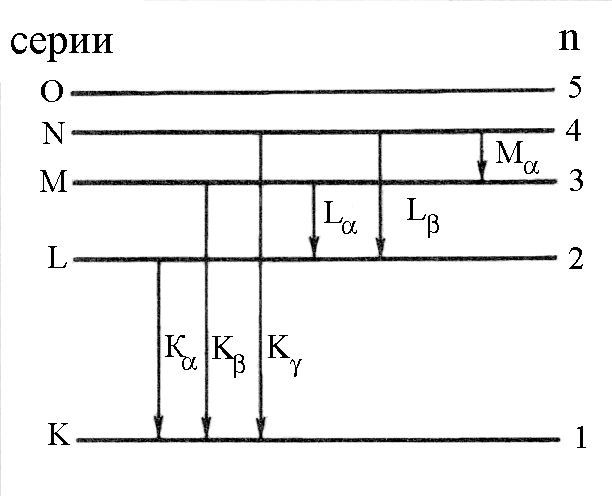
Рисунок 11.10 Схема энергетических переходов при получении
рентгеновского спектра (n – главное квантовое число).
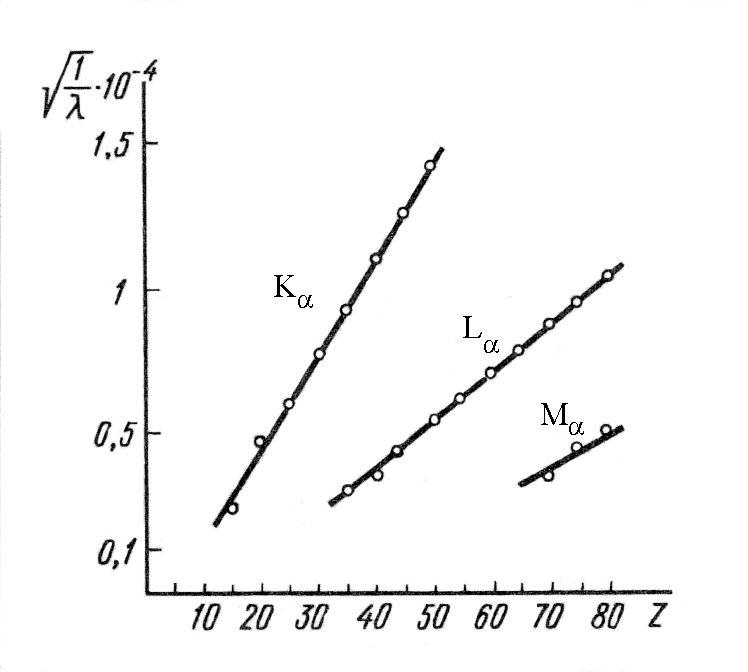
Рисунок 11.11 Зависимость длин волн рентгеновского излучения
от атомного номера элемента для спектральных серий.
Анализ рентгеновского
спектра позволяет выполнять качественные
и количественные определения элементов
в материалах сложного состава.
Охарактеризовать равноценность
химических связей однотипных элементов
в соединении. По рентгеновским спектрам
рассчитываются эффективные заряды
атомов
![]() ,
благодаря чему можно судить о типе
химической связи в соединении.
,
благодаря чему можно судить о типе
химической связи в соединении.
Если атом в соединении имеет эффективный заряд , то линии его спектра окажутся смещенными, по сравнению с линиями спектра свободного атома, на некоторую величину. Это дает возможность рассчитать значение и определить энергию связи 1s- электронов (рисунок 11.12).
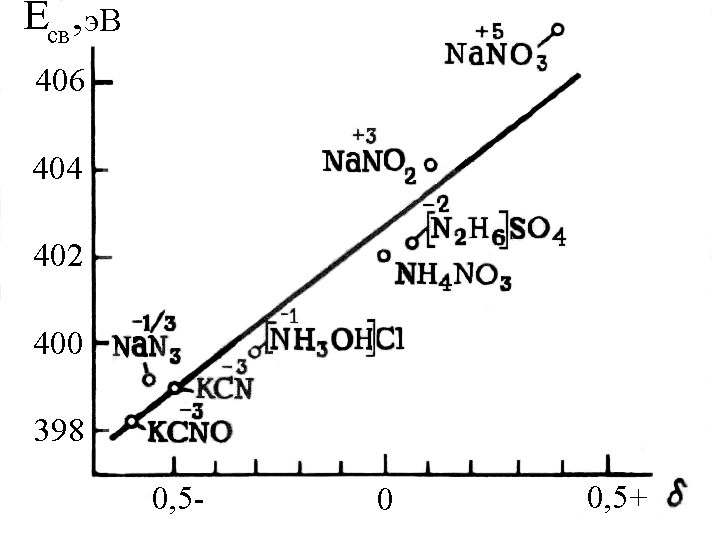
Рисунок 11.12. Зависимость энергии связи 1s-электронов атомов азота
в соединениях от величины эффективного заряда атома азота.
Рентгеновскую дифракцию нередко совмещают с дифракцией нейтронов на ядрах атомов. Эти два метода фактически дополняют друг друга и позволяют получить надежную информацию о распределении электронной плотности в молекулах кристаллов.
11.2 Масс-спектрометрия и ее применение в анализе
Масс-спектрометрия (МС) используется в вещественном и молекулярном анализе для установления молекулярной массы веществ и наиболее устойчивых структурных единиц. Метод основан на ионизации молекул анализируемого вещества (аналита) путем последующего разделения ионов по величине отношения их массы к заряду (m/z). По масс-спектру можно определить молекулярную массу; молекулярную формулу (брутто-формулу) и структуру химического вещества. На основании этого можно выделить несколько основных направления применения масс-спектрометрического анализа:
анализ структуры и состава органических соединений;
неорганический синтез
механизм реакций в органическом синтезе;
газофазные ионные реакции;
локальный анализ поверхности;
анализ биомакромолекул;
анализ лекарственных препаратов и ксенобиотиков;
изотопные реакции.
Приведем значение основных терминов, применяемых в масс-спектрометрии:
аналит – компонент пробы вещества, выделенный для дальнейшего испытания (обычно в методах МС и ЯМР);
азотное правило – позволяет определить четность массового числа молекулярного иона вещества аналита, содержащего такие элементы, как C, H, O, S и галогены;
детектор масс – электронный умножитель или иной прибор, предназначенный для регистрации величины ионного тока;
ионный кластер – набор пиков в масс-спектре с близкими значениями m/z, обусловленный существованием стабильных изотопов;
масс-спектр – запись развертки ионного пучка в соответствии со значением массового числа m/z;
масс-спектрометр – сложное устройство, часто в комбинации с газовым хроматографом или термоанализатором, предназначенное для анализа ионного и изотопного состава различных веществ;
массовое число m/z – число, равное отношению молекулярной массы иона к его заряду; для однозарядных ионов оно числено равно молекулярной массе
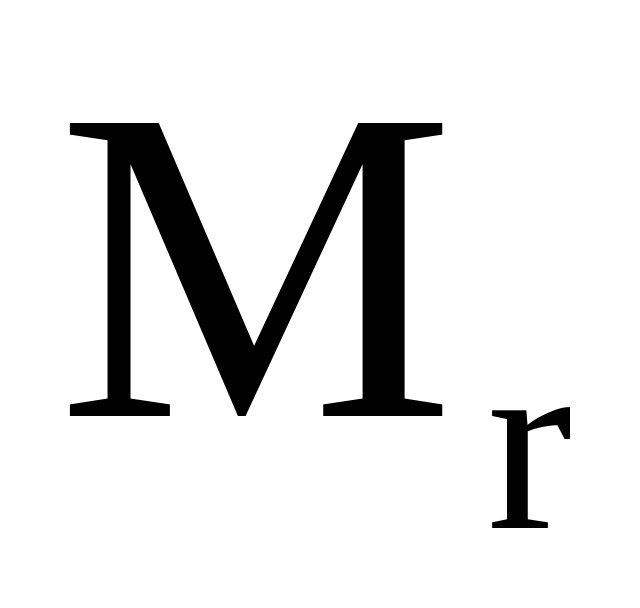 иона или радикала;
иона или радикала;молекулярный ион
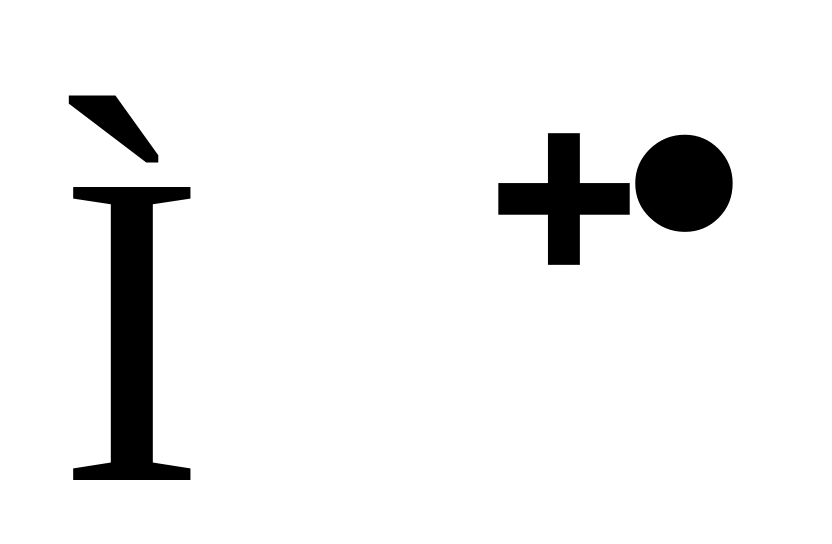 или
катион-радикал – положительно
заряженный ион, образующийся за счет
потери электрона молекулой вещества-аналита
в результате электронного удара.
Массовое число катион-радикала
соответствует молекулярной массе
аналита;
или
катион-радикал – положительно
заряженный ион, образующийся за счет
потери электрона молекулой вещества-аналита
в результате электронного удара.
Массовое число катион-радикала
соответствует молекулярной массе
аналита;НЭП – неподеленная электронная пара;
осколочный ион – ион, образующийся в результате дефрагментации молекулы вследствии разрыва химической связи;
перегруппировка – вторичная реакция в ионном пучке между осколочными ионами и радикалами, приводящая к образованию новых типов устойчивых фрагментов;
фрагментация (дефрагментация) – реакция разрыва химической связи в молекуле аналита под действием ЭУ с образованием более мелких фрагментов: осколочных ионов, радикалов и нейтральных молекул;
