
- •Лекарственные растения и сырьё, содержащие Витамины.
- •Классификация витаминов
- •Классификация лекарственного растительного сырья:
- •Основные формулы витаминов:
- •Распространение витаминов в растительном мире. Влияние факторов внешней среды и онтогенеза на накопление витаминов.
- •Особенности заготовки, сушки и хранения сырья, содержащего витамины.
- •Физико-химические свойства
- •Качественное определение
- •Количественное определение
- •Пути использования сырья, содержащего витамины.
- •Медицинское применение сырья и препаратов, содержащих витамины.
- •Калина обыкновенная
- •Сем. Жимолостные — Caprifoliaceae
- •Крапива двудомная — urtica dioica l. Сем. Крапивные — Urticaceae
- •Ноготки лекарственные –
- •Сем. Астровые — Asteraceae
- •Пастушья сумка —
- •Сем. Капустные — Brassicaceae
- •Рябина обыкновенная —
- •Сем. Розоцветные — Rosaceae
- •Череда трехраздельная —
- •Сем. Астровые — Asteraceae
- •Шиповник майский (ш. Коричный) —
- •И другие виды. Сем. Розоцветные — Rosaceae.
Качественное определение
Аскорбиновая кислота. Качественное обнаружение аскорбиновой кислоты основано на ее высокой восстановительной способности.
1. При действии на аскорбиновую кислоту раствором нитрата серебра происходит восстановление серебра, при этом аскорбиновая кислота окисляется в кетоформу:
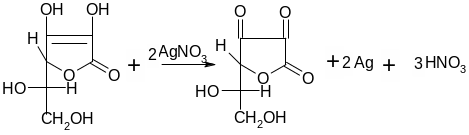
2. При действии на аскорбиновую кислоту реактивом Феллинга медь восстанавливается до гемиоксида меди красного цвета:
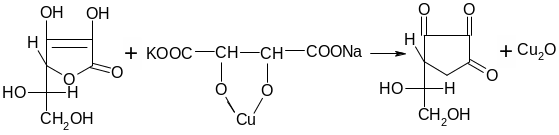
3. При действии раствором перманганата калия раствор обесцвечивается вследствие восстановления марганца до Mn2+:
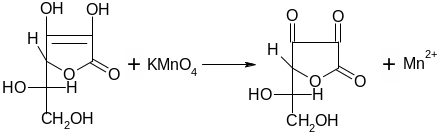
4 .
При взаимодействии аскорбиновой кислоты
с феррицианидом калия в присутствии
разведенной соляной кислоты и с
последующим добавлением раствора
трихлорида железа образуется берлинская
лазурь, окрашивающая раствор в синий
цвет:
.
При взаимодействии аскорбиновой кислоты
с феррицианидом калия в присутствии
разведенной соляной кислоты и с
последующим добавлением раствора
трихлорида железа образуется берлинская
лазурь, окрашивающая раствор в синий
цвет:
3H4[Fe(CN)6] + 4FeCl3→ 12HCl + Fe[Fe(Fe(CN)6]3
берлинская лазурь
5. Аскорбиновая кислота с солью железа (II) образует аскорбинат железа фиолетового цвета:

H2O
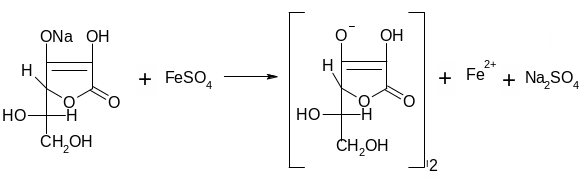
6. Иод обесцвечивается от действия аскорбиновой кислоты:
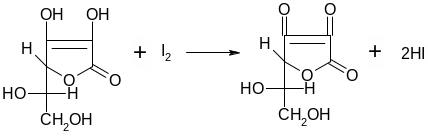
Перечисленные выше реакции можно провести с выделенной из сырья и очищенной от сопутствующих веществ субстанцией аскорбиновой кислоты.
В сырье аскорбиновую кислоту в основном определяют методом тонкослойной хроматографии после экстракции водой. В качестве сорбента используют силикагель G, полиамид, оксид алюминия, пластинки «Силуфол». Подвижной фазой чаще всего является система растворителей: ледяная уксусная кислота-ацетон-метанол-бензол(5:5:20:70) или (3:3:10:24); хлороформ - этилацетат (1:1); этилацетат - ледяная уксусная кислота (80:20); этанол - гексан (1:3).
После хроматографирования пластинку высушивают и для обнаружения аскорбиновой кислоты обрабатывают следующими реактивами: раствором 2,6-дихлорфенолиндофенолята натрия (аскорбиновая кислота проявляется в виде белых пятен на розовом фоне), щелочным раствором нитрата серебра (проявляется в виде темно-серых пятен), этанольным раствором фосфорномолибденовой кислоты (проявляется в виде темно-синих пятен на желто-зеленом фоне).
Каротиноиды. Для качественного обнаружения каротиноидов на хроматограмме используют их свойства образовывать с кислотами продукты разного цвета. Для этого применяют соляную, серную, фосфорную, азотную, муравьиную и трихлоруксусную кислоты. β-каротин с концентрированной азотной кислотой окрашивается в синий цвет, переходящий в зеленый, потом в желтый; β-каротин с концентрированной серной кислотой дает синюю окраску; с раствором хлорида сурьмы (III) в хлороформе (реакция Карра-Прайса) образуются продукты синего цвета. В сырье каротиноиды можно определить при помощи бумажной и тонкослойной хроматографии. Для этого проводят многократную экстракцию каротиноидов из сырья неполярными растворителями, такими как ацетон, спирт, петролейный эфир, или смесью этанол-ацетон (1:3).
Хроматографируют каротиноиды на бумаге в системе петролейный эфир-бензол (1:15). Для хроматографирования каротиноидов при помощи тонкослойной хроматографии используют следующие сорбенты: силикагель G; оксид алюминия; крахмал; оксиды кальция, магния; пластинки «Силуфол». В качестве системы растворителей применяют бензол-этиловый спирт (80:20), циклогексан-эфир (80:20), петролейный эфир-бензол-метанол (60:15:4), хлороформ-этиловый спирт (9:1). Пластинки, на которые нанесена смесь оксида магния и гидроксида кальция в бензоле, хроматографируют в системе бензол-н-гексан—этанол (40:20:1).
Для обработки хроматограмм часто применяют фосфорномолибденовую кислоту. В этом случае на желтом фоне каротиноиды проявляются в виде синих пятен при нагревании пластинки до 80 °С.
Витамин К1. Наличие этого витамина в сырье в основном определяют методом тонкослойной хроматографии после экстракции хлороформом или этиловым спиртом. В качестве сорбентов используют оксид алюминия, силикагель G, пластинки «Силуфол» в системах растворителей: бензол-хлороформ (1:1) бензол-ацетон (9:1), бензол-петролейный эфир (1:1), гексан-эфир (8:2).
В УФ-свете на хроматографической пластинке витамин K1 проявляется в виде пятна с зелено-желтой флуоресценцией. Для обнаружения витамина K1 на хроматографических пластинах применяют 95% серную кислоту, 60% хлорную кислоту и 65% азотную кислоту. Витамин K1 проявляется в виде бурых пятен. При обработке хроматограммы парами йода и после смачивания ее водой витамин К, проявляется в виде фиолетового пятна. После обработки 0,25% раствором родамина В, витамин K1 проявляется в УФ-свете в виде пятна фиолетового цвета.
Токоферолы в экстрактах определяют при помощи тонкослойной хроматографии на пластинках силикагель G в системе растворителей этилацетат-бензол (3:7), циклогексан-н-гексан-изопропиловый эфир-аммиак (20:20:10:1); петролейный эфир-бензол (1:1). Их обрабатывают раствором фосфорномолибденовой кислоты. При этом токоферолы образуют темно-синие пятна; с концентрированной азотной кислотой при нагревании хроматограммы до 80 °С - токоферолы дают пятна красно-оранжевого цвета.
