
- •1. Основные классы неорганических соединений
- •2. Строение атома
- •3. Химическая связь
- •4. Окислительно-восстановительные реакции
- •5. Химическая термодинамика. Кинетика химических процессов. Химическое равновесие.
- •6. Растворы. Способы выражения содержания веществ в растворе
- •3. Выполните расчеты, связанные с переходом от одной концентрации к другой
- •7. Физико-химические свойства растворов неэлектролитов и электролитов
- •8. Электролитическая диссоциация
- •9. Химические свойства металлов. Гальванический элемент. Коррозия металлов. Электролиз
- •10. Комплексные соединения
- •Оглавление
- •1. Основные классы неорганических соединений……………….………4
6. Растворы. Способы выражения содержания веществ в растворе
1. Рассчитайте массу растворенного вещества и объем растворителя (для раствора с заданной массовой долей) в задачах с №1 – №26; и объем более концентрированного раствора в задачах №27 – №56, необходимых для приготовления растворов. Плотности растворов приведены в приложении 3. Опишите методику приготовления данных растворов:
0,8 л раствора с массовой долей хлорида железа (III) 5% (раствора = 1049 кг/м3), исходя из кристаллогидрата FeCl37H2O.
0,65 л раствора с массовой долей сульфата меди (II) 8% (раствора = 1084 кг/м3), исходя из кристаллогидрата CuSO45H2O.
0,8 л раствора с массовой долей карбоната натрия 2% (раствора = 1019 кг/м3), исходя из кристаллогидрата Na2CO310H2O.
0,75 л раствора с массовой долей сульфата магния 6% (раствора = 1060 кг/м3), исходя из кристаллогидрата MgSO47H2O.
800 мл раствора с массовой долей хлорида бария 6% (раствора = 1053 кг/м3), исходя из кристаллогидрата ВаCl22H2O.
1,2 л раствора с массовой долей сульфата натрия 6% (раствора = 1053 кг/м3), исходя из кристаллогидрата Na2SO410H2O.
700 мл раствора с массовой долей хлорида меди (II) 8% (раствора = 1076 кг/м3), исходя из кристаллогидрата СuCl22H2O.
500 мл 0,1 н. раствора Cu(NO3)2 (fэкв =
 ),
исходя из кристаллогидрата Cu(NO3)23H2O.
),
исходя из кристаллогидрата Cu(NO3)23H2O.200 мл 0,2 н. раствора FeSO4 (fэкв = ), исходя из кристаллогидрата FeSO47H2O.
250 мл 0,5 н. раствора FeSO4 (fэкв = ), исходя из кристаллогидрата FeSO49H2O.
500 мл 0,2 н. раствора NiSO4 (fэкв = ), исходя из кристаллогидрата NiSO47H2O.
200 мл 0,2 н. раствора СoCl2 (fэкв = ), исходя из кристаллогидрата СoCl26H2O.
500 мл 0,3 н. раствора MgSO4 (fэкв = ), исходя из кристаллогидрата
MgSO4 6H2O.
500 мл 0,25 н. раствора MgCl2 (fэкв = ), исходя из кристаллогидрата MgCl26H2O.
200 мл 0,1 н. раствора ZnSO4 (fэкв = ), исходя из кристаллогидрата ZnSO47H2O.
250 мл 0,2 н. раствора AlCl3 (fэкв =
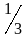 ),
исходя из кристаллогидрата AlCl36H2O.
),
исходя из кристаллогидрата AlCl36H2O.500 мл 0,25 н. раствора Al2(SO4)3 (fэкв =
 ),
исходя из кристаллогидрата Al2(SO4)3
18H2O.
),
исходя из кристаллогидрата Al2(SO4)3
18H2O.200 мл 0,2 М раствора сульфата калия-алюминия, исходя из кристаллогидрата KAl(SO4)212H2O.
200 мл 0,02 М раствора сульфата калия-хрома, исходя из кристаллогидрата KCr(SO4)212H2O.
500 мл 0,05 н. раствора CаCl2 (fэкв = ), исходя из кристаллогидрата CаCl2 6H2O.
0,5 л 0,025 М раствора сульфата магния, исходя из кристаллогидрата MgSO47H2O.
250 мл 0,05 М раствора тиосульфата натрия, исходя из кристаллогидрата Na2S2O35H2O.
500 мл 0,05 М раствора хлорида кальция, исходя из кристаллогидрата СaCl26H2O.
500 мл 0,03 М раствора карбоната натрия, исходя из кристаллогидрата Na2CO310H2O.
1 л 0,05 М раствора хлорида алюминия, исходя из кристаллогидрата AlСl36H2O.
200 мл 0,05 М раствора сульфата натрия, исходя из кристаллогидрата Na2SO410H2O.
1,2 л раствора с массовой долей серной кислоты 20% из раствора с массовой долей H2SO4 92%.
0,6 л раствора с массовой долей серной кислоты 12% из раствора с массовой долей кислоты 60%.
0,5 л 0,1 н. раствора фосфорной кислоты (fэкв = ) из раствора с массовой долей H3РO4 49% и плотностью – 1330 кг/м3.
1 л 0,2 н. раствора хлороводородной кислоты (fэкв = 1) из раствора с массовой долей HСl 12%.
0,5 л 0,25 н. раствора серной кислоты (fэкв = ) из раствора с массовой долей H2SO4 96%.
0,2 л 0,3 М раствора хлороводородной кислоты из раствора с массовой долей HСl 20%.
0,5 л 0,25 н. раствора сульфата магния (fэкв = ) из раствора с массовой долей соли 20% и плотностью 1310 кг/м3.
0,5 л 0,03 н. раствора хлорида бария (fэкв = ) из раствора с массовой долей соли 15% и плотностью 1147кг/м3.
1 л 0,05 М раствора азотной кислоты из раствора с массовой долей кислоты 32%.
250 мл 0,25 М раствора фосфорной кислоты из раствора с массовой долей фосфорной кислоты 40% и плотностью 1254 кг/м3.
0,6 л раствора с массовой долей гидроксида натрия 16% из раствора с массовой долей NaOH 40%.
0,8 л раствора с массовой долей азотной кислоты 12% из раствора с массовой долей кислоты 56%.
0,75 л раствора с массовой долей хлороводородной кислоты 8% из раствора с массовой долей кислоты 36%.
1,2 л раствора с массовой долей серной кислоты 12% из раствора с массовой долей кислоты 60%.
0,5 л 0,1 М раствора азотной кислоты из раствора с массовой долей кислоты 32%.
0,5 л 2 н. раствора серной кислоты (fэкв = ) из раствора с массовой долей кислоты 92%.
0,2 л 0,4 н. раствора серной кислоты (fэкв = ) из раствора с массовой долей кислоты 32%.
250 мл 0,2 М раствора гидроксида натрия из раствора с массовой долей NaOH 12%.
0,5л 0,2 М раствора нитрата калия из раствора с массовой долей KNO3 70% и плотностью 1600 кг/м3.
0,5 л 1,5 М раствора хлороводородной кислоты из раствора с массовой долей кислоты 36%.
0,75 л раствора с массовой долей гидроксида калия 12% из раствора с массовой долей КOH 40%.
1 л 0,02 М раствора хлороводородной кислоты из раствора с массовой долей кислоты 36%.
500 мл 0,2 М раствора гидроксида калия из раствора с массовой долей КOH 36%.
1 л 0,6 М раствора хлороводородной кислоты из раствора с массовой долей кислоты 28%.
0,5 л 0,2 н. раствора карбоната натрия (fэкв = ) из раствора с массовой долей соли 10% и плотностью 1103 кг/м3.
0,5 л 0,02 М раствора хлорида алюминия из раствора с массовой долей соли 20% и плотностью 1157 кг/м3.
100 мл 0,05 н. раствора хлорида цинка (fэкв = ) из раствора с массовой долей соли 20% и плотностью 1186 кг/м3.
0,2 л 0,5 н. раствора сульфата меди (fэкв = ) из раствора с массовой долей CuSO4 16% и плотностью 1180 кг/м3.
250 мл 0,5 М раствора гидроксида калия из раствора с массовой долей КOH 36%.
0,5 л 0,5 н. раствора серной кислоты (fэкв = ) из раствора с массовой долей кислоты 80%.
2. Вычислите массовую долю растворенного вещества; молярную концентрацию; молярную концентрацию эквивалента; моляльность и титр для:
Раствора карбоната натрия, если в 100 мл его содержится 10 г этой соли (плотность раствора 1100 кг/м3).
Раствора с массовой долей серной кислоты 20%.
Раствора хлорида натрия, если в 200 мл его содержится 20 г этой соли (плотность раствора 1070 кг/м3).
Раствора с массовой долей хлороводородной кислоты 20%.
Раствора сульфата меди (II), если в 300 мл его содержится 5 г этой соли (плотность раствора 1010 кг/м3).
Раствора с массовой долей ортофосфорной кислоты 20%, плотность которого 1200 кг/м3.
Раствора с массовой долей азотной кислоты 28%.
Раствора азотной кислоты, в 4 л которого содержится 932 г кислоты (плотность раствора 1120 кг/м3).
Раствора, который содержит в 3 л 175,5 г карбоната калия (плотность раствора 1414 кг/м3).
Раствора с массовой долей азотной кислоты 40%.
Раствора с массовой долей ортофосфорной кислоты 40%, плотность которого 1254 кг/м3.
Раствора гидроксида калия, если в 1 кг воды растворено 666 г гидроксида калия.
Раствора хлорида алюминия, если в 200 мл его содержится 32 г соли (плотность раствора 1149 кг/м3).
10 н. раствора серной кислоты (fэкв = ), плотностью 1290 кг/м3.
0,8 М раствора сульфата железа (III), если плотность раствора 1241 кг/м3.
8 М раствора азотной кислоты, плотность которого 1246 кг/м3.
Раствора с массовой долей сульфата меди (II) 16% и плотностью 1180 кг/м3.
Раствора хлорида натрия, содержащего в 0,75 литре 8,82 г соли (плотность раствора 1012 кг/м3).
Раствора гидроксида натрия, если в 0,5 л раствора плотностью 1023 кг/м3 содержится 10 г гидроксида натрия.
Раствора, в 100 мл которого содержится 22,6 г серной кислоты (плотность раствора 1143 кг/м3).
Раствора серной кислоты, если титр его 0,0195 г/мл (плотность раствора 1143 кг/м3).
Раствора с массовой долей хлорида цинка 20%, плотность которого 1186 кг/м3.
Раствора ортофосфорной кислоты, полученной при растворении 18 г кислоты в 282 мл воды, если плотность его 1031 кг/м3.
1,4 М раствора нитрата серебра, плотность которого 1128 кг/м3.
Раствора азотной кислоты, если в 3 л его содержится 316 г кислоты (плотность раствора 1054 кг/м3).
Раствора с массовой долей хлорида кальция 20% и плотностью 1178 кг/м3.
Раствора серной кислоты, если в 1 л раствора содержится 57,7 г этой кислоты (плотность раствора 1035 кг/м3).
Раствора с массовой долей гидроксида бария 7% и плотностью 1040 кг/м3.
