
- •1. Постулати термодинаміки, їх значення для обґрунтування термодинаміки.
- •2. Другий постулат термодинаміки. Рівняння стану, їх виведення для ід. Газу і парамагнетика.
- •3. Перше начало термодинаміки. Робота, енергія, теплота.
- •4. Друге начало термодинаміки для квазістат. Процесів. Мат. Обґрунтування існування ентропії.
- •5. Начало термодинаміки для нестац. Процесів. Імовірнісний зміст ентропії.
- •6. Зв'язок термічного і калорічного рівняння стану, приклади його застосування.
- •7. Заг. Властивості термодинамічних потенціалів, їх обґрунтування.
- •8.Термодинамічні потенціали для систем зі змінною кількістю частинок. Хім. Потенціал.
- •9. Загальні умови рівноваги і стійкості
- •11. Умови стійкості однорідної системи. Детермінанти і коефіцієнти стійкості.
- •12. Перша лема Гібса. Стат. Зміст коефіцієнтів стисливості. Відносна флуктуація енергії.
- •13. Третє начало термодинаміки
8.Термодинамічні потенціали для систем зі змінною кількістю частинок. Хім. Потенціал.
Запишемо основне рівняння термодинаміки для системи, що складається з рідини та газу.
![]()
Якщо задана кількість часток пару та рідини, то виникає додаткова робота (крім PdV).

Це потенціали для системи зі змінною кількістю частинок.

V,S – екстенсивні потенціали(можуть бути віднесені к одній частинці), T,P – інтенсивні.

Хімічний потенціал – це є енергія Гібса на одну частинку.
Він є інтенсивним параметром.
![]()
Треба
ввести потенціал, який би дав можливість
знайти кількість частинок N.
Він має залежність від
![]()
9. Загальні умови рівноваги і стійкості
Будемо виходити з основного співвідношення т. д-ки для нестатичних процесів (об’єднує 1-ше і 2-ге начала для нестаціонарних процесів).
![]() (1)
(1)
умови рівноваги і стійкості будемо знаходити для конкретних умов
Ізольована система
1)
![]()
![]()
процеси самі ідуть в бік збільшення S
![]() в
стані рівноваги S
максимальне.
Умова максимуму в варіаціях (віртуальних
змінних):
в
стані рівноваги S
максимальне.
Умова максимуму в варіаціях (віртуальних
змінних):
![]()
нехай система знаходиться в рівновазі з термостатом, не змінює V i N :
2)![]()
![]()
вільна енергія зменшується і в стані рівноваги мінімальна
![]() умова
мінімуму на варіаційній мові:
умова
мінімуму на варіаційній мові:
![]()
3)![]()
![]()
![]()
аналогічно і для інших процесів. Всі потенціали в стані рівноваги мінімальні:
![]()
![]()
![]()
умова, коли перша варіація =0, дає умову рівноваги. Коли 2-га вар-я >0 дає мову стійкості (не для ізольованої системи).
11. Умови стійкості однорідної системи. Детермінанти і коефіцієнти стійкості.
У
стані рівноваги потенціали мінімальні,
і це пов'язано з тим, що
![]() .
Будемо казати, що S,
V
I
U
мають т.з. будь-які віртуальні зміни δS,
δV,
δU.
.
Будемо казати, що S,
V
I
U
мають т.з. будь-які віртуальні зміни δS,
δV,
δU.
Якщо в системі з'явилися такі зміни, то нам необх. знайти такі умови, щоб система завдовольняла флюктуаціям повернулась в попередній стан.
![]() —
диференціал
U.
—
диференціал
U.
![]() —
друга
варіація U.
Перша варіація дає умову рівноваги,
друга — стійкої рівноваги. Вираз δ2U
– квадратична форма:
—
друга
варіація U.
Перша варіація дає умову рівноваги,
друга — стійкої рівноваги. Вираз δ2U
– квадратична форма:
![]() .
.
Умови невід'ємності КФ полягають у тому, що визначник цієї форми і всі його головні мінори позитивні.
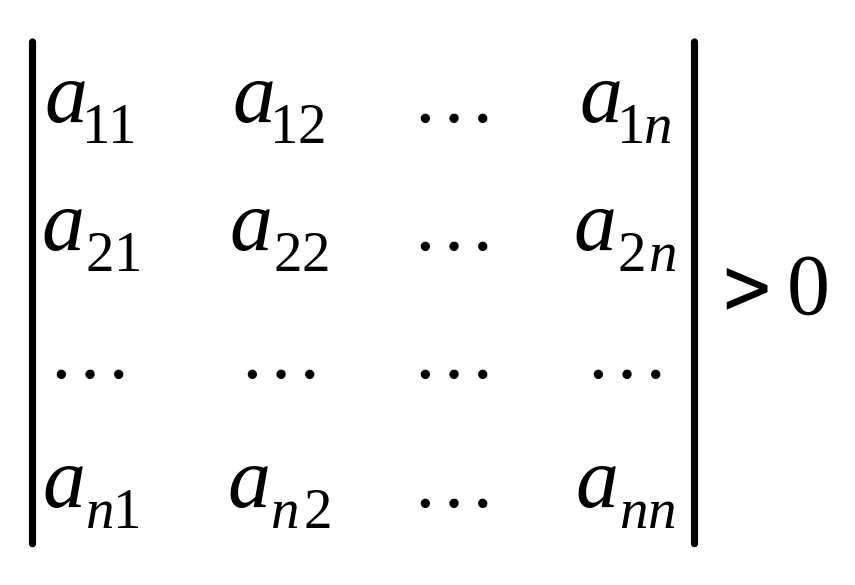 ,
,
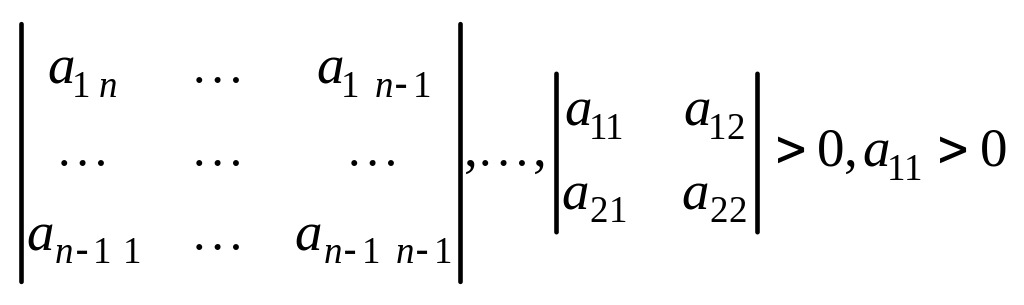 .
.
Це т.з. Критерій Сільвестра.

 —
адіабатні
коефіцієнти стійкості
—
адіабатні
коефіцієнти стійкості
Ця
матриця дорівнює якобіану
![]() D
– детермінант Сільвестра.
D
– детермінант Сільвестра.
Якщо
є функції
![]() ,
то визначник символічно записується
як
,
то визначник символічно записується
як
 і
зветься Якобіаном. Властивості Якобіана:
1) будь-яку похідну можна записати як
і
зветься Якобіаном. Властивості Якобіана:
1) будь-яку похідну можна записати як
![]() ;
2)
;
2)![]() ;
3)
;
3) — обернений Якобіан. Теорія якобіанів
використовується при переході від одних
змінних до інших; 4)
— обернений Якобіан. Теорія якобіанів
використовується при переході від одних
змінних до інших; 4)
![]() .
.
Назвемо Якобіан коефіцієнтом стійкості. Для того, щоб система була у стані термодинамічної рівноваги, необхідно щоб D, який являє собою якобіан, збудований з похідних сил по відповідним координатам і всі його головні мінори були позитивні. Величини на головній діагоналі
![]() і
і
![]() назвемо адіабатними коефіцієнтами
стійкості (АКС).
назвемо адіабатними коефіцієнтами
стійкості (АКС).
![]()
— коефіцієнт Гука (шв. звука). Обернена величина — стисливість.
![]() — адіабатне
поширення.
— адіабатне
поширення.
Всі похідні в ΔС беруться по термодинамічних координатах. Кожній координаті відповідає термодинамічна сила. V, S = const => ідуть ізохорні адіабатні процеси. Практично легше підтримати const P i T (сталі сили). Перейдемо від похідних по координатах до похідних по силах. Використаємо третю властивість і побудуємо зворотн. ΔС.
![]()

![]() ,
,
![]() —
обернені коефіцієнти стійкості . Це
ізодинамічні величини при сталих силах,
а величини
—
обернені коефіцієнти стійкості . Це
ізодинамічні величини при сталих силах,
а величини
![]() ,
,
![]() назвемо ізодинамічними коефіцієнтами
стійкості(ІКС). За стійкості системи
відповідають: D,
АКС, ІКС, а не будь-які величини. Перш
ніж дослідити будь-які системи, необхідно
впевнитись, що вона стійка.
назвемо ізодинамічними коефіцієнтами
стійкості(ІКС). За стійкості системи
відповідають: D,
АКС, ІКС, а не будь-які величини. Перш
ніж дослідити будь-які системи, необхідно
впевнитись, що вона стійка.

Знайдемо відповідність між ІКС та АКС.
![]()
![]() .
Перейдемо від величини
до Якобіану (детермінанту). Робимо
роздвижку
.
Перейдемо від величини
до Якобіану (детермінанту). Робимо
роздвижку![]() ,
де
—
адіабатний термічний коефіцієнт
стійкості.
,
де
—
адіабатний термічний коефіцієнт
стійкості.
![]() —
ізодинамічний
термічний коефіцієнт стійкості.
—
ізодинамічний
термічний коефіцієнт стійкості.
Розглянемо АКС:
![]()
![]() ,
,
![]() .
.
Це рівняння пов'язує ΔС з КС.
КС мають прозорий статичний зміст. Вони обернено пропорційні флуктуаціям системи.
