
- •Содержание
- •Введение
- •Требования к выполнению домашнего задания по расчету термодинамических циклов тепловых двигателей
- •Основные понятия и расчетные соотношения
- •Первое начало термодинамики
- •Термодинамические процессы изменения состояния
- •Круговые процессы (циклы)
- •Второе начало термодинамики
- •Термодинамические циклы поршневых двигателей внутреннего сгорания
- •Термодинамические циклы газотурбинных установок
- •Пример расчета термодинамического цикла поршневого двигателя внутреннего сгорания
- •Пример расчета термодинамического цикла газотурбинной установки
- •Контрольные вопросы
- •Литература
Первое начало термодинамики
Первое начало термодинамики является математическим выражением закона сохранения и превращения энергии.
Первое начало термодинамики по балансу рабочего тела для 1 простого тела записывается следующим образом:
![]() ,
(8)
,
(8)
где
![]() – удельный приведенный термодинамический
теплообмен;
– удельный приведенный термодинамический
теплообмен;
![]() – количество теплоты, подведенное к 1
кг
системы извне;
– количество теплоты, подведенное к 1
кг
системы извне;
![]() – удельное количество теплоты внутреннего
теплообмена в
процессе 1-2,
– удельное количество теплоты внутреннего
теплообмена в
процессе 1-2,
![]() ;
;
![]() – изменения удельной внутренней энергии
и удельной энтальпии газа,
;
– изменения удельной внутренней энергии
и удельной энтальпии газа,
;
![]() – удельная термодинамическая и
потенциальная работы в обратимых
процессах,
;
– удельная термодинамическая и
потенциальная работы в обратимых
процессах,
;
![]() ;
;
![]() – удельная внешняя термодинамическая
работа,
– удельная внешняя термодинамическая
работа,
![]() – удельная термодинамическая работа
необратимых потерь.
– удельная термодинамическая работа
необратимых потерь.
Внутренняя энергия, энтальпия и энтропия 1 идеального газа в j-м состоянии согласно закону Джоуля находятся по следующим соотношениям:
![]() ;
(9)
;
(9)
![]() ;
(10)
;
(10)
![]() ,
(11)
,
(11)
где
![]() ,
,
![]() – вторые средние изобарная и изохорная
теплоемкости,
– вторые средние изобарная и изохорная
теплоемкости,
![]() ;
;
![]() ;
;
![]() .
.
Термодинамические процессы изменения состояния
Любое изменение термодинамического состояния системы называется термодинамическим процессом.
Большинство термодинамических процессов изменения состояния простых тел описывается уравнением политропы с постоянным показателем
![]() ,
(12)
,
(12)
где
n
– показатель политропы, в общем случае
изменяющийся в пределах
![]() .
.
Термодинамическая
и потенциальная работы 1
газа определяются в координатах
![]() как площади между кривой процесса и
соответствующими координатами (рис.
1).
как площади между кривой процесса и
соответствующими координатами (рис.
1).
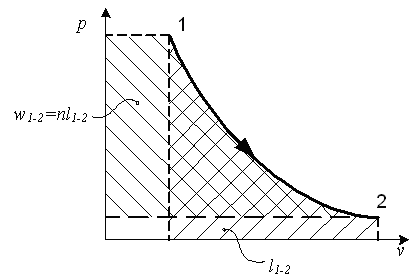
Рис. 1. Политропический процесс
Удельные термодинамическая и потенциальная работы в политропических процессах можно рассчитать по следующим соотношениям:
![]() ;
(13)
;
(13)
![]() ,
(14)
,
(14)
где
![]() – характеристика расширения или сжатия,
– характеристика расширения или сжатия,
![]() .
(15)
.
(15)
Характеристика расширения или сжатия для идеальных газов может быть определена по формуле
![]() .
(15.а)
.
(15.а)
Количество теплоты, подводимое или отводимое от 1 кг идеального газа в политропном процессе, может быть рассчитано по следующему соотношению:
![]() .
(16)
.
(16)
Расчетные соотношения для определения удельных значений термодинамической и потенциальной работ и теплообмена в простейших процессах имеют следующий вид:
– изобарный
процесс (![]() )
)
![]() ,
(17)
,
(17)
![]() ,
(18)
,
(18)
![]() ;
(19)
;
(19)
– изохорный
процесс (![]() )
)
![]() ,
(20)
,
(20)
![]() ,
(21)
,
(21)
![]() ;
(22)
;
(22)
– изопотенциальный
процесс (для
идеального газа – изотермический
процесс) (![]() )
)
![]() ;
(23)
;
(23)
– адиабатный
процесс (![]() )
)
![]() ,
(24)
,
(24)
![]() .
(25)
.
(25)
Внутренняя
энергия, энтальпия и энтропия являются
функциями состояния. В связи с этим,
изменение их значений в процессе будет
определяться как разность конечного
(![]() )
и начального (
)
и начального (![]() )
значений
)
значений
![]() ,
(26)
,
(26)
где
z
– функция состояния (![]() ).
).
