
- •Лекция 1
- •Часть 1. Металловедение и термическая обработка металлов.
- •2. Классификация материалов и требования к ним.
- •3. Металлы и их свойства. Металлическая связь.
- •4. Кристаллическое строение металлов. Типы кристаллических решеток.
- •5Анизотропия свойств кристаллов.
- •Лекция 2 процессы плавлЕнИя и кристаллизации металлов
- •2. Процесс зарождения и роста кристаллов.
- •3. Строение слитков.
- •4. Скорость процесса кристаллизации.
- •5. Величина зерна.
- •Методы исследования кристаллического строения металла.
- •7Диффузия.
- •Лекция 3 превращения металлов в твердом состоянии. Металлические сплавы.
- •2. Магнитные превращения.
- •3. Основные понятия о сплавах.
- •Механические смеси.
- •Химические соединения в сплавах.
- •Лекция 4 диаграммы состояния
- •2.Принцип построения диаграммы состояния.
- •Диаграмма состояния для сплавов, образующих механические смеси. Ι тип диаграммы состояния.
- •4.Анализ диаграмм состояния двойных сплавов. Правило фаз. Правило отрезков.
- •5. Диаграма состояния п типа (с неограниченной растворимостью в твердом состоянии).
- •6. Диаграмма состояния ш типа.
- •7.Связь между свойствами сплава и типом диаграммы состояния. Правило Курнакова.
7Диффузия.
Многие процессы, протекающие в металлах и сплавах, в том числе кристаллизация, носят диффузионный характер.
В кристаллическом теле под диффузией понимают перемещение атомов на расстояния, превышающие средние межатомные расстояния данного вещества. Если процесс перемещения атомов не связан с изменением концентрации в отдельных объемах, то процесс называется самодиффузией.
Самодиффузия – это перемещение атомов основного металла в своей собственной кристаллической решетке.
Диффузия, сопровождающаяся изменением концентрации, происходит в сплавах с повышенным содержанием примесей и называется гетеродиффузией.
Каждый атом совершает случайные блуждания, т.е. ряд скачков между различными равновесными положениями в решетке. Любая атомная теория должна начинаться с рассмотрения механизма, объясняющего, каким образом данный атом перемещается в решетке.
Для описания процесса диффузии в твердом теле предложено несколько возможных механизмов: циклический, обменный, вакансионный, межузельный.
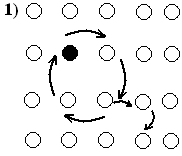 По циклическому механизму
диффузии перескок представляет собой
совместное перемещение группы атомов
(вращение). Такое вращение не требует
большой энергии, но маловероятно.
По циклическому механизму
диффузии перескок представляет собой
совместное перемещение группы атомов
(вращение). Такое вращение не требует
большой энергии, но маловероятно.
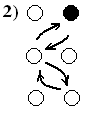 Обменный
механизм является частным случаем
циклического (гр. из 2-х атомов) и
заключается в обмене соседних атомов.
Обменный
механизм является частным случаем
циклического (гр. из 2-х атомов) и
заключается в обмене соседних атомов.
 При вакансионном
механизме диффузии атомы обмениваются
местами с вакансией.
При вакансионном
механизме диффузии атомы обмениваются
местами с вакансией.
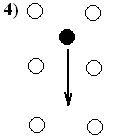 При
межузельном механизме атом переходит
в состояние равновесия в ближайшее
междоузлие.
При
межузельном механизме атом переходит
в состояние равновесия в ближайшее
междоузлие.
В металлах диффузия преимущественно осуществляется по вакансионному механизму. При диффузии в металле элементов с малым атомным радиусом (С, N2, H2) механизм межузельный.
Скорость диффузии определяется количеством вещества m, диффундирующего через единицу площади поверхности раздела в единицу времени. m зависит от градиента концентрации элемента dc/dx в направлении, перпендикулярном к поверхности раздела и пропорционально коэффициенту Д: dx
m= - Д dc - закон Фика.
Знак « - » указывает, что диффузия протекает в направлении от объемов с большей концентрацией к объемам с меньшей концентрацией.
Коэффициент Д [см2/с] – количество вещества, диффузирующего через единицу площади 1 см2 в единицу времени (1 с.) при перепаде концентраций равном 1. Коэффициент зависит от природы сплава, размеров зерна и от температуры.
“Д” в твердых сплавах крайне чувствителен к дефектам кристаллической решетки, возникающим при нагреве, напряжениях, деформациях и других воздействиях. Увеличение числа дефектов (главным образом вакансий) облегчает перемещение атомов и приводит к росту “Д”.
Лекция 3 превращения металлов в твердом состоянии. Металлические сплавы.
Полиморфизм.
Магнитные превращения.
Основные понятия о сплавах.
Механические смеси.
Химические соединения в сплавах.
Твердые растворы.
Атомы данного элемента могут образовать, если исходить только из геометрических соображений, любую кристаллическую решетку. Однако, реально существующим типом решетки, наиболее устойчивым, является решетка с низким запасом свободной энергии.
В ряде случаев при изменении температуры и давления для одного и того же металла становится устойчивой другая решетка.
Существование металла (вещества) в нескольких кристаллических формах носит название полиморфизма, или аллотропии.
Различные кристаллические формы одного вещества называются полиморфными или аллотропическими модификациями.
Аллотропические изменения характерны для таких металлов, как Co, Al, Sn, Mn, Ti, Zn, U, Fe. Это металлы, имеющие большое практическое значение.
Аллотропические формы обозначаются греческими буквами α, β, γ, δ и т.д. по мере повышения температуры. Т.е. при самой низкой температуре аллотропическая форма обозначается α. Эти индексы добавляются к соответствующим химическим символам.
Полиморфизм основан на законе устойчивости состояния с наименьшим запасом энергии, а запас свободной энергии зависит от температуры. Поэтому в одном интервале температур устойчива α-форма, а в другом – β и т.д.
Температура, при которой осуществляется переход из одной модификации в другую, называется температурой аллотропического превращения.
Полиморфные превращения происходят путем зарождения центров и роста кристаллов и имеют свои особенности для различных металлов. Рассмотрим аллотропические превращения на примере Fe.
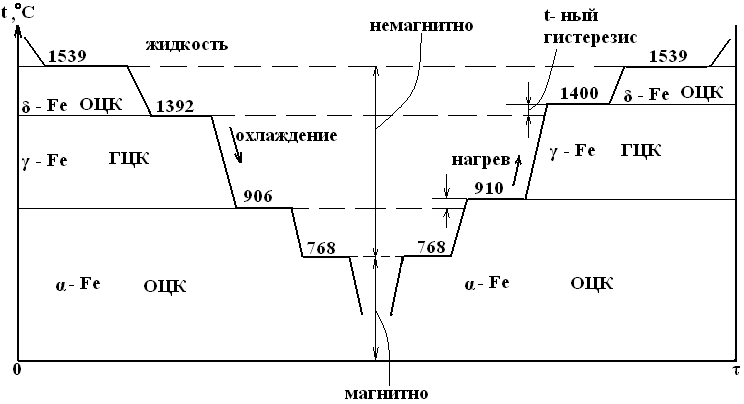
При температуре до 910 °С железо существует в форме α. При 9100С ОЦК Feα переходит в ГЦК Feγ, которая при 14000С вновь превращается в ОЦК Feα. Высокотемпературная α-решетка обозначается также δ (дельта). Таким образом, у железа одна и та же решетка устойчива в 2-х интервалах температур.
При температуре 7680С получается горизонтальный участок на кривой охлаждения, связанный не с перестройкой решетки, а с изменением магнитных свойств. Выше 7680С Fe магнитно и называют его иногда β (бэта) – Fe. Оно более пластично, вызко, обладает большей растворимостью углерода. При температуре 15390С – ОЦК трансформируется в жидкость.
Превращение одной аллотропической формы в другую при нагреве чистого металла сопровождается поглощением тепла и происходит при постоянной температуре. На термической кривой в координатах температура-время превращение отмечается горизонтальным участком. При охлаждении происходит выделение тепла (скрытой теплоты превращения), что приводит также к постоянству температуры. Вследствие переохлаждения эта температура более низка, чем при нагреве (возникает температурный гистерезис) – разница между реальными температурами плавления и кристаллизации.
Таким образом, суть аллотропических превращений заключается в переходе кристаллических решеток из одной в другую. Явление полиморфизма имеет большое практическое значение. На существовании аллотропических превращений основана термическая обработка стали.
