
- •Лекция 6-8. Агрегатные состояния вещества
- •1. Агрегатные состояния вещества
- •1.1. Плазма
- •1.2. Газообразное состояние
- •1.3. Жидкости
- •1.3.1. Жидкие кристаллы
- •1.3.1.1. Общие сведения о жидких кристаллах.
- •1.3.1.2. Открытие жидких кристаллов
- •1.3.2. Классификация жидких кристаллов
- •1.4. Твердые вещества
- •1.4.1. Аморфные вещества
- •1.4.2. Кристаллические вещества
- •1.4.2.1. Изоморфизм и полиморфизм
- •2. Рентгеноструктурный анализ
- •3. Строение кристаллов
- •3.1. Элементы симметрии
- •3.2. Кристаллические системы (типы кристаллических решеток)
- •3.3. Основные характеристики элементарной ячейки
- •3.4. Расчёт основных размеров элементарных ячеек кубической системы
- •3.5. Классификация кристаллов по типу химических связей
- •4. Атомные нарушения структуры кристалла
- •4.1. Классификация дефектов структуры
- •4.1.1. Точечные дефекты
- •4.1.2. Образование точечных дефектов
- •4.2. Линейные деффекты (дислокации)
- •4.2.1.Краевая и винтовая дислокации
- •Поверхностные дефекты
- •4.4. Плотность дислокаций
- •4.5. Широта области гомогенности
- •4.6. Индексация граней
3.2. Кристаллические системы (типы кристаллических решеток)
Всё разнообразие кристаллических решёток классифицируется по некоторым важнейшим признакам. Самое главное свойство кристалла — пространственная симметрия и по ней решётки разделены на 7 сингоний, 32 класса симметрии. Другая важная характеристика — положение атомов в элементарной ячейке, на нём основана классификация кристаллических решёток Браве.
Размер и форму элементарной ячейки можно изобразить с помощью длин трёх отрезков (a, b, c), отсекаемых на координатах (x, y, z) и трёх углов между ними (, , ). Для описания положения граней кристалла естественно пользоваться приемами аналитической геометрии, а именно системой осей координат. Но если в аналитической геометрии предпочитают декартовы координаты (угол между осями =90 0), то в кристаллографии выбирают систему координат так, чтобы оси координат были параллельны ребрам кристалла.

1. Кубическая a=b=c; ===90
2. Тетрагональная a=bc;
3. Ромбическая abc;
(орторомбическая)
4. Моноклинная abc;
5. Триклинная abc;
6. Гексагональная a=bc; =120
7. Тригональная a=b=c; ==90
(ромбоэдрическая)
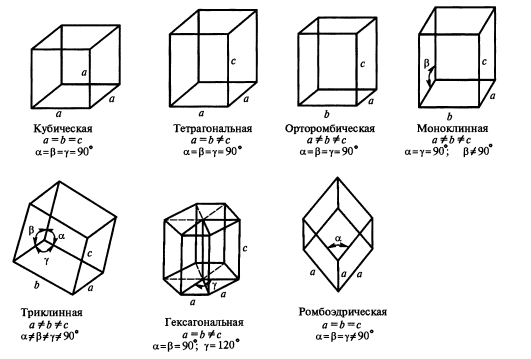
Рис. 3. Основные системы кристаллов. 7 разных способов упорядоченного расположения в пространстве одинаковых точек.


3.3. Основные характеристики элементарной ячейки
1. Важнейшей характеристикой кристаллической решётки является а – величина ребра.
2. Кратчайшее расстояние между частицами в ячейке – d.
3. Координационное число – k – число одинаковых частиц, расположенных на кратчайшем расстоянии от данной частицы.
4. Число частиц, необходимое для построения элементарной ячейки – n.
5. Эффективный (кажущийся) радиус rэф=d/2.
Рассмотрим примеры. В кубической системе можно выделить 3 вида кристаллических решеток: простая, ОЦК. и ГЦК.
а) простая кубическая решётка (ПК)

а – длина ребра (справочная величина)
d = а
k = 6 число ближайших частиц находящихся на расстоянии d.
n=⅛.8=1 – каждая частица в узле кристаллической решётки принадлежит ей лишь на 1/8, так как она принадлежит одновременно 8 кубами сходящимся в данной вершине. А вершин в кубе всего – 8.
При такой упаковке решётки одинаковыми атомами доля пространства занятого ими в одном кубе, то есть плотность элементарной кристаллической ячейки составляет = 52,4 %.
В решётке этого типа кристаллизируются в обычных условиях некоторые галогениды щелочных металлов (NaCl, KCl…) и большая часть оксидов, сульфидов, селенидов щелочноземельных металлов.
б) объёмно-центрированная кубическая решётка (ОЦК)
П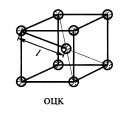 ростая+частица
в ячейке, расположенная в точке пересечения
диагоналей куба.
ростая+частица
в ячейке, расположенная в точке пересечения
диагоналей куба.
а
 (половина диагонали
куба)
(половина диагонали
куба)k=8
n=⅛.8+1=2 (поскольку одна частица находится внутри элементарной ячейки).
При такой упаковке решётки одинаковыми атомами доля пространства занятого ими в одном кубе, (плотность упаковки) составляет = 68 %.
В решётке этого типа кристаллизируются: CsCl, щелочные металлы, -Fe, -Ti, W, Mo, V, Ta, -Cr, -Fe, Nb, Ba, + некоторые актиноиды, а также при высоких температурах Hf, Zn, Mn, Te.
в) гранецентрированная кубическая решётка (ГЦК)
Простая + 6 частиц, расположенных на каждой грани в точке пересечения диагоналей квадрата.

а
 (половина диагонали
квадрата)
(половина диагонали
квадрата)k=12
n=8.⅛+6.½=4 (так как одной частице в вершинах куба добавляются ещё 6 (6.½) в серединах граней на пересечении диагоналей, а эта частица только наполовину принадлежит этой ячейке),
= 74 %.
В решётке этого типа кристаллизируются в обычных условиях: Al, Cu, Ag, Pd, Pb, Th (торий), -Fe, -Co, Ni, Rh (родий), Ir, Pt, Mn (↓T).
г) гексагональная плотная упаковка (ГПУ)
1 .
а
– длина ребра, равная стороне правильного
шестиугольника в основании призмы.
.
а
– длина ребра, равная стороне правильного
шестиугольника в основании призмы.
h
– высота призмы, которая равна
![]()
2. d=а
3. k=12
4. n=12.1/6+2.½+3=6 (в каждой вершинке призмы расположен атом, одновременно принадлежащий шести сходящимся в одной точке призмам. Вершин 12, они содержат 121/6=2 атома. В центре верхнего и нижнего оснований лежат атомы, наполовину принадлежащие данной решётке. Внутри находятся ещё 3 атома, = 74 %.
В таких решётках кристаллизируются: Be, Mg,Са, Zn,Sr, Cd, Ti, Tl, Zr, Hf, Sc, Y, -Cr, -Co, Ru, Os, Re, а так же большинство лантаноидов.
