
- •Техника безопасности
- •1. Электропроводность растворов электролитов
- •Электропроводность растворов электролитов
- •Удельная электропроводность
- •Кондуктометрическое титрование
- •Определение растворимости труднорастворимой соли.
- •Работа 1.1. Определение концентрационной зависимости удельной и молярной электропроводности сильного электролита
- •Порядок выполнения работы:
- •Работа 1.2. Определение константы диссоциации слабого электролита методом электропроводности
- •Порядок выполнения работы:
- •Работа 1.3. Кондуктометрическое титрование
- •Порядок выполнения работы:
- •Работа 1.4. Кондуктометрическое определение термодинамических параметров растворения труднорастворимого соединения
- •Порядок выполнения работы:
- •Перед выполнением работы:
- •К защите работы:
- •2. Электродвижущие силы Возникновение потенциалов на границах фаз.
- •Электродный потенциал
- •Водородный электрод
- •Измерение электродных потенциалов
- •Электрохимический (гальванический) элемент
- •Концентрационный гальванический элемент
- •Измерение эдс гальванического элемента компенсационным методом
- •Температурная зависимость эдс.
- •Электроды сравнения
- •Хлорсеребряный электрод
- •Окислительно-восстановительные электроды и их потенциалы
- •Мембранные равновесия. Стеклянный электрод
- •Кислотно-основные буферные системы
- •Механизм буферного действия
- •Буферная емкость
- •Порядок выполнения работы:
- •Порядок выполнения работы:
- •Порядок выполнения работы:
- •Окислительно-восстановительных потенциалов
- •Порядок выполнения работы:
- •Буферной ёмкости буферных систем
- •Порядок выполнения работы:
- •Порядок выполнения работы:
- •Контрольные вопросы Перед выполнением работы:
- •К защите работы:
- •3. Адсорбция
- •Метод полных концентраций
- •Термодинамика адсорбции по Гиббсу
- •Уравнение адсорбции Гиббса
- •Адсорбция из жидких растворов на поверхности твердых адсорбентов
- •Теплоты адсорбции
- •Работа 3.1. Изучение адсорбции паров воды на твердом адсорбенте
- •Порядок выполнения работы:
- •Перед выполнением работы:
- •К защите работы:
- •Работа 3.2. Изучение адсорбции уксусной кислоты из водного раствора на активированном угле
- •Интерферометрический метод анализа концентрации растворов.
- •Технология проведения адсорбции и методика определения равновесных концентраций растворов и расчета адсорбции по результатам эксперимента:
- •Перед выполнением работы:
- •К защите работы:
- •Работа 3.3. Изучение адсорбции поверхностно-активных веществ (пав) на границе воздух-раствор
- •Измерение поверхностного натяжения жидкостей методом Ребиндера.
- •Расчет адсорбции на границе раздела водный раствор – воздух.
- •Порядок выполнения работы:
- •Проверка выполнимости правила Дюкло – Траубе
- •Перед выполнением работы:
- •К защите работы:
- •4. Газовая хроматография
- •Общие сведения о газовом хроматографе
- •Детекторы
- •Детектор по теплопроводности (дтп)
- •Пламенно-ионизационный детектор (пид)
- •Качественный и количественный анализ в газовой хроматографии.
- •Определение мольных теплот растворения газов и паров в жидкостях газохроматографическим методом
- •Порядок работы на хроматографе лхм-80
- •Работа 4.1. Качественный и количественный анализ смеси углеводородов с помощью газовой хроматографии на колонке с апьезоном, нанесенным на хроматон.
- •Определение качественного состава смеси углеводородов по совпадению времен удерживания компонентов контрольной смеси с временами удерживания углеводородов c6 - с9 .
- •Расчет поправочных коэффициентов для углеводородов c6 - с9 и определение количественного состава контрольной смеси углеводородов в мольных процентах.
- •Перед выполнением работы:
- •К защите работы:
- •Работа 4.2. Определение мольных теплот растворения нормальных углеводородов c6- c9 в апьезоне хроматографическим методом
- •Перед выполнением работы:
- •К защите работы:
- •Работа 4.3. Определение индексов ковача веществ и их температурных коэффициентов на апьезоне
- •Перед выполнением работы:
- •К защите работы:
- •Химическая кинетика
- •Кинетические уравнения реакций различных порядков Реакции нулевого порядка
- •Реакции первого порядка
- •Реакции второго порядка
- •Реакции n-го порядка
- •Способы определения порядков реакции.
- •Зависимость скорости реакции от температуры
- •Сложные реакции
- •Работа 5.1. Кинетика омыления этилацетата в присутствии ионов гидроксила.
- •Порядок выполнения работы:
- •Определение æ0.
- •Определение константы скорости реакции при разных температурах.
- •Определение энергии активации и предэкспоненциального множителя.
- •Перед выполнением работы:
- •К защите работы:
- •Работа 5.2. Изучение кинетики гомогенно-каталитического разложения н2о2 .
- •Порядок подготовки установки к работе и работа на ней.
- •Порядок проведения кинетических опытов:
- •Варианты задания и методика расчетов.
- •Изучение зависимости скорости реакции разложения перекиси водорода от концентрации катализатора.
- •Влияние начальной концентрации н2о2 на период полупревращения. Определение порядка реакции.
- •III. Определение константы равновесия и константы скорости реакции разложения перекиси водорода.
- •Перед выполнением работы:
- •К защите работы:
- •Работа 5.3. Изучение кинетики инверсии сахарозы.
- •Методика измерения угла вращения на поляриметре (сахариметре)
- •Методика измерения угла вращения на автоматическом поляриметре
- •Порядок выполнения работы:
- •Перед выполнением работы:
- •К защите работы:
- •Работа 5.4. Изучение кинетики реакции окисления иодид-ионов ионами трёхвалентного железа фотометрическим методом
- •Порядок выполнения работы:
- •Перед выполнением работы:
- •К защите работы:
Концентрационный гальванический элемент
Если привести в соприкосновение два раствора различных концентраций одного и того же электролита, то начнется самопроизвольный процесс их выравнивания. Этот процесс сопровождается уменьшением энергии Гиббса, поэтому он может служить источником ЭДС. Гальванический элемент, составленный из двух полуэлементов, отличающихся друг от друга только концентрацией электролитов, называется концентрационным. Примером такого элемента может служить цепь, составленная из двух серебряных электродов:
Ag | AgNO3 || AgNO3 | Ag .
(С1) (С2)
Потенциалопределяющей является реакция:
Ag+ + e- == Ag.
Пусть в этой цепи концентрация раствора AgNO3 в левом полуэлементе (С1) меньше, чем в правом (С2). Электродный потенциал металлического (серебряного в данном случае) электрода, в соответствии с уравнением Нернста, равен:
![]()
где С(Ag+) - концентрация ионов серебра в растворе. Так как металл обоих электродов один и тот же, стандартные потенциалы Е0(Ag) левого и правого электродов равны. Концентрации ионов серебра в растворах различны в левом и правом полуэлементах, поэтому электродные потенциалы левого и правого электродов также различаются - правый электрод имеет более положительный заряд, чем левый. ЭДС такого концентрационного гальванического элемента равна:
E = Еправ - Елев.
Подставляя в последнее выражение Еправ и Елев, рассчитанные по уравнению Нернста, получаем:
![]() .
2.9
.
2.9
Из (II.9) следует, что величина ЭДС концентрационного гальванического элемента определяется логарифмом отношения концентраций электролитов. Это отношение изменяется не больше чем на два-три порядка, поэтому ЭДС цепей такого типа не превышает 0.2-0.3 В.
При замыкании внешней цепи электроны с левого электрода переходят на правый. Система стремится к восстановлению нарушенного равновесия за счет ускорения реакции окисления на левом электроде и реакции восстановления на правом. В результате концентрация ионов С2 в правом приэлектродном пространстве уменьшается, а в левом (С1) - возрастает. Когда концентрации растворов сравняются, ЭДС цепи станет равной нулю.
Измерение эдс гальванического элемента компенсационным методом
В реальных условиях гальванические элементы работают необратимо, поэтому в работу превращается лишь часть изменения энергии Гиббса реакции, протекающей в элементе. Особенностью электрохимического процесса в гальваническом элементе является возможность его проведения в условиях, близких к обратимости.
Для измерения ЭДС гальванического элемента нельзя использовать обычный низкоомный вольтметр, поскольку его включение во внешнюю цепь нарушает электродные равновесия вследствие протекания значительного тока во внутренней цепи вольтметра. При замыкании внешней цепи гальванического элемента нарушаются термодинамические равновесия на межфазных границах металл - раствор, например, в медно-цинковом элементе ускоряются процессы окисления цинка и восстановления меди. Концентрация ионов цинка у поверхности цинкового электрода увеличивается по сравнению с ее равновесным значением, а концентрация ионов меди у поверхности медного электрода уменьшается. Изменение концентраций ионов уменьшает ЭДС элемента по сравнению с равновесным значением, и тем сильнее, чем больше сила тока в цепи.
Для измерения равновесной величины ЭДС гальванического элемента необходимо обеспечить бесконечно медленное протекание процесса, т.е. протекание во внешней цепи элемента бесконечно малого тока. Поэтому для измерения ЭДС гальванических элементов применяют потенциометры с компенсационной схемой, когда ЭДС элемента компенсирована противоположно направленной ЭДС внешнего источника. Такой прием позволяет измерять ЭДС при практическом отсутствии тока в цепи, т.е. когда элемент не работает и его ЭДС максимальна. Высокочувствительные гальванометры позволяют измерять токи 10-8-10-9 А, а прохождение через электролит такого слабого тока даже в течение многих лет не приводит к выделению на электродах заметных количеств вещества.
Схема измерения ЭДС гальванического элемента компенсационным методом приведена на рис. II.6. В измерительную схему включают внешний источник ЭДС (И ) таким образом, чтобы его ЭДС была направлена навстречу измеряемой ЭДС гальванического элемента (X). С помощью подвижного контакта С можно отбирать произвольную часть ЭДС внешнего источника. Перемещением контакта С вдоль реохорда (проволочного сопротивления) находят такое положение контакта, когда гальванометр (Г ) показывает отсутствие тока в цепи АХГС. Это означает, что часть ЭДС внешнего источника, снимаемая с отрезка АС реохорда, практически полностью компенсирует ЭДС элемента (X) Величина тока в цепи определяется отношением ЕХ / RХ, где RХ - сопротивление участка АС реохорда.
Чтобы отказаться от измерения тока в цепи, перед определением ЕХ вместо элемента Х в измерительную схему включают другой элемент, э.д.с. которого известна. Например, э.д.с. стандартного (нормального) элемента Вестона (N) при 293 К равна 1.0183 В, она хорошо воспроизводится и практически не зависит от температуры.
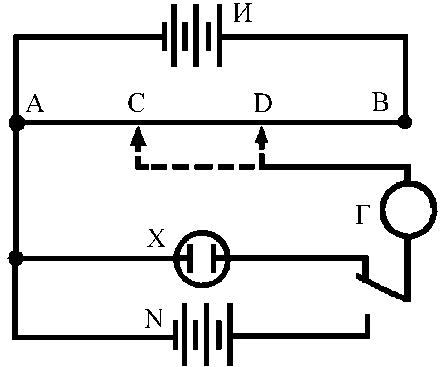
Рис.2.6. Схема измерения ЭДС компенсационным методом
Пусть э.д.с. элемента N компенсируется частью э.д.с. внешнего источника, снимаемой с участка реохорда AD, тогда ток в цепи определяется отношением ЕN / RN, где RN - сопротивление участка АD реохорда. Сопротивление участка реохорда пропорционально его длине, поэтому
![]() откуда
откуда
![]() 2.10
2.10
В настоящее время для измерения ЭДС применяют высокоомные потенциометры различных конструкций, содержащие все элементы компенсационной установки. Измерение ЭДС компенсационным методом при помощи потенциометров дает весьма точные результаты при измерениях электродных потенциалов или опытном определении неизвестной ЭДС. Но этот метод неприменим, если внутреннее сопротивление элемента велико, например, у гальванических цепей со стеклянным электродом. Значения электродвижущей силы гальванического элемента определяют непосредственно на чувствительных вольтметрах постоянного тока с сопротивлением от 108 до 109 Ом и отсчетом до 1 мВ. Через такой вольтметр течет очень маленький ток, поэтому измеренная ЭДС практически не отличается от измеренной на компенсационной установке.
Для измерений ЭДС некомпенсационным методом применяют ламповые потенциометры, ламповые милливольтметры, рН-метры и ионометры различных конструкций. Шкалы приборов отградуированы в милливольтах или единицах рН. Метод используют для потенциометрического титрования и в ионометрии.
При измерениях ЭДС электрохимических цепей некомпенсационным методом надо учитывать, что проходящий через элемент ток более 10-5 А вызывает концентрационную и химическую поляризацию и измеренная ЭДС меньше равновесного значения.
