
- •Выход и характеристика экстрактивных веществ
- •Состав тритерпеноидов коры в. Verrucosa [6], % по массе*
- •* Здесь и в табл. 4 в скобках приведены средние значения.
- •Состав субериновых кислот коры в. Verrucosa [6], % по массе*
- •Состав и выход продуктов щелочной плавки тритерпеноидов [103] .
- •Список литературы
А. Н. Кислицын
Центральный научно-исследовательский
и проектный институт лесохимической промышленности
ЭКСТРАКТИВНЫЕ ВЕЩЕСТВА БЕРЕСТЫ:
ВЫДЕЛЕНИЕ, СОСТАВ, СВОЙСТВА, ПРИМЕНЕНИЕ
ОБЗОР
KISLITSYN А. N. BIRCH BARK EXTRACTIVES: ISOLATION, COMPOSITION. PROPERTIES. APPLICATION. It was shown that the birch bark being a multitonnage industrial waste is a promising chemical raw material comprising 20...40% of extractives and 30...40% of suberin. The methods of extractives isolation are fairly simple and feasible. The main component of the extractives is betulin, a pentacyclic triterpenic diol C30H50O2. Its concentration in the extractives is minimum 60%. Betulinol with the bark material content 95% can be obtained by recrystallization. The suberic acid is a complex mixture of approximately thirty aliphatic C18-C22 mono- and dicarbonic saturated and unsaturated oxy- and epoxy acids. The extractives and suberic acids may find use in production of such products as film formers, plasticizers and surfactants. Be tulinol itself, with its biologically active properties, is of great interest for the synthesis of various derivatives, promising biologically active substances.
Keywords: birch bark, extractives, suberic acids, composition, properties, application.
Ключевые слова: береста, экстрактивные вещества, субериновые кислоты, состав, свойства, применение.
Древесина березы широко используется в фанерном и (в возрастающих объемах) в целлюлозно-бумажном производствах. Березовая кора – многотоннажный отход процесса переработки березы. Содержание коры составляет примерно 12,5% от массы древесины [1, 2], а по неопубликованным данным ВНИИБа – даже 16...17%. На долю наружного слоя коры-бересты приходится 16...20% от ее массы [1, З], Береста, имеющая необычный состав — она содержит до 50% «экстрактивных» веществ, извлекаемых органическими растворителями и щелочами, — представляет большой потенциальный интерес для химической переработки с целью получения новых (например, поверхностно-активных, пленкообразующих, полимерных и т. п.) продуктов и биологически активных веществ. Поэтому, учитывая доступность и потенциальную ценность бересты для химической переработки, целесообразно рассмотреть имеющиеся многочисленные литературные данные о способах выделения из нее химических продуктов, их составе, свойствах и возможных областях применения. Но прежде необходимо уточнить некоторые термины.
В 1788 г. Ловиц из березовой коры путем сублимации выделил соединение, которое Мэзон в 1831 г. назвал бетулином (от лат. betula — береза). В дальнейшем бетулин стали выделять экстракцией органическими растворителями и последующей перекристаллизацией экстрактивных веществ, называя бетулином как экстрактивные вещества, так и индивидуальный тритерпеновый спирт C30H50O2, получаемый при перекристаллизации из экстрактивных веществ. Между тем последние – сложная смесь с массовой долей бетулина 60...85%, и называть их бетулином неправильно. Это экстрактивные вещества. Что касается тритерпенового спирта C30H50O2, то в литературе употребляются названия «бетулин», «бетулинол», в Chemical Abstracts он фигурирует как луп-20(29)-ен-3р,28-диол. Мы используем название «бетулинол», показывающее, что это спирт.
Суберин (от лат. suber – пробковое дерево) – такое название дал Бусиньоль в 1836 г. веществам, извлеченным из коры пробкового дерева Quercus suber спиртовой щелочью. Этим словом называют до сих пор как вещество, находящееся в пробке или бересте, так и получаемые из них кислоты. С «химической» точки зрения это совершенно разные вещества: суберин – полиэфир (полиэстолид), кислоты – смесь мономерных соединении, из которых построен суберин. Поэтому кислоты, получаемые при омылении суберина, следует называть субериновыми кислотами, а не суберином.
Основными химическими компонентами бересты являются собственно экстрактивные вещества (вещества, извлекаемые органическими растворителями), суберин (полиэстолид нерегулярного строения), лигнин и полисахариды. Береста берез Betula verrucosa и B. pubescens – основных видов, произрастающих на евразийской территории, – содержит 20...40% экстрактивных веществ и 30...40% субериновых кислот – продуктов омыления суберина спиртовой щелочью [4...9]. Некоторые другие виды берез характеризуются следующим содержанием экстрактивных веществ и субериновых кислот в бересте (%): В. alba 14,1 и 19,7; В. costata 21,0 и 8,6; В. davurica 20,0 и 25,5 и В. ermani 19,0 и 38,8 соответственно [8].
Содержание экстрактивных веществ, и в том числе бетулинола, зависит не только от вида березы, но и от места произрастания и возраста дерева, сезонности [7, 10...14].
Выделение экстрактивных веществ и субериновых кислот. Химические свойства экстрактивных веществ и суберина предопределяют возможные способы переработки бересты: экстрактивные вещества выделяют экстракцией органическими растворителями; суберин, нерастворимый в растворителях, омыляют щелочью и извлекают в виде солей субериновых кислот.
Выделение экстрактивных веществ и субериновых кислот возможно двумя способами: путем последовательного раздельного их выделения (последовательный способ) и путем одновременного извлечения с последующим разделением (совмещенный способ).
По первому способу вначале из бересты извлекают экстрактивные вещества, а затем субсриновые кислоты. В качестве экстрагента для извлечения экстрактивных веществ опробованы алифатические углеводороды и их хлорпроизводные, бензол, спирты C1–C4, ацетон. Хотя растворимость экстрактивных веществ в этих растворителях невелика (не более 50 г/л при температуре кипения), все растворители, за исключением петролейного эфира, пригодны для этой цели. В лабораторной практике чаще всего используют этанол или бензол, экстрагирующая способность которых одинакова, или их смесь.
Пасих [15] исследовал процесс извлечения экстрактивных веществ в аппарате Сокслета и нашел, что наибольший выход достигается при использовании трихлорэтилена (44%) по сравнению с 28, 25 и 22% при использовании бензола, диэтилового эфира и хлороформа. Он же попытался интенсифицировать процесс экстракции с помощью ультразвука, но не получил положительных результатов.
Яэскелайнен [16] изучил кинетику и глубину извлечения экстрактивных веществ рядом растворителей и установил, что петролейный эфир после 30-ч экстракции извлекает всего 6,0%, четыреххлористый углерод, перхлорэтилен и ацетон 33,4...36,4%, а этанол, трихлорэтилен и метиленхлорид 40,3...42,3% экстрактивных веществ от массы бересты. Анализ этих данных показал, что имеется тенденция увеличения скорости и глубины экстракции с ростом «полярности» (Ет) растворителя.
Основательно изучен процесс извлечения бетулинола из бересты Эккерманом и Экманом [17]. Изучение скорости экстракции бетулинола в процессе нагревания 100 г бересты в 1 л растворителя показало следующее. При использовании бересты мелкого помола (размер частиц 0,15...1,5 мм) происходит быстрое растворение бетулинола в большинстве использованных растворителей (углеводородный растворитель LIAV-200, дихлорметан, метанол, изопропанол-азеотроп, этанол-азеотроп, 2-бутанол-азеотроп, ацетон), в течение 5 мин в раствор переходит свыше 90% содержащегося в бересте бетулинола. Исключение составляет углеводородный растворитель LIAV-110. Из-за плохой растворимости бетулинола в последнем экстракт становится насыщенным уже при растворении 30% бетулинола бересты. При обработке более крупной бересты (размер частиц 0,8...4,0 мм) наблюдается дифференциация в скоростях и глубине экстракции бетулинола различными растворителями. Наивысшая скорость экстракции – при использовании LIAV-200 благодаря высокой температуре процесса (не ниже 150°С). 90%-ная степень извлечения достигается через 30 мин. При использовании других растворителей скорость и глубина экстракции увеличиваются в ряду дихлорметан<изопропанол=изобутанол=аце-тон<метанол<этанол, за 60 мин извлекается от 75 до 93% бетулинола от содержащегося в бересте.
Микроскопическое изучение сечений частиц бересты, подвергнутой экстракции, показало, что проникновение растворителя и диффузия экстрактивных веществ из бересты происходят, в основном, между слоями пластинок. Поэтому для ускорения процесса экстракции очень важно не только измельчить бересту до частиц определенного размера (по площади), но и разодрать их на тонкие пластинки.
Авторы [17] изучили устойчивость бетулинола в кипящем растворе LIAV-200 при барботаже воздуха. Установлено, что бетулинол неустойчив, сразу начинается его окисление, через 10 ч окисляется 28%, через 20 – 75% бетулинола. В присутствии бересты благодаря наличию в ней фенольных компонентов, действующих как антиокснданты, окисление начинается значительно позже – более чем через 100 ч.
В работе [17] изучен также процесс выделения тритерпеноидов из экстрактов, полученных экстракцией в аппарате Сокслета. Чтобы обеспечить растворимость извлекаемых тритерпсноидов, в колбу заливали 1,5 л растворителя на 100 г бересты. Экстракт упаривали до объема 440 мл, охлаждали до 15°С, выдерживали 24 ч и отделяли кристаллический осадок от маточника фильтрацией. Выход и характеристика продуктов, полученных при этом, приведены в табл. 1.
Таблица 1.
Выход и характеристика экстрактивных веществ
Показатель |
Углеводородный растворитель, Ткип 150…185°C |
Дихлорметн |
Метанол |
Изопропанол-вода (азеотроп) |
Этанол-вода (азеотроп) |
Ацетон |
2-Бутанол-вода (азеотроп) |
Выход экстрактивных веществ, % от массы бересты |
31 |
33 |
34 |
35 |
35 |
35 |
35 |
Массовая доля бетулинола в экстрактивных веществах, % |
71 |
67 |
64 |
64 |
63 |
63 |
62 |
Массовая доля кристаллического осадка из упаренного экстракта, % от массы экстрактивных веществ |
91 |
73 |
71 |
70 |
68 |
64 |
63 |
Массовая доля бетулинола в кристаллическом осадке, % |
76 |
71 |
72 |
78 |
70 |
74 |
82 |
Выход бетулинола, перешедшего в кристаллический осадок, % от содержания бетулинола в экстрактивных веществах |
97 |
77 |
80 |
85 |
75 |
75 |
83 |
Из таблицы следует, что большинство растворителей извлекает примерно одинаковое количество экстрактивных веществ (33...35%) с примерно одинаковой массовой долей бетулинола в них – 62...67%. Экстракт, полученный с растворителем LIAV-200, более светлый, что объясняется меньшей экстракцией полярных компонентов этим неполярным растворителем. Поэтому выход экстрактивных веществ с ним самый низкий (31%), а концентрация бетулинола в экстрактивных веществах самая высокая (71%). В осадок переходит 97% бетулинола от содержания его в экстрактивных веществах, тогда как при использовании других растворителей в осадок переходит значительно меньшее количество – 75...85%. Среди последних заслуживают внимания два растворителя – 2-бутанол (азеотроп) и изопропанол (азеотроп); в кристаллическом осадке из них самая высокая массовая доля бетулинола (82 и 78%), а в осадок переходит 83 и 85% бетулинола соответственно.
тритерпеноидов в кристаллическом осадке и в фильтрате (маточнике) представлено в табл. 2. Из таблицы видно, что, если не брать во внимание растворитель LIAV-200, наибольшая концентрация бетулинола наблюдается в осадке из азеотропа изопропанол-вода. По расчетам в фильтрате концентрация бетулинола в 2,5 раза ниже, а всех остальных в 3,1 раза выше, чем в кристаллическом осадке.
Таблица 2.
МАССОВАЯ ДОЛЯ ТРИТЕРПЕНОИДОВ В БЕРЕСТЕ И СООТНОШЕНИЕ ИХ В КРИСТАЛЛИЗАТЕ И ФИЛЬТРАТЕ ДЛЯ РАЗЛИЧНЫХ РАСТВОРИТЕЛЕЙ [17]
Тритерпеноид |
Концентрация в сухой бересте, г/кг |
Отношение массовых долей тритерпеноидов в кристаллизате и фильтрате для растворителей |
||||||
Углеводородный растворитель, Ткип 150...185°С |
Изопропанол-вода (азеотроп) |
2-Бута-нол-вода (азеотроп) |
Метанол |
Ди-хлор метан |
Аце-тон |
Этанол-вода (азеотроп) |
||
Бетулинол |
220,0 |
74,3 |
8.2 |
6.5 |
5,5 |
4,3 |
3,8 |
3,6 |
Лупеол |
20,0 |
1.4 |
0,7 |
0,9 |
1,9 |
1,0 |
1,4 |
0.9 |
Прочие |
25,8 |
3,5 |
1.0 |
0,9 |
1,1 |
1,1 |
0,9 |
0,8 |
Авторы [17] предлагают два способа получения бетулинола в зависимости от требуемой чистоты его. В качестве экстрагента в обоих случаях используется углеводородный растворитель LIAV-200. В первом варианте вышеописанным способом получают кристаллический осадок, в который из экстракта переходит 97% бетулинола с содержанием основного вещества 76%. По второму варианту этот кристаллический осадок подвергается повторной кристаллизации из азеотропа 2-бутанол-вода. В результате массовая доля основного компонента повышается до 95%, но уменьшается доля перешедшего в кристаллический продукт бетулинола до 80% от содержания его в экстракте. Таковы данные об изучении первой стадии последовательного способа переработки бересты.
Вторая стадия – омыление суберина с получением субериновых кислот – специально никем не изучалась. Обычно омыление суберина проводят большим избытком спиртового или водно-спиртового раствора гидроксида калия. Дальнейшая обработка экстракта сводится к отгонке спирта. разложению солей разбавленной сильной кислотой и отделению субериновых кислот фильтрацией или экстракцией органическими растворителями. При омылении суберина водной щелочью выход субериновых кислот не меняется, но скорость омыления ниже, чем при использовании спиртовой щелочи. Состав кислот при омылении водной щелочью иной вследствие перехода главного компонента субериновых кислот – 9,10-эпокси-18-гидроксиоктадекановой кислоты – в 9,10,18-тригидроксиоктадекановую [18].
Следует упомянуть, что некоторые исследователи использовали иную последовательность извлечения экстрактивных веществ и субериновых кислот: вначале извлекали щелочерастворимые компоненты обработкой аммиачной водой (Schulze. Pierch, Chem. Ber., 1922, Bd. 55, S. 2332-2347) или раствором соды (Dieschendorfer, Grillmayer, Monatshefte Chem., 1926, H. 47, S. 419), а затем – экстрактивные вещества. Показано [19], что бетулин (экстрактивные вещества), полученный таким образом, содержит меньше примесей и легче подвергается очистке.
Бетулинол из бересты можно выделить не только экстракцией, но и сублимацией. Так его впервые и получил Ловиц. Метод исследовался и позже (Vesterberg, Chem. Ber., 1932, Bd. 65, S. 1305). Однако бетулинол в сублимате сильно загрязнен, и выход его невелик. Лучшие результаты получены при вакуумной (давление 1,3...1,8 кПа) сублимации бетулинола из бересты, предварительно обработанной кипящими водными растворами щелочи. Выход сублимата 23%. Содержание бетулинола высокое, так как после 1...2 перекристаллизаций из спирта получено вещество с температурой плавления 258...259°С [19].
Возможен и принципиально иной путь выделения субериновых кислот – алкоголизом полиэфира суберина, в частности обработкой метанолом в присутствии серной кислоты [18, 20]. Правда, в этом случае получаются не субериновые кислоты, а метиловые эфиры их. Кроме того, эпоксикислоты превращаются в 9-(или 10)-метокси-10-(или 9)-гидроксипроизводные. Степень превращения суберина около 90%.
При щелочной плавке бересты, освобожденной от экстрактивных веществ, с гидроксидом калия при 330°С суберин превращается в смесь насыщенных моно- и дикарбоновых кислот. Выход таких кислот составил 450...500 г/кг сухой проэкстрагированной бересты [20].
Совмещенный способ извлечения экстрактивных веществ и субериновых кислот из бересты предложен Т. И. Федорищевым [21]. Сущность его состоит в следующем. Измельченная береста истирается совместно с водной щелочью. К полученной корьещелочной массе добавляется изопропанол (азеотроп), и смесь при нагревании перемешивается. Суспензия твердого лигноуглеводного остатка в спиртоводном растворе разделяется фильтрованием. Из фильтрата отгоняется спирт, к остатку добавляется вода. Из образующейся водно-бетулиновой эмульсии отделяются фильтрацией экстрактивные вещества (бетулин), а из фильтрата выделяются субериновые кислоты. Изучено [22] влияние расхода щелочи, модуля спирт–водная щелочь, примеси луба на выход и качество продуктов. Найдены оптимальные параметры процесса. Выход экстрактивных веществ и субериновых кислот равен 23,5...25,5 и 30,0...31,5% при содержании их в бересте 23,6 и 29,5% соответственно. Состав продуктов не изучался.
Литературные данные показывают, таким образом, что химическая переработка бересты с получением экстрактивных веществ (или бетулинола) и субериновых кислот вполне технически осуществима. Информации о реализации химической переработки бересты в промышленности не имеется.
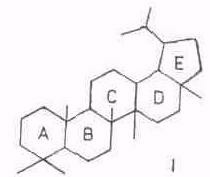
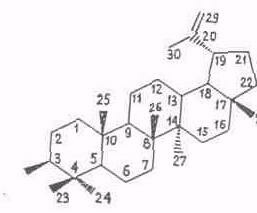
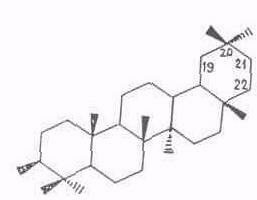
Химический состав тритерпеноидов. В экстрактивных веществах внешней коры берез большинства видов преобладают пентациклические тритерпеноиды лупанового ряда (I), реже олеананового (II). Найдены также представители ряда урсана (III).
Все они различаются лишь скелетом кольца Е. Основным представителем тритерпеноидов ряда лупана является бетулинол, обусловливающий белый цвет коры. Массовая доля бетулинола в бересте колеблется в очень широких пределах (10...35%) в зависимости от вида березы, места и условий произрастания, возраста дерева и др. факторов [16, 23, 24]. Минимальное содержание бетулинола отмечено для березы с черной корой – В. davurica, где это соединение является минорным, а преобладают тритерпеноиды ряда олеанана – олеаноловая кислота и ее производные [23,. 25], да и содержание экстрактивных веществ в коре этой березы низкое. Постоянный спутник бетулинола в тритерпеноидах из В. verrucosa и В. pubescens – лупеол (~10% от бетулинола). В работе [26] отмечено аномально высокое содержание лупеола примерно равное массе бетулинола. Биосинтез бетулинола протекает через гераниол, сквален и лупеол [24].


Для качественного определения принадлежности вещества к группе тритерпеноидов предложено использовать УФ-спектроскопию в концентрированной серной кислоте. Различные тритерпеноиды ряда I, II, III имеют общий максимум поглощения при 310 нм, который характеризуется большой экстинкцией и не меняется при введении в молекулу различных заместителей. Стероиды указанного максимума поглощения не дают [27].
Для разделения тритерпеноидов при исследовании химического состава применяется препаративная тонкослойная и колоночная хроматография [13, 14, 28...36] (как правило, на силикагеле), для анализа – газожидкостная хроматография с использованием набивных и капиллярных колонок (как правило, с SE-30 в качестве жидкой фазы) [6, 13, 14, 30, 37...44]. Разработана методика количественного определения бетулинола [45]. Используется для исследования состава тритерпеноидов также высокоэффективная жидкостная хроматография [46]. Для детектирования вместо УФ-спектроскопии и рефрактометрии недавно предложено использовать более чувствительный (в 5 раз) метод комбинационного рассеяния света [47].
Финскими [6, 36] и российскими (Н. И. Уварова с сотр., Тихоокеанскнй ин-т биоорганической химии ДВЦ РАН) [11, 13, 14, 23, 25, 48, 49] исследователями в экстрактах из внешней коры берез, произрастающю на евразийской территории — В. pubescens, В. verrucosa Ehrh. (В. pendula Roth.), В. costata, В. davurica. В. ermanii, В. mandshurica и В. maximowicziana – идентифицированы следующие тритерпеноиды:
|
R1 |
|
R2 |
IV |
–OH |
XIV |
–CH3 |
V |
–OH |
XV |
–CH2OH |
VI |
–OH |
XVI |
–CHO |
VII |
–OH |
XVII |
–COOH |
VIII |
–OH |
XVIII |
–COOCH3 |
IX |
=O |
— |
–CH3 |
Х |
=O |
— |
–CHO |
XI |
=O |
— |
–COOH |
|
–OCOCH3 |
XIX |
–COOH |
XII |
–OCOCH=CH–C6H3(OH)2 |
— |
–CH2OH |
XIII |
–OCOCH=CH–C6H3(OH)2 |
XX |
–COOH |
лупеол (IV), бетулинол (V), бетулиновый альдегид (VI), бетулиновая кислота (VII), метилбетулинат (VIII), лупенон (IX), бетулоновый альдегид (X), бетулоновая кислота (XI), кофеаты бетулинола (XII) и бетулнновой кислоты (XIII), р-амирнн (XIV), эритродиол (XV), олеаноловый альдегид (XVI), олеаноловая кислота (XVII), метилолеанолат (XVIII), ацетат (XIX) и кофсат (XX) олеаноловой кислоты, лупан-3β,20-диол (моногинол) (XXI, R1=OH, R2=CH3), лупан-3β,20,28-триол (XXI, R1=OH, R2=CH2OH), кофеат лупан-Зβ,20,28 (XXI, R1= C6H3(OH)2–CH=CH–COO, R2=CH2OH), урсоловая кислота (XXII), аллобетулин (XXIII) и Зβ-ацетил-11α,12α-эпоксиолеан-13,28-олид (XXIV). 6α-Ацетоксиурсоловая кислота выделена из коры березы В. utillis [50].
Наиболее полный количественный состав тритерпеноидов коры березы B. verrucosa приведен в работе Экмана [6] (табл. 3). Массовая доля тритерпеноидов в свежей бересте составляет 21,0... 40,0% (в среднем 31,5%), в промышленных образцах с ЦБП – в среднем 26,9%.
Таблица 3
