
- •Квантовая физика
- •Квантовые свойства электромагнитного излучения (эми) Тепловое излучение (ти)
- •Фотоэффект
- •Тормозное рентгеновское излучение
- •Корпускулярно-волновой дуализм
- •Эффект Комптона
- •Атом Резерфорда-Бора. Формула Резерфорда
- •Дифференциальное сечение
- •Спектральные закономерности
- •Постулаты Бора
- •Опыт Франка и Герца (1913)
- •Модель атома Бора
- •Спектральные серии водородоподобных систем
- •Магнитный момент атома водорода
- •О теории Бора
- •Волновые свойства частиц
- •Опыты Дэвисона и Джермера (1927)
- •Опыты Томсона и Тартаковского
- •Другие опыты
- •Парадоксальное поведение микрочастиц
- •Критерий классического описания
- •Принцип неопределенности
- •Опыт со щелью
- •Размер атома водорода
- •Состояние частицы
- •Принцип суперпозиции
- •Уравнение Шредингера
- •Стационарные состояния
- •Квантование
- •Частица в прямоугольной яме
- •Квантовый гармонический осциллятор
- •Колебания в молекуле
- •П отенциальные барьеры
- •Туннельный эффект
- •Средние значения физических величин
- •Операторы
- •Основные постулаты квантовой теории
- •Квантование момента импульса
- •П роекция момента импульса
- •Ротатор
- •Квантование атомов
- •Плотности распределения вероятности
- •Правило отбора
- •Тонкая структура спектральных линий
- •Спин электрона
- •Полный момент импульса электрона
- •Механический момент многоэлектронного атома
- •Правила отбора
- •Принцип Паули
- •О периодической системе Менделеева
- •Характеристические рентгеновские спектры
- •Магнитные свойства атома
- •Опыт Штерна и Герлаха
- •Спиновой магнитный момент
- •Полный магнитный момент атома
- •Эффект Зеемана(1896)
- •П ростой эффект Зеемана
- •Сложный эффект Зеемана
- •Эффект Пашена-Бака
- •Электронный парамагнитный резонанс
- •Атомное ядро Некоторые сведения о ядре
- •Размеры ядра
- •Спин ядра(I)
- •Масса и энергия связи ядра
- •Удельная энергия связи
- •Механизм взаимодействия нуклонов
- •Модели ядра
- •Радиоактивность
- •Закон радиоактивного распада
- •Типы радиоактивности
- •Ядерные реакции
- •Выход ядерной реакции
- •Энергия реакции
- •Квантовые статистики (кс)
- •Фазовые ячейки
- •Квантовые распределения
- •Число фазовых ячеек
- •Распределение частиц
- •Свободные электроны в металле
- •Энергия Ферми
- •Зонная теория твердого тела Предпосылки возникновения зонной теории
- •Образование электронных зон
- •Характеристика энергетических зон
- •Металлы, диэлектрики и полупроводники
- •Собственная проводимость полупроводников (п/п)
- •Примесная проводимость полупроводников
- •Электропроводность металлов
- •Энергия молекулы
- •Элементарные частицы
- •Фундаментальные взаимодействия
- •Хронология
- •Систематика
- •Античастицы
- •Законы сохранения
- •Заряды элементарных частиц
- •Странность
- •Шарм (очарование) и красота (прелесть)
- •Четность
- •Изотопический спин
- •Кварковая модель адронов
- •Современная картина мира
П ростой эффект Зеемана
Простой эффект Зеемана- расщепление спек-
тральной линии на три компоненты.
Простой эффект:
Присущ спектральным линиям, не имеющим тонкой структуры(такие линии возникают при переходах между синглентными уровнями
(S=0,
J=L,
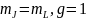 ).
).
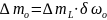 ,
где
,
где
 возникает три компоненты, для которых
возникает три компоненты, для которых

Сложный эффект Зеемана
Наряду с простым, наблюдается сложный эффект Зеемана- расщепление спектральной линии источника в магнитном поле на число компонент более трех.
Сложный эффект Зеемана:
связан с зависимостью расщепления уровней от множителя Ланде g (т.е. с наличием спина y ) ;
наблюдается в слабом магнитном поле.
Эффект Пашена-Бака
В сильном магнитном
поле связь между моментами
 разрывается и по отношению к полю они
ведут себя независимо друг от друга. В
этом случае:
разрывается и по отношению к полю они
ведут себя независимо друг от друга. В
этом случае:
дополнительная энергия
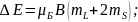
действуют правила отбора:
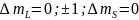 ;
;в результате наблюдается триплет, аналогично простому эффекту Зеемана.
Таким образом, для атомов с тонкой структурой по мере увеличения В поля наблюдается:
тонкое расщепление (В
 );
);сложный эффект Зеемана (В мало);
эффект Пашена-Бака (В велико).
Наиболее сложная картина – 2)
Электронный парамагнитный резонанс
Электронный парамагнитный резонанс (ЭПР) – явление перехода атома в пределах
одного уровня от одного подуровня к другому под одновременным воздейст-
вием внешнего магнитного поля В и электромагнитного излучения с часто-
той
 (ЭПР открыл Е.К. Завойский в 1944 г.) .
(ЭПР открыл Е.К. Завойский в 1944 г.) .
Теория ЭПР:
У атома парамагнетика каждый уровень с квантовым числом Jрасщепляется в магнитном поле на 2J+1 подуровней (по числу возможных );
интервал между подуровнями

если на атом в таком состоянии направить ЭМВ с частотой
 ,
то под действием ее магнитной составляющей
(согласно правилам отбора) происходит
ЭПР.
,
то под действием ее магнитной составляющей
(согласно правилам отбора) происходит
ЭПР.
С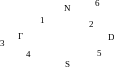 хема
установки (радиоспектроскопа):
хема
установки (радиоспектроскопа):
1 – образец парамагнетика , 2 – объемный резонатор , 3 – СВЧ-генератор, 4 – волновод,
5 – детектор , 6 – полюса электромагнита.
В
радиоспектроскопе применяют генератор
фиксированной частоты
и источник плавно регулируемого
магнитного поля В. При некотором значении
В детектор регистрирует резкое увеличение
поглощения образцом энергии СВЧ –
колебаний
(
λ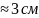 ).
).
Эксперименты
с ЭПР дают возможность определить
величину
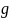 по
известным В и
по
известным В и
 По известному
можно вычислить магнитный момент атома
в состоянии с квантовым числом J.
По известному
можно вычислить магнитный момент атома
в состоянии с квантовым числом J.
Атомное ядро Некоторые сведения о ядре
Состав: ядро состоит из нуклонов (протоны и нейтроны).
Протон: несет положительный заряд е; обладает массой
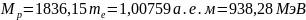 ;
спин S =
;
спин S = ;
собственный магнитный момент
;
собственный магнитный момент
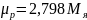 ,
где
,
где
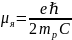 =5,05
=5,05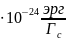 – ядерный
магнетон
(единица измерения магнитных моментов
нуклонов).
– ядерный
магнетон
(единица измерения магнитных моментов
нуклонов).
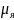 =
=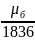 ;
собственный магнитный момент протона
в 660 раз меньше магнитного момента
электрона.
;
собственный магнитный момент протона
в 660 раз меньше магнитного момента
электрона.
Нейтрон: заряд q=0; масса
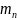 =1838,68
=1838,68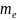 =1,00898a.e.м=939,55
МэВ.
=1,00898a.e.м=939,55
МэВ.
Магнитный
момент
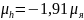 ,
т.е.
,
т.е.
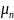 ↑↓ «направлению» спина.
↑↓ «направлению» спина.
В свободном состоянии нейтрон нестабилен и распадается на протон, электрон и нейтрино:N →p+e+v
Основные характеристики ядра: Z и A.
Зарядовое число (или атомный номер) (Z)– количество протонов в ядре.
Заряд ядра q=Ze
Массовое
число (A)
– количество нуклонов в ядре. Символическое
обозначение химического элемента
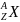 .
Число нейтронов в ядре N
=
A-Z
.
Число нейтронов в ядре N
=
A-Z
Конкретные ядра (как и атомы), отличающиеся по составу, часто называют нуклидами.
Изотопы – ядра с одинаковым Z и разным А.
Изобары – ядра с одинаковым А и разным Z.
Атомы изотопов обладают очень близкими физико-химическими свойствами, однако наблюдаются и различия (особенно у изотопов:
 ).
).Атомы:
 – обычный водород,
– обычный водород, .
.Ядра:
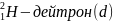 ;
:
;
:

Число изотопов у разных атомов различно.
