
- •Отчет по лабораторной работе №1
- •По дисциплине:
- •Санкт-Петербург
- •Отчет по лабораторной работе №2
- •По дисциплине:
- •Санкт-Петербург
- •Лабораторная работа 2
- •По дисциплине:
- •Санкт-Петербург
- •Лабораторная работа 3
- •По дисциплине:
- •Санкт-Петербург
- •Отчет по лабораторной работе №3
- •По дисциплине:
- •Санкт-Петербург

vk.com/club152685050 | vk.com/id446425943
Федеральное агентство по образованию Санкт-Петербургский государственный горный институт им. Г.В. Плеханова
(технический университет)
Кафедра общей и физической химии
Отчет по лабораторной работе №1
По дисциплине: |
Химия нефти и газа |
|
(наименование учебной дисциплины согласно учебному плану)
Тема: определение кислотности нефтепродуктов методом потенциометрического титрирования
Санкт-Петербург
2004

vk.com/club152685050 | vk.com/id446425943
Цель работы:
Определить уровень кислотности в предложенной пробе бензина.
Сущность работы:
Определение условия кислотности основано на реакции нейтрализации: Н+ + ОН- 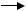
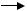 Н2О. Вследствие протекания реакции потенциал стеклянного электрода постепенно понижается. Как только все ионы Н+ окажутся связанными, наступает резкий скачок потенциала. При дальнейшем добавлении щелочи потенциал электрода меняется незначительно. Электродом сравнения служит хлорсеребряный электрод.
Н2О. Вследствие протекания реакции потенциал стеклянного электрода постепенно понижается. Как только все ионы Н+ окажутся связанными, наступает резкий скачок потенциала. При дальнейшем добавлении щелочи потенциал электрода меняется незначительно. Электродом сравнения служит хлорсеребряный электрод.
Ход работы:
В стакан налили 50 мл бензина. Установили стакан на магнитную мешалку и включили ее. Подключили рН-метр (электроприбор измеряющий ЭДС, уровень рН). При этом электроды
опустили в бензин. При необходимости, если бензина недостаточно, добавили растворитель ( СНСl3 C2 H5OH ). Замерив значение ЭДС бензина, мы добавляем в него по
0,5 мл раствора KОН, с концентрацией равной CK |
0,05 |
экв |
, и заносим показания прибора |
||||||
л |
|
||||||||
|
|
|
|
|
|
|
|
||
(Е) в таблицу №1. Производим расчет |
E |
, где |
E En 1 |
En |
, а |
V - шаг титрования (в |
|||
V |
|||||||||
|
|
|
|
|
|
|
|
||
нашем случае |
V 0,5мл ). Полученные результаты расчетов также заносим в таблицу №1. |
Щелочь добавляем до тех пор, пока ЭДС не будет изменяться на незначительную величину.

vk.com/club152685050 | vk.com/id446425943
Таблица №1.
№ |
VNaOH , мл |
Е, мВ |
E/ V |
1 |
0 |
-508 |
128 |
2 |
1 |
-380 |
806 |
3 |
1,5 |
23 |
164 |
4 |
2 |
105 |
-104 |
5 |
2,5 |
53 |
-122 |
6 |
3 |
-8 |
-64 |
7 |
3,5 |
-40 |
-46 |
8 |
4 |
-63 |
-34 |
9 |
4,5 |
-80 |
-24 |
10 |
5 |
-92 |
-28 |
11 |
5,5 |
-106 |
-50 |
12 |
6 |
-131 |
-110 |
13 |
6,5 |
-186 |
-248 |
14 |
7 |
-310 |
-98 |
15 |
7,5 |
-359 |
-22 |
16 |
8 |
-370 |
-14 |
17 |
8,5 |
-377 |
-8 |
18 |
9 |
-381 |
-8 |
19 |
9,5 |
-385 |
-6 |
20 |
10 |
-388 |
-6 |
21 |
10,5 |
-391 |
-4 |
22 |
11 |
-393 |
-2 |
23 |
11,5 |
-394 |
-2 |
24 |
12 |
-395 |
-2 |
25 |
12,5 |
-396 |
-2 |
26 |
13 |
-397 |
|
Пример расчета:
E
Рассчитаем V для n=5:
E En 1 En |
E E6 E5 8 53 61мВ |
E |
|
61 |
122В / л |
|
V |
0,5 |
|||
|
|
На основании полученных результатов строим график зависимости Е от VKОН и
дифференциальную кривую (зависимость |
E |
от VKОН). |
|
V |
|||
|
|

vk.com/club152685050 | vk.com/id446425943
Графики:
|
|
|
Потенциометрическая кривая |
|
|
|
|
||||||
200 |
Е,мВ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
100 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Vкон,мл |
|
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
-100 |
|
|
|
|
|
|
|
|
|
|
|
|
|
-200 |
|
|
|
|
|
|
|
|
|
|
|
|
|
-300 |
|
|
|
|
|
|
|
|
|
|
|
|
|
-400 |
|
|
|
|
|
|
|
|
|
|
|
|
|
-500 |
|
|
|
|
|
|
|
|
|
|
|
|
|
-600 |
|
|
|
|
|
|
|
|
|
|
|
|
|
EV
1000
800
600
400
200
0
-200
-400
Дифференциальная кривая
,В/л
Vкон,мл
0 |
2 |
4 |
6 |
8 |
10 |
12 |
14 |
Определение кислотности:
CK VТ СТ , где СТ – концентрация KOH (0,05 экв/л)
Vа
Va – объем пробы взятой для анализа (50мл)
VТ – объем KOH (мл)
vk.com/club152685050 | vk.com/id446425943
Кислотность рассчитываем в точке, которая будет являться максимумом на графике дифференциальной кривой (эквивалентная точка):
C |
|
|
VТ СТ |
|
1 0,05 |
0,001 |
экв |
K |
|
|
|
||||
|
|
Vа |
50 |
|
л |
||
|
|
|
|
||||
Вывод: в проделанной работе, методом потенциометрического титрирования нам удалось определить концентрацию кислоты находящейся в бензине, она равна 0,001 экв/л.
