Министерство образования и науки Российской Федерации
Государственное бюджетное образовательное учреждение высшего
профессионального образования
«Ярославский государственный технический университет»
Кафедра «Химическая технология органических веществ»
Отчет защищен
с оценкой__________________
Старший преподаватель
____________ Л.М.Соболева
«___» ______________ 2012
Дегидрирование этилбензола
Отчет о лабораторной работе
по дисциплинам: «Химическая технология органических веществ»,
«Экспериментальные методы органического синтеза»
ЯГТУ 240100.62 – 006 ЛР
Отчет выполнил
студент гр. ДСХ-30
__________ Д.Д.Гоголева
«___»____________ 2011
2012
Р еферат
15 с., 2 рис., 3 табл., 2 источник
ДЕГИДРИРОВАНИЕ , ЭТИЛБЕНЗОЛ, СТИРОЛ, ТОЛУОЛ, БЕНЗОЛ, КАТАЛИЗАТ, ХРОМОТОГРАФИЯ, МАТЕРИАЛЬНЫЙ БАЛАНС, СТЕПЕНЬ ПРЕВРАЩЕНИЯ, ВЫХОД ОТ ТЕОРИТИЧЕСКИ ВОЗМОЖНОГО
Объектом исследования является этилбензол.
Цель работы – проведение дегидрирования этилбензола в присутствии катализатора КМС на лабораторной контактной установке с целью изучения влияния условной реакции ( температура, объемной скорости подачи, разбавление водяным паром) на материальный баланс и безразмерные характеристики процесса.
В работе использовались физико-химические методы анализа.
В
процессе работы был изучен процесс
дегидрирования этилбензола в присутствии
катализатора КМС при температуре реакции
580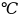 и
объемной скорости 1,28
и
объемной скорости 1,28
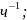 проведен хромотографический анализ
катализата, составлен материальный
баланс процесса; рассчитаны основные
безразмерные характеристики процесса.
проведен хромотографический анализ
катализата, составлен материальный
баланс процесса; рассчитаны основные
безразмерные характеристики процесса.
Содержание
Введение 1 Теоретическое обоснование процесса 2 Экспериментальная часть 3 Обобщение и оценка результатов Заключение Список используемых источников
|
Введение
Производство
основных мономеров для синтетического
каучука и других полимеров – одно из
самых крупномасштабных в промышленности
основного органического и нефтехимического
синтеза. Среди различных способов
получении мономеров процесса
каталитического дегидрирования
углеводородов занимают ведущее положение
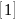
Для дегидрирования алкиларенов используются железокислные катализаторы. Железосодержащие катализаторы способны работать без регенерации непрерывно или длительными циклами дегидрирования. В своем составе катализаторы содержат железо в виде окислов или шпинелей, окислы хрома, цинка, кремния, калия.
1 Теоретическое обоснование процесса
Каталитическое дегидрирование олефинов и алкиларенов в промышленности осуществляют в присутствии водяного пара или инертного газа. Это способствует повышению равновесной степени превращения.
Уравнение реакции дегидрирования в общем виде:
А
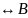 +
+

где А – олефин или алкиларен ;
В – диен или виниларен.
Предположим,
что в исходной смеси содержится 1 моль
А и n(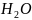 )
моль водяного пар; равновесия степень
превращения
)
моль водяного пар; равновесия степень
превращения
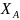 .
Тогда, при устовившемся равновесии,
количество молей получившегося продукта
А, будет равно количество молей
и количеству молей прореагировавшего
А, т.е.
.
Тогда, при устовившемся равновесии,
количество молей получившегося продукта
А, будет равно количество молей
и количеству молей прореагировавшего
А, т.е.
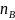 =
=
 =
=
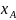 ;
остается непрореагировавшим 1-
молей А, Количество молей воды остается
постоянным
;
остается непрореагировавшим 1-
молей А, Количество молей воды остается
постоянным
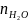 .
Суммарное количество молей в равновесной
смеси:
.
Суммарное количество молей в равновесной
смеси:
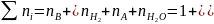 +
+
Составим уравнение константы равновесия для реакции дегидрирования:
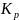 =
=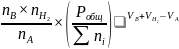
Где
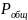 - общее давление в системе;
- общее давление в системе;
Подставим в это уравнение предположенные выше значения количеств молей и получим :
=
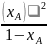


Анализ уравнения показывает, что применение инертного разбавителя в процессе дегидрирования способствует повышению равновесной степени превращения исходного углеводорода. Кроме того, разбавление водяным паром благоприятно для кинетики дегидрирования описывается кинетическим уравнением первого порядка. В то же время, побочная реакция олигомеризации (димеризации) диена, приводящая к коксообразованию и другим продуктам, обычно описывается уравнением второго порядка. Следовательно, разбавление водяным паром значительно снизит ее скорость.
Цель работы: проведение дегидрирования этилбензола в присутствии катализатора КМС на лабораторной контактной установке с целью изучения влияния условной реакции ( температура, объемной скорости подачи, разбавление водяным паром) на материальный баланс и безразмерные характеристики процесса.
2 Экспериментальная часть
2.1 Характеристика сырья и материалов
Физико- химические свойства исходных веществ и продуктов реакции [2] представлены в таблице 1
Таблица 1 – Физико- химические свойства исходных веществ и продуктов реакции
Вещество |
Молярная масса, г/моль |
Плотность, г/с |
Температура кипения,
|
Растворимость в воде |
Растворимость в углеводородах |
Этилбензол |
106.17 |
0.867 |
136.2 |
р |
н.р |
Стирол |
104.15 |
0.906 |
145.2 |
н.р |
р |
Бензол |
78.11 |
0.879 |
80.1 |
р |
р |
Толуол |
92.14 |
0.867 |
110.6 |
0.2 |
сп |