
- •1.Сколько граммов кристаллогидрата сульфата магния нужно взять для приготовления 250 мл раствора с молярной концентрацией эквивалента 0,01 моль/дм3?
- •2.Рассчитать молярную концентрацию эквивалента раствора сульфата цинка, если для его приготовления навеску 3,5989 г кристаллогидрата сульфата цинка растворили в воде в мерной колбе объёмом 500 мл?
- •1.Рассчитать навеску дигидрата трилона б, которая потребуется для приготовления 500 мл раствора с молярной концентрацией эквивалента 0,1 моль/дм3?
- •2.Рассчитать молярную концентрацию эквивалента раствора трилона б, если для его приготовления навеску 4,65 г дигидрата трилона б растворили в воде в мерной колбе объёмом 250 мл?
1.Рассчитать навеску дигидрата трилона б, которая потребуется для приготовления 500 мл раствора с молярной концентрацией эквивалента 0,1 моль/дм3?
-
Дано:
Решение:
V=500 мл=0,5 л
Сf=0,1 моль/дм3
m=?
1.Рассчитать молярную массу Na2C10H14O8N2 ∙ 2H2O
М=(2∙22,99+10∙12,01+14∙1,01+8∙16+2∙14,01)+2∙18=372,24 г/моль
2. Рассчитать молярную массу эквивалента дигидрата трилона Б:
f = 1/2
Мf = М • f

3.Рассчитать навеску, необходимую для приготовления раствора:
m= Сf •Mf •V
m=0,1 моль/дм3 ∙ 186,12 г/моль ∙ 0,5л =9,31 г.
Ответ: Для приготовления 500 мл раствора трилона Б с Cf=0,1 моль/дм3 потребуется навеска дигидрата равная 9,31 г.
2.Рассчитать молярную концентрацию эквивалента раствора трилона б, если для его приготовления навеску 4,65 г дигидрата трилона б растворили в воде в мерной колбе объёмом 250 мл?
-
Дано:
Решение:
m=4,65 г
V=250мл
Сf=?
1.Записать молярную массу эквивалента дигидрата трилона Б:
М=372.24г/моль
f = 1/2
Мf =186.12г/моль
2.Рассчитать число моль эквивалентов KMnO4 в навеске:

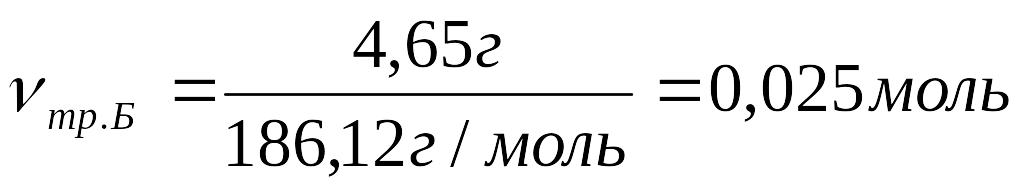
3.Рассчитать молярную концентрацию эквивалента KMnO4:
0,025моль ____ 250 мл
Х моль ____ 1000 мл
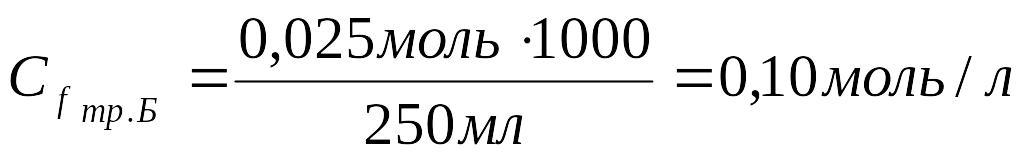
Ответ: Молярная концентрация раствора трилона Б равна 0,10 моль/дм3.
3.Рассчитать объём раствора дигидрата трилона Б с молярной концентрацией эквивалента 0,1 моль/дм3, который потребуется для приготовления 500 мл раствора с молярной концентрацией эквивалента 0,05 моль/дм3?
-
Дано:
Решение:
Сf конц=0,1 моль/дм3
Vразб=500мл
Сf разб=0,05 моль/дм3
Vконц=?
I способ
1.Рассчитать объём раствора по закону эквивалентов:
Сfконц ∙ Vконц= Сf разб ∙ V разб
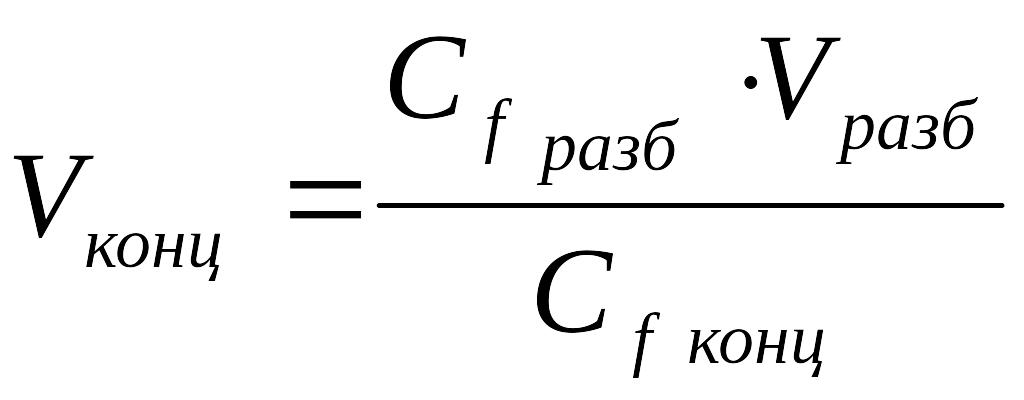


Ответ: Объём концентрированного раствора трилона Б равен 250 мл.
II способ
1.Рассчитать коэффициент разведения:


2. Рассчитать объём раствора:

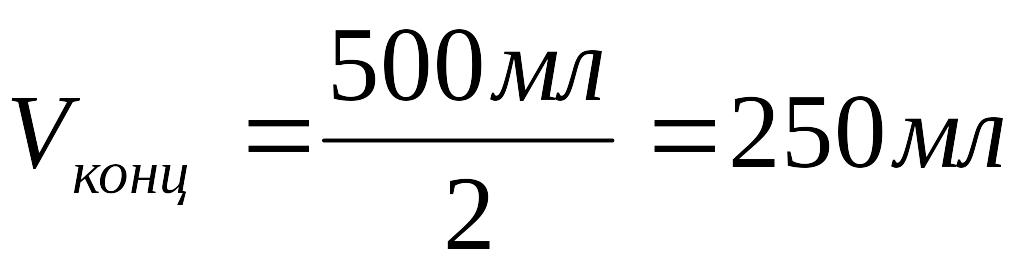
Ответ: Объём концентрированного раствора трилона Б равен 250 мл.
Задачи для самостоятельного решения.
1.Сколько граммов дигидрата трилона Б потребуется для приготовления 500 мл раствора с молярной концентрацией эквивалента 0,05 моль/дм3?
2.Навеска дигидрата трилона Б 23,24 г растворена в воде в мерной колбе объёмом 250 мл. Рассчитать молярную концентрацию этого раствора?
3.Рассчитать объём дигидрата трилона Б с Cf=1моль/дм3, необходимого для приготовления 50 мл раствора с молярной концентрацией эквивалента 0,05 моль/дм3? Перечислить посуду, необходимую для выполнения разведения?
4.Для проведения анализа лаборант взял 5 мл дигидрата трилона Б с молярной концентрацией эквивалента 1 моль/дм3 , поместил в мерную колбу объёмом 50 мл и довёл до метки дистиллированной водой. Рассчитать молярную концентрацию приготовленного раствора?
5.Рассчитать навеску дигидрата трилона Б для приготовления 2,5 л рабочего раствора с молярной концентрацией эквивалента 0,1 моль/дм3?
6.Навеска дигидрата трилона Б 4,63 г растворена в воде в мерной колбе объёмом 500 мл. Рассчитать молярную концентрацию эквивалента приготовленного раствора?
7.Рассчитать объём дигидрата трилона Б с Cf=1 моль/дм3, необходимого для приготовления 200 мл раствора с молярной концентрацией эквивалента 0,01 моль/дм3? Перечислить посуду, необходимую для выполнения разведения?
8..Для проведения анализа лаборант взял 2,5 мл дигидрата трилона Б с молярной концентрацией эквивалента 0,1 моль/дм3 , поместил в мерную колбу объёмом 25 мл и довёл до метки дистиллированной водой. Рассчитать молярную концентрацию приготовленного раствора?
9.Рассчитать навеску рабочего раствора трилона Б дигидрата, необходимую для приготовления 250 мл раствора с молярной концентрацией эквивалента 1 моль/дм3?
10.Навеска дигидрата трилона Б 3,83 г растворена в воде в мерной колбе объёмом 200 мл. Рассчитать молярную концентрацию приготовленного раствора?
11.Рассчитать объём дигидрата трилона Б с Cf=0,1 моль/дм3, необходимого для приготовления 25 мл раствора с молярной концентрацией эквивалента 0,01 моль/дм3? Перечислить посуду, необходимую для выполнения разведения?
12.Для проведения анализа лаборант взял 10,0 мл дигидрата трилона Б с молярной концентрацией эквивалента 1 моль/дм3 , поместил в мерную колбу объёмом 100 мл и довёл до метки дистиллированной водой. Рассчитать молярную концентрацию приготовленного раствора?
13.Сколько граммов дигидрата трилона Б потребуется для приготовления 200 мл раствора с молярной концентрацией эквивалента 0,25 моль/дм3?
3.Определение концентрации рабочего раствора |
Обучающие задачи |
1.При проведении анализа на титрование 10,00 мл раствора кристаллогидрата сульфата цинка (Сf=0,1 моль/л; К=0,9987) израсходовали 10,10 мл рабочего раствора трилона Б. Рассчитать молярную концентрацию эквивалента и титр рабочего раствора?
-
Дано:
Решение:
V соли=10,00 мл
Сf соли=0,01 моль/л
К=0,9987
V тр.Б.=10,10 мл
Т=?; Сf=?
1. Рассчитать молярную концентрацию эквивалента трилона Б:
Сf соли ∙ V соли= Сf тр.Б. ∙ V тр.Б.


2. Записать молярную массу эквивалента трилона Б:
М=372.24г/моль
f = 1/2
Мf =186.12г/моль
3. Рассчитать титр трилона Б:


Ответ: Титр рабочего раствора равен 0,01840 г/мл; молярная концентрация эквивалента рабочего раствора равна 0,09888 моль/л.
2.На титрование 10,00 мл раствора кристаллогидрата сульфата магния (Т=0,01241 г/мл) израсходовали 9,75 мл раствора трилона Б. Рассчитать титр и молярную концентрацию эквивалента рабочего раствора?
-
Дано:
Решение:
Vсоли=10,00 мл
Тсоли=0,01241 г/мл
Vтр.Б.=9,75 мл
Т=?; Сf=?
1. Записать молярную массу эквивалента сульфата магния:
М = 246,38 г/моль
f = 1/2
Mf = 123,19 г/моль
2.Рассчитать молярную концентрацию эквивалента сульфата магния:
3.Рассчитать молярную концентрацию эквивалента трилона Б:
Сf соли∙ Vсоли.= Сf тр.Б. ∙ V тр.Б.
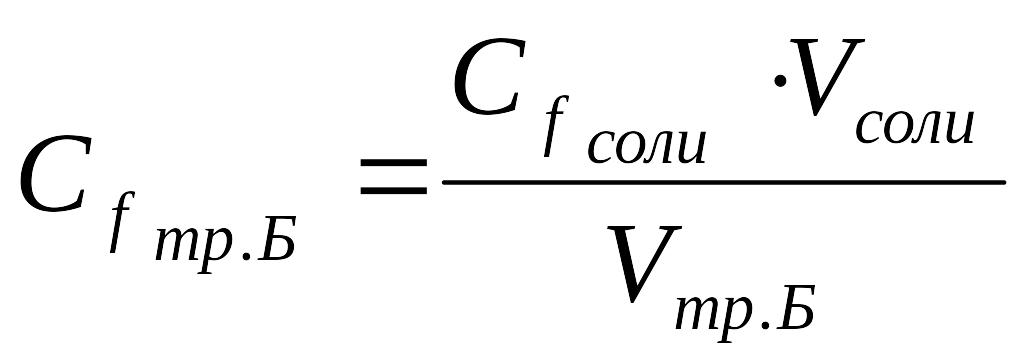
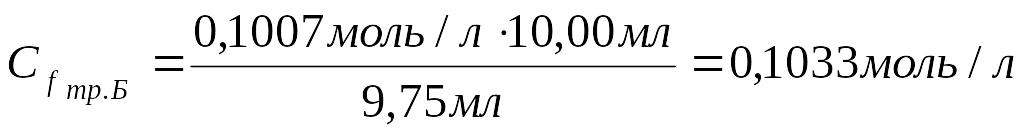
4.Записать молярную массу эквивалента трилона Б:
М=372.24г/моль
f = ½
Мf =186.12г/моль
5.Рассчитать титр трилона Б:
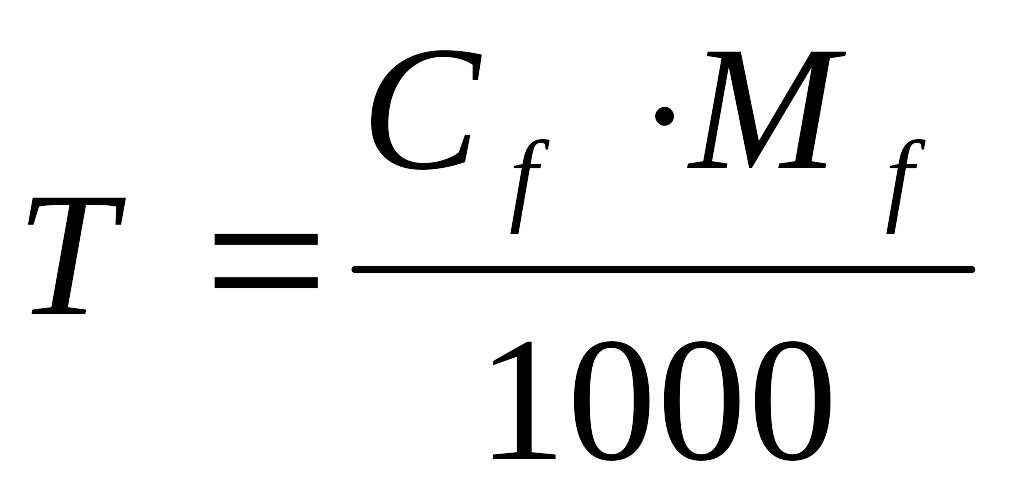

Ответ: Титр рабочего раствора равен 0,01923 г/мл; молярная концентрация эквивалента рабочего раствора равна 0,1033 моль/л.
3.Для приготовления исходного раствора навеска сульфата магния 1,2450 г растворена в мерной колбе на 200 мл. На титрование 5,00 мл этого раствора израсходовали 4,90 мл рабочего раствора трилона Б. Рассчитать молярную концентрацию эквивалента и титр раствора трилона Б?
-
Дано:
Решение:
m=1,2450 г
Vколбы=200 мл
Vсоли=5,00 мл
V тр.Б.=4,90 мл
Т=?; Сf=?
1. Рассчитать титр сульфата магния:

2.Записать молярную массу эквивалента сульфата магния:
М = 246,38 г/моль
f = 1/2
Mf = 123,19 г/моль
3. Рассчитать молярную концентрацию эквивалента сульфата магния:

4. Рассчитать молярную концентрацию эквивалента трилона Б:
Сf соли ∙ Vсоли.= Сf тр.Б. ∙ V тр.Б.

5.Записать молярную массу эквивалента трилона Б:
М=372,24г/моль
f =1/2
Мf =186,12г/моль
6. Рассчитать титр трилона Б:

Ответ: Титр раствора трилона Б равен 0,009596 г/мл; молярная концентрация эквивалента раствора трилона Б равна 0,05156 моль/л.
Задачи для самостоятельного решения.
1.Навеска 1,2456 г кристаллогидрата сульфата магния растворена в воде в мерной колбе объёмом 200 мл. На титрование 20,00 мл этого раствора расходуется 22,40 мл раствора трилона Б.Рассчитать молярную концентрацию эквивалента и титр рабочего раствора?
2.На титрование 25,00 мл раствора кристаллогидрата сульфата цинка (Сf=0,1 моль/дм3;К=0,9578) израсходовали 24,85 мл раствора трилона Б.Рассчитать молярную концентрацию эквивалента титр раствора трилона Б?
3.На титрование 10,00 мл исходного раствора кристаллогидрата MgSО4(Т=0,006353г/мл) израсходовали 9,95 мл рабочего раствора трилона Б. Рассчитать молярную концентрацию эквивалента и титр рабочего раствора?
4.Для приготовления исходного раствора, навеска кристаллогидрата сульфата цинка 3,0589 г растворена в воде в мерной колбе объёмом 250 мл. На 20.00 мл этого раствора при титровании расходуется 21,20 мл устанавливаемого раствора. Определить молярную концентрацию эквивалента и титр рабочего раствора?
5.При проведении анализа на титрование 10,00 мл раствора кристаллогидрата сульфата магния (Сf =0,05 моль/дм3;К=0,9748) израсходовали 9,85 мл раствора трилона Б.Рассчитать молярную концентрацию эквивалента и титр раствора трилона Б?
6.При титровании 5,00 мл исходного раствора кристаллогидрата ZnSО4 (Т=0,007351г/мл) израсходовали 4,75 мл рабочего раствора трилона Б. Рассчитать титр и молярную концентрацию эквивалента раствора трилона Б?
7.Навеска 6,1987 г кристаллогидрата MgSO4 растворена в воде в мерной колбе объёмом 500 мл. На титрование 25,00 мл этого раствора израсходовали 19,25 мл раствора трилона Б.Определить молярную концентрацию эквивалента и титр рабочего раствора?
8.На титрование 5,00 мл раствора кристаллогидрата сульфата цинка (Сf=0,25 моль/дм3;К=0,9897) израсходовали 4,75 мл раствора трилона Б.Рассчитать молярную концентрацию эквивалента титр раствора трилона Б?
9.На титрование 20,00 мл исходного раствора кристаллогидрата MgSО4(Т=0,06548 г/мл) израсходовали 19,85 мл рабочего раствора трилона Б. Рассчитать молярную концентрацию эквивалента и титр рабочего раствора?
10.Для приготовления исходного раствора, навеска кристаллогидрата сульфата цинка 17,5512 г растворена в воде в мерной колбе объёмом 500 мл. На 5,00 мл этого раствора при титровании расходуется 5,35 мл устанавливаемого раствора. Определить молярную концентрацию эквивалента и титр рабочего раствора?
11.При проведении анализа на титрование 20,00 мл раствора кристаллогидрата сульфата магния (Сf =0,1 моль/дм3;К=0,9985) израсходовали 21,40 мл раствора трилона Б.Рассчитать молярную концентрацию эквивалента и титр раствора трилона Б?
12.При титровании 25,00 мл исходного раствора кристаллогидрата ZnSО4 (Т=0,072548 г/мл) израсходовали 25,25 мл рабочего раствора трилона Б. Рассчитать титр и молярную концентрацию эквивалента раствора трилона Б?
13.Навеска 15,3115 г кристаллогидрата сульфата магния растворена в воде в мерной колбе объёмом 250 мл. На титрование 10,00 мл этого раствора расходуется 10,45 мл раствора трилона Б.Рассчитать молярную концентрацию эквивалента и титр рабочего раствора?
14.При проведении анализа на титрование 10,00 мл раствора кристаллогидрата сульфата цинка (Сf =0,05 моль/дм3;К=0,9876) израсходовали 9,65 мл раствора трилона Б.Рассчитать молярную концентрацию эквивалента и титр раствора трилона Б?
15.При титровании 25,00 мл исходного раствора кристаллогидрата MgSО4 (Т=0,01320г/мл) израсходовали 24,75 мл рабочего раствора трилона Б. Рассчитать титр и молярную концентрацию эквивалента раствора трилона Б?
4. Определение концентрации вещества в пробе. |
Обучающие задачи |
1.Для проведения анализа лаборант взял 5,00 мл пробы воды и оттитровал раствором дигидрата трилона Б. На титрование пробы пошло 5,15 мл рабочего раствора (Т=0,009582 г/мл). Рассчитать массовую концентрацию катиона Са2+: мг/л; г/л?
-
Дано:
Решение:
Vпробы=15,00 мл
V тр.Б.=15,15 мл
Ттр.Б=0,00958 г/мл
СfСа2+.=?;мг/л, г/л.
1. Записать молярную массу эквивалента дигидрата трилона Б:
М=372.24г/моль
f = 1/2
Мf =186.12г/моль
2. Рассчитать молярную концентрацию эквивалента трилона Б:

3. Рассчитать молярную концентрацию эквивалента катиона Са2+ по закону эквивалентов:
Сf Са2+∙ V Са2+= Сf тр.Б. ∙ Vтр.Б


4. Записать молярную массу эквивалента катиона Са2+:
М = 40.08г/моль
f = 1/2
Mf = 20.04 г/моль
5. Рассчитать массовую концентрацию катиона Са2+ в пробе (мг/л; г/л):
Сm = Сf ∙ Mf
Сm Са2+.= 0,05302 моль/л ∙ 20,04 г/моль=1,063 г/л
1,0421г г/л ∙ 1000=1063 мг/л
Ответ: Массовая концентрация катиона Са2+ в пробе равна:
Сm Са2+=1,063 г/л
=1063 мг/л
2.Поступила проба сточной воды, содержащая катион Mg2+. На титрование 10,00 мл этой пробы израсходовано 9,85 мл раствора дигидрата трилона Б (Сf=0,05 моль/л; К=0,9976). Рассчитать массовую концентрацию катиона Mg2+ в пробе: мг/мл, г/л, мг/мл?
-
Дано:
Решение:
Vпробы=10,00 мл
V тр.Б.=9,85 мл
Сfтр.Б.=0,05моль/л;
К=0,9976
Сf Mg2+=?; мг/мл, г/л, мг/мл.
1. Рассчитать молярную концентрацию эквивалента катиона Mg2+:
Сf Mg2+ ∙ V Mg2+= Сf тр.Б ∙ V тр.Б


2. Записать молярную массу эквивалента катиона Mg2+:
М = 24,31 г/моль
f = 1/2
Mf = 12,16 г/моль
3. Рассчитать массовую концентрацию катиона Mg2+ в пробе (мг/л; г/л; мг/мл):
Сm = Сf ∙ Mf
Сm Mg2+= 0,04913 моль/л ∙ 12,16 г/моль=0,597 г/л
0,597 г/л ∙ 1000=597 мг/л
0,597 мг/мл
Ответ: Массовая концентрация катиона Mg2+ в пробе равна: Сm Mg2+= 0,597 г/л
=597 мг/л
=0,597 мг/мл
Задачи для самостоятельного решения.
1.Поступила проба сточной воды, содержащей катион Са2+ .На титрование 5,00 мл этой пробы израсходовано 9,95 мл раствора дигидрата трилона Б (Сf=0,1 моль/дм3;К=0,9875).Рассчитать массовую концентрацию катиона Са2+ в пробе: мг/л, г/л, мг/мл?
2.Проба воды, поступившая в лабораторию для определения концентрации катиона Са2+ была оттитрована раствором дигидрата трилона Б (Т=0,09150 г/мл). На титрование 5,00 мл этой пробы пошло 5,15 мл рабочего раствора. Рассчитать массовую концентрацию катиона Са2+ в пробе: мг/л, мг/мл,?
3.В лабораторию поступила проба питьевой воды, содержащей катион Mg2+. На титрование 10,00 мл пробы лаборант израсходовал 9,75 мл рабочего раствора дигидрата трилона Б (Сf=0,05 моль/дм3;К=0,9685).Рассчитать массовую концентрацию катиона Mg2+ в пробе: мг/мл, г/л?
4.Лаборант получил пробу воды, которую необходимо было проверить на содержание катионов Mg2+. Он отмерил 5,00 мл этой пробы и оттитровал их раствором дигидрата трилона Б (Т=0,00935 г/мл), объём рабочего раствора, пошедшего на титрование пробы 5,45 мл. Рассчитать массовую концентрацию катиона Mg2+ в пробе: мг/л, г/л?
5.Поступила проба сточной воды, содержащей катион Mg2+. На титрование 5,00 мл этой пробы израсходовано 4,75 мл раствора дигидрата трилона Б (Сf=0,25 моль/дм3;К=0,9815). Рассчитать массовую концентрацию катиона Mg2+ в пробе: мг/л, г/л, мг/мл?
6.Проба воды, поступившая в лабораторию для определения концентрации катиона Са2+ была оттитрована раствором дигидрата трилона Б (Т=0,01875 г/мл). На титрование 10,00 мл этой пробы пошло 10,15 мл рабочего раствора. Рассчитать массовую концентрацию катиона Са2+ в пробе: мг/л, мг/мл,?
7.В лабораторию поступила проба питьевой воды, содержащей катион Mg2+. На титрование 20,00 мл пробы лаборант израсходовал 19,75 мл рабочего раствора дигидрата трилона Б (Сf=0,1 моль/дм3;К=0,9987).Рассчитать массовую концентрацию катиона Mg2+ в пробе: мг/мл, г/л?
8.Лаборант получил пробу воды, которую необходимо было проверить на содержание катионов Са2+. Он отмерил 10,00 мл этой пробы и оттитровал их раствором дигидрата трилона Б (Т=0,04853 г/мл), объём рабочего раствора, пошедшего на титрование пробы 9,45 мл. Рассчитать массовую концентрацию катиона Са2+ в пробе: мг/л, г/л?
9.Поступила проба сточной воды, содержащей катион Са2+ .На титрование 25,00 мл этой пробы израсходовано 25,35 мл раствора дигидрата трилона Б (Сf=0,05 моль/дм3;К=0,9678). Рассчитать массовую концентрацию катиона Са2+ в пробе: мг/л, г/л, мг/мл?
10.Проба воды, поступившая в лабораторию для определения концентрации катиона Mg2+ была оттитрована раствором дигидрата трилона Б (Т=0,009654 г/мл). На титрование 20,00 мл этой пробы пошло 21,15 мл рабочего раствора. Рассчитать массовую концентрацию катиона Mg2+ в пробе: мг/л, мг/мл,?
11.В лабораторию поступила проба питьевой воды, содержащей катион Са2+. На титрование 5,00 мл пробы лаборант израсходовал 4,95 мл рабочего раствора дигидрата трилона Б (Сf=0,5 моль/дм3;К=0,9784).Рассчитать массовую концентрацию катиона Са2+ в пробе: мг/мл, г/л?
12.Для проведения анализа лаборант взял 5 мл рабочего раствора (Сf=1 моль/дм3) и развёл его в колбе объёмом 50 мл. Полученным раствором он оттитровал пробу воды на содержание катионов Са2+. На титрование 25,00 мл пробы израсходовали 24,75 мл раствора дигидрата трилона Б. Рассчитать массовую концентрацию катиона Са2+ в пробе: мг/л, мг/мл,?
13.Для проведения анализа лаборант взял 2,5 мл рабочего раствора (Сf=0,1 моль/дм3) и развёл его в колбе объёмом 25 мл. Полученным раствором он оттитровал пробу воды на содержание катионов Mg2+. На титрование 20,00 мл пробы израсходовали 19,75 мл раствора дигидрата трилона Б. Рассчитать массовую концентрацию катиона Mg2+ в пробе: мг/л, мг/мл,?
14.Для проведения анализа лаборант взял 5 мл рабочего раствора (Сf=1 моль/дм3) и развёл его в колбе объёмом 100 мл. Полученным раствором он оттитровал пробу воды на содержание катионов Са2+. На титрование 5,00 мл пробы израсходовали 5,25 мл дигидрата трилона Б. Рассчитать массовую концентрацию катиона Са2+ в пробе: мг/л, мг/мл, г/мл?
