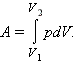- •Кинематика материальной точки. Инерциальные системы отсчёта.
- •Первый и второй законы Ньютона. Сила, масса, импульс.
- •Третий закон Ньютона. Закон сохранения импульса. Центр масс.
- •Работа переменной силы. Потенциальное поле сил.
- •Кинетическая и потенциальная энергия. Законы сохранения энергии.
- •Кинематика вращательного движения. Момент сил. Условия равновесия твердого тела.
- •Основное уравнение динамики вращательного движения. Момент инерции
- •Работа внешних сил при вращательном движении. Кинетическая энергия при вращательном движении.
- •Момент импульса твердого тела. Закон сохранения момента импульса.
- •Гармонические колебания. Скорость, ускорение. Сила в колебательном движении.
- •Энергия гармонического колебания.
- •Вынужденные колебания. Резонанс.
- •Волны. Продольные и поперечные. Уравнение волны.
- •Термодинамический и молекулярно-кинетический методы изучения макроскопических тел. Изопроцессы.
- •Уравнение состояния идеального газа. Универсальная газовая постоянная.
- •Основное уравнение молекулярно-кинетической теории газов для давления и энергии. Выводы из уравнения.
- •Закон распределения молекул по скоростям Максвелла и Больцмана.
- •Число столкновений и средняя длина свободного пробега молекул.
- •Явления переноса в газах. Диффузия.
- •Внутренне трение. Теплопроводность.
- •Внутренняя энергия системы. Степени свободы. Теплоемкость.
- •25. Первое начало термодинамики ми его применение к изопроцессам.
- •Адиабатический процесс и его уравнение.
- •Работа газа при изопроцессах.
- •Обратимые и необратимые процессы. Второе начало термодинамики.
- •Энтропия.
- •Второе начало термодинамики, его статистический смысл.
- •Реальные газы. Уравнение Ван-дер-Ваальса.
- •Изотермы Ван-дер-Ваальса. Внутренняя энергия реального газа.
- •Эффект Джоуля-Томпсона.
- •Электростатическое поле. Закон Кулона.
- •Поток вектора напряженности (смещение). Теорема Остроградского-Гаусса.
- •Электроемкость конденсатора.
- •Диэлектрики в электрическом поле.
- •Поляризация диэлектриков. Электрическое смещение. Диэлектрическая проницаемость среды.
- •Сегнетоэлектрики. Пьезоэффект.
- •Недостатки классической теории электропроводности металлов.
- •Зависимость сопротивления от температуры. Сверхпроводимость.
- •Законы Кирхгофа.
Адиабатический процесс и его уравнение.
Адиабатным называется процесс, происходящий при условии отсутствия теплообмена. Близким к адиабатному может считаться процесс быстрого расширения или сжатия газа. При этом процессе работа совершается за счет изменения внутренней энергии, т.е. , поэтому при адиабатном процессе температура понижается. Поскольку при адиабатном сжатии газа температура газа повышается, то давление газа с уменьшением объема растет быстрее, чем при изотермическом процессе.Процессы теплопередачи самопроизвольно осуществляются только в одном направлении. Всегда передача тепла происходит к более холодному телу. Второй закон термодинамики гласит, что неосуществим термодинамический процесс, в результате которого происходила бы передача тепла от одного тела к другому, более горячему, без каких-либо других изменений. Этот закон исключает создание вечного двигателя второго рода.Показатель адиабаты. Уравнение состояния имеет вид PV? = const.,
где ? = Cp /Cv – показатель адиабаты.Теплоемкость газа зависит от условий, при которых тепло …Если газ нагреть при постоянном давлении P, то его теплоемкость обозначается СV.Если - при постоянном V, то обозначается Cp.
В этом процессе газ остается теплоизолированным от внешней среды. Внутренняя энергия самого газа не остается постоянной, т. к. газ совершает работу при своем расширении (или при сжатии над ним совершается работа).
Общее
уравнение адиабатического процесса
получают из первого начала термодинамики,
полагая
![]() в соответствии с условием теплоизолированности.
в соответствии с условием теплоизолированности.
Тогда уравнение (8) имеет вид
![]() (18)
(18)
Применим (18) к адиабатическому расширению газа. Подставляя (10) в (18) имеем
![]() (19)
(19)
Разделив
(19) на
![]() ,
найдем
,
найдем
![]() (20)
(20)
где
![]() - показатель адиабаты, который в работе
определяется для воздуха.
- показатель адиабаты, который в работе
определяется для воздуха.
Интегрируя, а затем, потенцируя (20) получаем
![]() (21)
(21)
Поскольку
![]() > 1 ,то
> 1 ,то
![]()
![]() >0
и, следовательно, адиабатическое
расширение сопровождается охлаждением,
а сжатие – нагреванием.
>0
и, следовательно, адиабатическое
расширение сопровождается охлаждением,
а сжатие – нагреванием.
Комбинируя выражение (21) с уравнением (6), получаем уравнение, связывающее давление с объемом
![]() (22)
(22)
Уравнение (22) называют уравнением адиабаты.
Работа газа при изопроцессах.
При осуществлении теплообмена между двумя телами в условиях равенства нулю работы внешних сил и в тепловой изоляции от других тел, по закону сохранения энергии . Если изменение внутренней энергии не сопровождается работой, то , или же , откуда . Это уравнение называется уравнением теплового баланса.Применение первого закона термодинамики к изопроцессам.Одним из основных процессов, совершающих работу в большинстве машин, является процесс расширения газа с совершением работы. Если при изобарном расширении газа от объема V1до объема V2 перемещение поршня цилиндра составило l, то работа A совершенная газом равна , или же если V – const, то ? U=?Q. Если сравнить площади под изобарой и изотермой, являющиеся работами, можно сделать вывод, что при одинаковом расширении газа при одинаковом начальном давлении в случае изотермического процесса будет совершено меньше количество работы. Кроме изобарного, изохорного и изотермического процессов существует т.н. адиабатный процесс.
Внутренняя энергия тела может изменяться, если действующие на него внешние силы совершают работу (положительную или отрицательную). Например, если газ подвергается сжатию в цилиндре под поршнем, то внешние силы совершают над газом некоторую положительную работу A'. В то же время силы давления, действующие со стороны газа на поршень, совершают работу A = –A'. Если объем газа изменился на малую величину ΔV, то газ совершает работу pSΔx = pΔV, где p – давление газа, S – площадь поршня, Δx – его перемещение.При расширении работа, совершаемая газом, положительна, при сжатии – отрицательна. В общем случае при переходе из некоторого начального состояния (1) в конечное состояние (2) работа газа выражается формулой:
|
или в пределе при ΔVi → 0:
|
В изохорном процессе (V = const) газ работы не совершает, A = 0.
В изобарном процессе (p = const) работа, совершаемая газом, выражается соотношением:
A = p (V2 – V1) = pΔV.
|
В изотермическом процессе температура газа не изменяется, следовательно, не изменяется и внутренняя энергия газа, ΔU = 0.Первый закон термодинамики для изотермического процесса выражается соотношением Q = A.Количество теплоты Q, полученной газом в процессе изотермического расширения, превращается в работу над внешними телами. При изотермическом сжатии работа внешних сил, произведенная над газом, превращается в тепло, которое передается окружающим телам.Наряду с изохорным, изобарным и изотермическим процессами в термодинамике часто рассматриваются процессы, протекающие в отсутствие теплообмена с окружающими телами. Сосуды с теплонепроницаемыми стенками называются адиабатическими оболочками, а процессы расширения или сжатия газа в таких сосудах называются адиабатическими.Работа газа в адиабатическом процессе выражается через температуры T1 и T2 начального и конечного состояний: A = CV (T2 – T1).