
полезности / Метода Сульфирование и сульфатирование Журавлев, Котельникова 2014
.pdfМинистерство образования и науки Российской Федерации Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования «Кузбасский государственный технический университет имени Т. Ф. Горбачева»
Кафедра технологии органических веществ и нефтехимии
ПРОЦЕССЫ СУЛЬФИРОВАНИЯ И СУЛЬФАТИРОВАНИЯ
Методические указания к лабораторным работам по дисциплине «Химия и технология органических веществ» для
студентов направления подготовки 240100.62 «Химическая технология» профиля 240106.62 «Химическая технология органических веществ» всех форм обучения
Составители В. А. Журавлев Т. С. Котельникова
Утверждены на заседании кафедры Протокол № 23 от 13.05.2014
Рекомендованы к печати учебно-методической комиссией направления 240100.62
Протокол № 13 от 13.05.2014
Электронная копия хранится в библиотеке КузГТУ
Кемерово 2014
1
1. ЦЕЛЬ РАБОТ
На примере реакций сульфатирования высших спиртов и сульфирования ароматических углеводородов изучить указанные реакции. Ознакомиться с теорией процессов сульфатирования и сульфирования, химизмом, механизмом и кинетикой. Получить навыки синтеза и анализа предусмотренных методическими указаниями продуктов, исследовать зависимость свойств получаемых продуктов от концентрации серной кислоты, соотношения субстрат : серная кислота и времени реакции.
2. ТЕОРЕТИЧЕСКИЕ ПОЛОЖЕНИЯ
Процессы сульфатирования и сульфирования находят широкое применение в промышленности основного органического синтеза. Наиболее важны алкансульфокислоты, ароматические сульфокислоты, оксисульфокислоты, аминосульфокислоты.
Сульфокислоты являются промежуточными продуктами в синтезе красителей, лекарственных средств и др. Соли алкансульфокислот – моющие средства, флотореагенты, присадки к техническим маслам. Сульфированные высокомолекулярные соединения используются в качестве ионообменных смол катионообменного типа.
Алкилсульфаты, получаемые процессами сульфатирования высших спиртов и α-олефинов, являются, в частности, анионными поверхностно-активными веществами (ПАВ) и составляют основу моющих средств и текстильно-вспомогательных веществ, эмульгаторов и стабилизаторов пен.
2.1. Процессы сульфирования
Реакциями сульфирования (по международной номенклатуре – сульфонирования) называют химические процессы, в результате которых в органическую молекулу вводится сульфо-
группа -SO3H (-SO2OH) или ее производные (-SO2Cl, -SO2ONa).
Продуктами этих реакций являются сульфокислоты, их соли или хлорангидриды. Сульфокислоты (сульфоновые кислоты) получают на основе как ароматических, так и алифатических углево-
2
дородов. Сульфокислоты обладают всеми характерными свойствами кислот: образуют соли (сульфонаты), галогенангидриды, ангидриды, амиды (сульфамиды) и др. Сульфокислоты гидролизуются до углеводородов, при сплавлении со щелочами группы - SO3H замещаются на ОН-группы.
В качестве сульфирующих агентов используют концентрированную серную кислоту (концентрация не ниже 92 %), олеум, серный ангидрид. Сульфирование серной кислотой является обратимым процессом, сульфирование олеумом и серным ангидридом протекает необратимо.
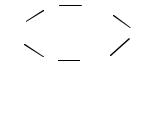
Самый активный из сульфирующих агентов – свободный серный ангидрид (Тпл =16,8 ºС, Ткип= 44,8 ºС), при обычных условиях существует в тримерной форме
.
Сильным сульфирующим агентом является олеум, активность которого возрастает с повышением концентрации избыточного серного ангидрида. Менее энергична серная кислота, так как при ее взаимодействии с углеводородом выделяется вода, тормозящая процесс сульфирования вплоть до полной его остановки. По этой причине при сульфировании серной кислотой требуется относительно высокая температура (80–100 ºС и выше), в то время как олеум и серный ангидрид активны при комнатной и более низкой температуре.
Кроме того, для синтеза сульфокислот в ряде случаев используют процессы сульфохлорирования (например, хлорсульфоновой кислотой – HOSO2Cl) и сульфоокисления (под воздействием SO2 в среде О2). Большое значение эти процессы имеют при получении сульфокислот на основе парафинов, так как последние серной кислотой не сульфируются.
Однако большее распространение в промышленности имеет сульфирование ароматических соединений. При использовании различных сульфирующих агентов эта реакция может быть представлена уравнениями
ArH + H2SO4 ↔ ArSO2OH + H2O; |
(1) |
3 |
|
ArH +H2SO4·SO3 → ArSO2OH + H2SO4 |
(2) |
ArH + SO3 → ArSO2OH |
(3) |
При проведении реакции сульфирования возможно последовательное введение двух и более сульфогрупп, при этом вторая стадия протекает много медленнее первой из-за дезактивирующего влияния сульфогруппы. Сульфирование серным ангидридом и олеумом сопровождается побочной реакцией образования сульфонов
2ArH + 2SO3 → ArSO2Ar + H2SO4 , |
(4) |
чему способствует повышение температуры. Другая побочная реакция – образование ангидридов сульфокислот
2ArSO2OH + SO3 → (ArSO2)2O + H2SO4 , |
(5) |
выход которых повышается при избытке серного ангидрида. Ангидриды сульфокислот путем нагревания с небольшим количеством воды или 92–96%-ной серной кислотой можно переводить в сульфокислоты
(ArSO2)2O + H2O → 2ArSO2OH. |
(6) |
Возможны и другие побочные реакции. При выборе условий проведения процесса это необходимо учитывать (снижать температуру, применять растворители и т. д.).
Реакция сульфирования ароматических соединений, подобно хлорированию и алкилированию, принадлежит к числу типичных процессов электрофильного замещения в ароматическом ядре. Природа электрофильной частицы зависит от условий реакции, но, наиболее вероятно, что это SO3 в свободном состоянии или связанном с «носителем», например в виде H2SO4 SO3. При сульфировании серным ангидридом или олеумом скорость реакции описывается уравнением
r = k[ArH][SO3].
При реакции с серной кислотой наблюдаются более сложные закономерности, причем скорость сульфирования оказывается обратно пропорциональной содержанию воды
4
r =K [ArH]n . [H2O]
Из H2SO4 образуются небольшие количества SO3 по реакции
2H2SO4 ↔ HSO4– + H3O+ + SO3. |
(7) |
Это является одной из главных причин проведения сульфирования избытком серной кислоты.
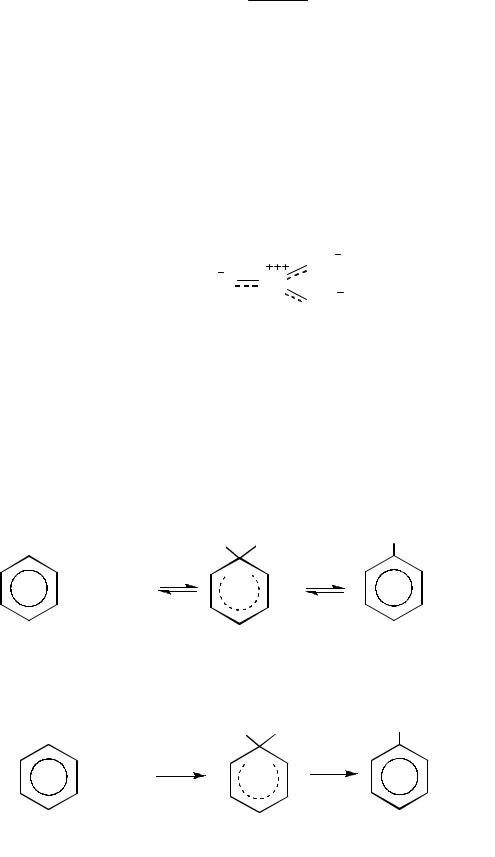
Атаку ароматического субстрата осуществляет атом серы, поскольку он сильно положительно поляризован (электронодефицитен)
δ |
O δ |
δO S |
O δ |
|
При сульфировании серной кислотой образуется ион сульфония
2H2SO4 ↔ H3SO4+ + HSO4– ;
H3SO4+ ↔ SO3H+ + H2O,
который атакует ароматическую молекулу. Механизм сульфирования можно представить следующим образом:
(8)
При сульфировании серным ангидридом процесс может быть изображен следующим образом:
(9)
В практических условиях при сульфировании олеумом или серной кислотой реакционная масса является обычно гетерофаз-
5
ной, причем сама химическая реакция протекает в слое сульфирующего агента. Поэтому на общую скорость процесса влияет растворимость ароматического углеводорода в серной кислоте или олеуме, а также скорость диффузии и поверхность контакта фаз. Последние два фактора существенны при сульфировании олеумом, когда сама химическая реакция протекает быстро. Для процесса с серной кислотой химическая реакция является медленной стадией, определяющей суммарную скорость процесса.
Особое место в процессах сульфирования занимает сульфирование высокомолекулярных соединений с целью получения ионообменных материалов. К ионообменным материалам относят высокомолекулярные соединения, молекулы которых содержат ионогенные группы, способные к диссоциации и обмену подвижных ионов на ионы других соединений в растворе.
Нерастворимые синтетические иониты с трехмерной пространственной структурой макромолекул по знаку заряда обменивающихся ионов делятся на катиониты, аниониты и амфотерные иониты (амфолиты).
Синтетические иониты, используемые в качестве твердых сорбентов, получают, главным образом, на основе сополимеров в виде сферических гранул путем суспензионной (гранульной) полимеризации.
Реакции введения сульфогрупп в полимерную матрицу аналогичны соответствующим реакциям низкомолекулярных соединений, однако в случае сополимеров трехмерной структуры процесс осложняется диффузионными явлениями, затрудняющими полноту превращения. Для обеспечения проницаемости сополимера сульфирующим агентом его подвергают предварительному набуханию в органическом растворителе, который отгоняется в процессе сульфирования.
При синтезе сильнокислотного катионита КУ-2 сульфированию подвергают сополимер стирола с дивинилбензолом (ДВБ). Реакция протекает по схеме

6
CH CH2 |
CH CH2 |
|
|
CH CH2 |
|
CH CH2 |
|
||
|
|
+ nH2SO4 |
|
|
|
. |
(10) |
||
|
|
|
|
|
|
|
|
||
|
|
|
- nH2O |
|
|
|
|||
|
|
|
|
|
|
|
|||
n |
CH CH2 |
|
|
SO |
H |
n |
CH |
CH2 |
|
|
|
3 |
|
|
|
|
|||
Введение сульфогрупп в сополимер стирола с дивинилбензолом осуществляется либо обработкой его серной кислотой (олеумом), либо путем сульфохлорирования хлорсульфоновой кислотой с последующим омылением. Большее распространение имеет метод сульфирования серной кислотой, так называемое прямое сульфирование. После сульфирования, отмывки сульфомассы и отжима избыточной воды получают сульфокатионит, вступающий в реакции ионного обмена по схеме
(11)
На тепловых электростанциях проводят полную деминерализацию воды, поэтому после первой ступени (катионитового фильтра) вода проходит вторую ступень (анионитовый фильтр), где освобождается от анионов
(12)
2.2. Процессы сульфатирования
Реакциями сульфатирования называют реакции взаимодействия сульфатирующего агента со спиртами и олефинами, приводящие к образованию моноэфиров серной кислоты (алкилсер-
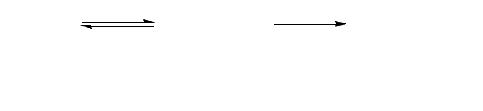
7
ной кислоты). Сульфатирование, таким образом, это частный случай реакции этерификации.
В качестве сырья для получения алкилсерных кислот обычно используют высшие жирные спирты фракции С10−С18, получаемые восстановлением соответствующих синтетических жирных кислот, или α-олефины примерно с таким же числом углеродных атомов.
В зависимости от субстрата получают первичные или вторичные алкилсерные кислоты. Первичные получают сульфатированием первичных высших спиртов, вторичные – взаимодействием сульфатирующего реагента с α-олефинами или вторичными высшими спиртами.
2.2.1.Сульфатирование спиртов
При сульфатировании жирных спиртов образующийся сульфоэфир подвергают нейтрализации водным раствором щелочи с получением первичного алкилсульфоната
(13)
В качестве сульфатирующих агентов применяют концентрированную серную кислоту, хлорсульфоновую кислоту, триоксид серы, сульфаминовую кислоту и N-сульфокарбамид. Реакция сульфатирования спиртов серной кислотой является обратимой, сильноэкзотермичной, главным образом из-за тепла, выделяющегося при растворении серной кислоты в спирте и образующейся воде. Реакционная способность первичных спиртов на порядок выше, чем вторичных. Для повышения равновесной степени превращения спирта применяют концентрированную кислоту (98– 100 %) в избытке по отношению к спирту (2:1). При этих условиях выход первичных алкилсульфатов достигает 80–90 %.
При сульфатировании кислота выполняет одновременно роль и реагента, и катализатора, а реакция протекает с разрывом связи S–O. Наиболее медленной стадией является атака протонированной кислоты молекулой спирта
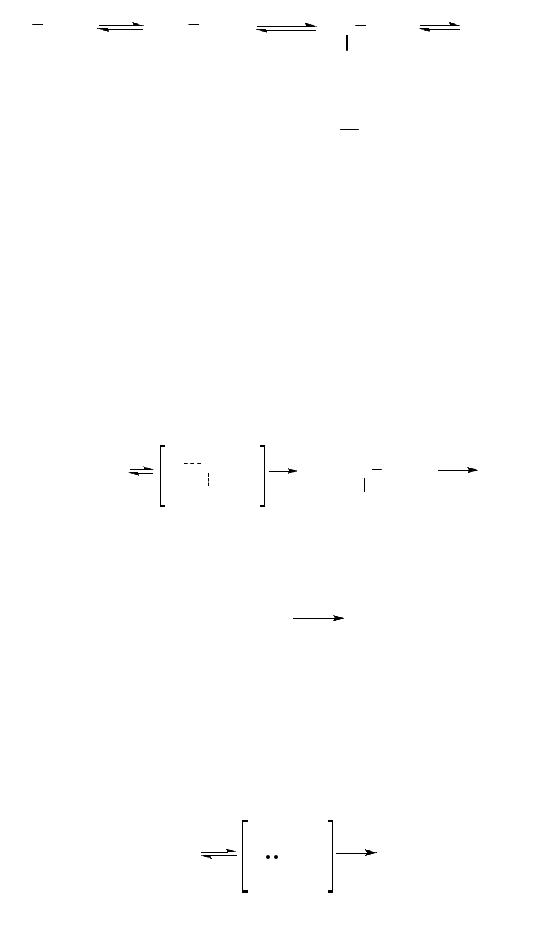
8
(14)
Этому механизму соответствует кинетическое уравнение r=k1h0{[H2SO4][ROH] − K1 [ROSO3H][H2O]},
где k1 – константа скорости прямой реакции; h0 – кислотность среды; K – константа равновесия.
Сульфатирование серной кислотой протекает сравнительно медленно (время реакции 1–3 ч) и тормозится образующейся водой. Для подавления нежелательных побочных реакций процесс проводят при температуре 20–40 ºС.
Со значительно большей скоростью сульфатирование идет под воздействием хлорсульфоновой кислоты, обладающей очень высокой реакционной способностью. Реакция протекает с большой скоростью уже при комнатной температуре, имеет первый порядок по кислоте и спирту
(15)
При повышении температуры, особенно при сульфатировании вторичных спиртов, реакция сопровождается образованием побочных продуктов, например, хлорпроизводных:
(16)
Большое применение в качестве сульфатирующего агента имеет серный ангидрид. Его электрофильные свойства обусловлены наличием вакантных орбиталей на атоме серы, в результате чего происходит взаимодействие ангидрида с кислородным атомом спирта с образованием комплекса, переходящего в алкилсерную кислоту
(17)
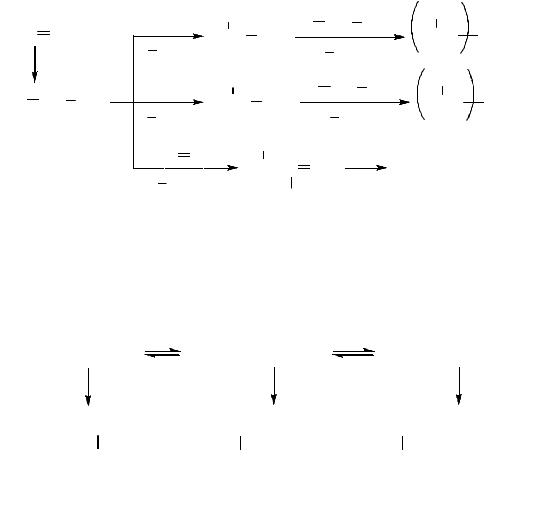
9
Реакция протекает мгновенно с выделением значительного количества тепла, что способствует образованию местных перегревов и побочных продуктов (олефинов, карбонильных соединений, смол), ухудшающих качество целевого продукта. Поэтому при использовании триоксида серы его разбавляют инертным газом и применяют интенсивное перемешивание.
2.2.2. Сульфатирование олефинов
Сульфатирование олефинов протекает путем присоединения серной кислоты по двойным связям согласно правилу Марковникова. Вследствие чего из олефинов образуются вторичные алкилсерные кислоты. Взаимодействие олефинов с серной кислотой протекает последовательно с образованием моно- и диалкилсерных кислот. В качестве побочных продуктов могут образовываться олигомеры, полимеры и, при наличии в серной кислоте воды, спирт. Реакция протекает через промежуточное образование карбкатиона по схеме
(18)
Карбкатионы способны к быстрой изомеризации с переносом гидрид-ионов без деструкции углеродной цепи. Поэтому высшие н-олефины дают смесь вторичных алкилсульфатов с разным положением сульфатной группы
(19)
