
- •По аналитической химии
- •Введение
- •1 Титриметрические методы анализа
- •1.1 Эквивалент. Фактор эквивалентности
- •Задания для самостоятельного расчета
- •1.2 Основные расчетные формулы в титриметрических методах анализа
- •1.3 Расчет содержания вещества методом обратного титрования
- •1.4 Переходные формулы для расчетов концентраций
- •1.5 Расчет ошибок кислотно-основного титрования
- •Задачи для самостоятельного решения
- •2 Расчеты в гравиметрических методах анализа
- •2.1 Основные расчетные формулы в гравиметрических методах анализа.
- •Задачи для самостоятельного решения
- •3 Расчет рН в растворах
- •3.1 Формулы для расчета рН в растворах
- •3.2 Формулы для расчета рН в растворах гидролизующихся солей
- •3.3 Формулы для расчета рН в буферных растворах
- •Задачи для самостоятельного решения
- •Литература
- •Содержание
3 Расчет рН в растворах
3.1 Формулы для расчета рН в растворах
3.1.1 В растворе сильной кислоты рассчитать рН можно по формуле
![]() ,
(35)
,
(35)
где СА - концентрация кислоты.
![]() ,
(36)
,
(36)
где рКW - показатель константы ионизации воды справочные данные.
![]() ,
(37)
,
(37)
где рКА - показатель константы ионизации кислоты справочные данные.
3.1.2 В растворе сильного основания рассчитать рН можно по формуле:
![]() ,
(38)
,
(38)
где СВ - концентрация основания.
![]() (39)
(39)
![]() (40)
(40)
3.2 Формулы для расчета рН в растворах гидролизующихся солей
3.2.1 Если даны соль слабой кислоты и сильного основания
![]() ,
(41)
,
(41)
где СS-концентрация соли.
![]() (42)
(42)
![]() (43)
(43)
3.2.2 Если даны соль сильной кислоты и слабого основания
![]() (44)
(44)
![]() (45)
(45)
![]() (46)
(46)
3.2.3 Если даны соль слабой кислоты и слабого основания
![]() (47)
(47)
![]() (48)
(48)
![]() (49)
(49)
3.3 Формулы для расчета рН в буферных растворах
3.3.1 Кислотные буферные системы
![]() (50)
(50)
![]() (51)
(51)
3.3.2 Основные буферные системы
![]() (52)
(52)
![]() (53)
(53)
Задачи для самостоятельного решения
-
Вычислить рН раствора NaOH,массовая доля 0,2%. Ответ:12,7
-
Вычислить рН раствора KOH,массовая доля 0,19%. Ответ:12,47
-
Вычислить рН раствора HCl,массовая доля 0,36%. Ответ:1,0
-
Вычислить рН раствора HNO3,массовая доля 0,32%. Ответ:1,3
-
Вычислить рН раствора H2SO4,массовая доля 0,4%. Ответ:1,1
-
Вычислить рН раствора NaOH, если плотность раствора ρ ═ 1,002. Ответ:12,95
-
Вычислить рН раствора КOH,если плотность раствора ρ ═ 1,004. Ответ:13,0
-
Вычислить рН раствораHCl, если плотность раствора ρ ═ 1,000. Ответ.1,0
-
Вычислить рН раствора HNO3, если плотность раствора ρ ═ 1,003. Ответ:1,7
-
Вычислить рН раствора H2SO4, если плотность раствора ρ ═ 1,005. Ответ:0,7
-
Вычислить рН 0,1M раствора HNO2 , если К═6,9 · 10-4. Ответ: 2,1
-
Вычислить рН 0.2M раствора HCN , если К═ 5 · 10-10. Ответ:5,0
-
Вычислить рН 0,01M раствора HCOOH, если К═1,8·10-4. Ответ:2,9
-
Вычислить рН 0,02M раствора CH3COOH,если К═1,74·10-5. Ответ:3,24
-
Вычислить рН 0,5M раствора NH4OH, если К═1,76·10-5. Ответ:11,03
-
Вычислить рН 0,2M раствора HJO, если К═2,3·10-11. Ответ:5,67
-
Вычислить рН 0,1M раствора фенола, если К═1,0·10-10. Ответ:5,5
-
Вычислить рН 0,1M раствора гидроксиламина, если К═8,9·10-9. Ответ:9,47
-
Вычислить рН 0,1M раствора хлорноватистой кислоты, если К═2,95·10-8. Ответ: 4,27
-
Вычислить рН 0,1M раствора циановой кислоты, если К═2,7·10-4. Ответ:2,3
-
Вычислить рН 0,1M раствора CH3COONa, если
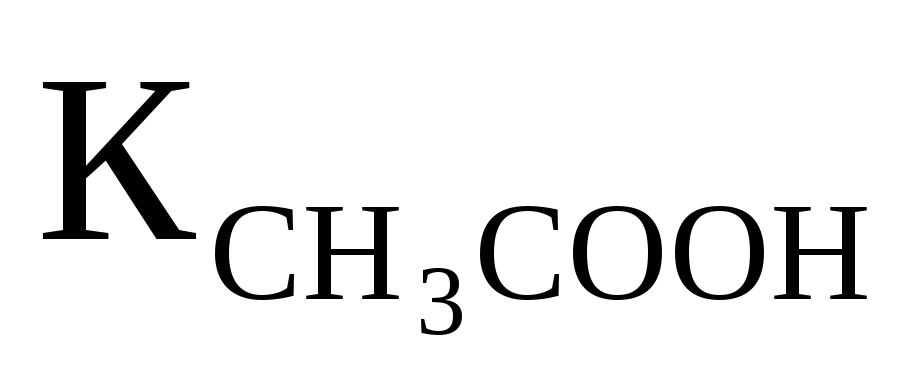 ═1,74·10-5.
Ответ:8,88
═1,74·10-5.
Ответ:8,88 -
Вычислить рН 0,1M раствора NH4Cl, если
 ═1,76·10-5.
Ответ: 5,12
═1,76·10-5.
Ответ: 5,12 -
Вычислить рН 0,1M раствора KCN, если КHCN═6.2·10-10. Ответ:11,15
-
Вычислить рН 0,1M раствора NH4CN, если КHCN═6.2·10-10. Ответ:9,27
-
Вычислить рН 0.1M раствора Na2SO3, если
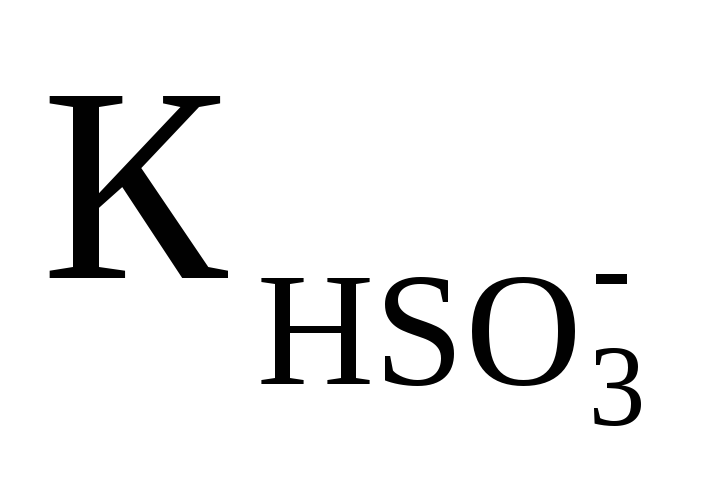 ═ 6.2·10-10.
Ответ:10,1
═ 6.2·10-10.
Ответ:10,1 -
Вычислить рН 0.1M раствора NaHSO3, если
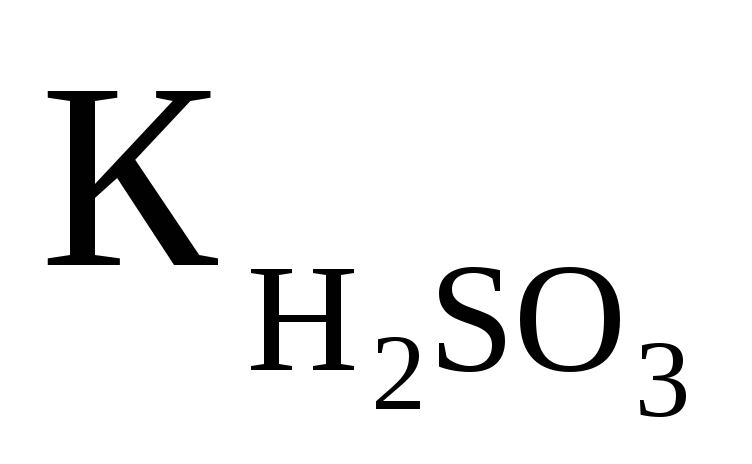 ═1,4·10-2.
Ответ:7,42
═1,4·10-2.
Ответ:7,42 -
Вычислить рН 0,1M раствора раствора Na2 CO3, если
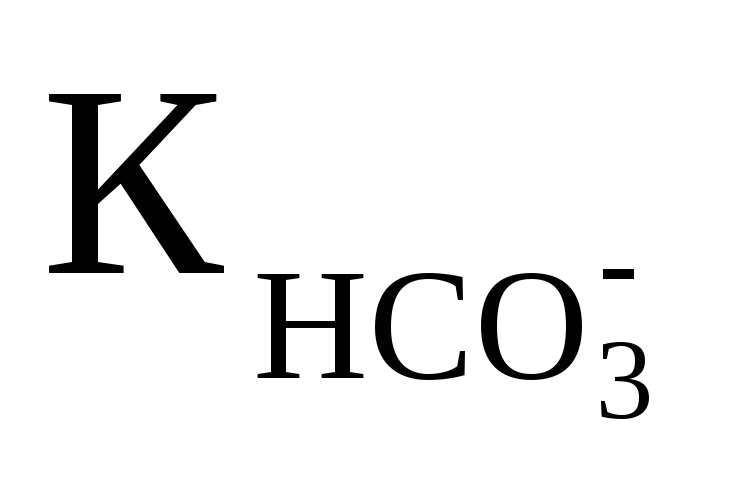 ═ 4,8·10-11.
Ответ:11,66
═ 4,8·10-11.
Ответ:11,66 -
Вычислить рН 0.1M раствора NaHCO3, если
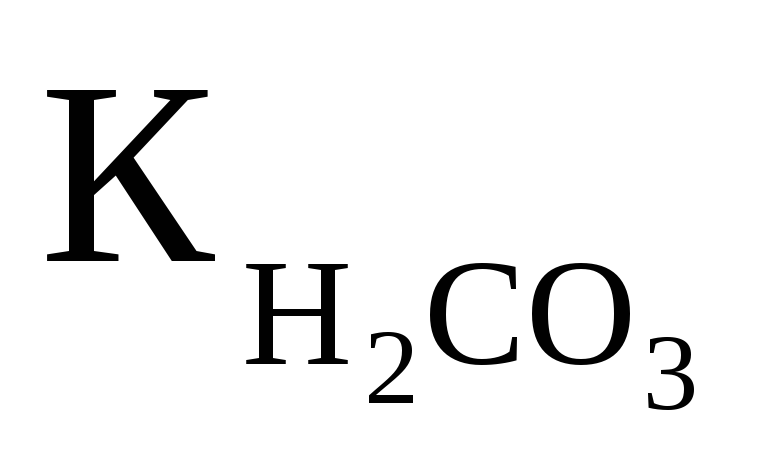 ═4,5·10-7.
Ответ:9,67
═4,5·10-7.
Ответ:9,67 -
Вычислить рН 0,1M раствора (NH4)2CO3, если
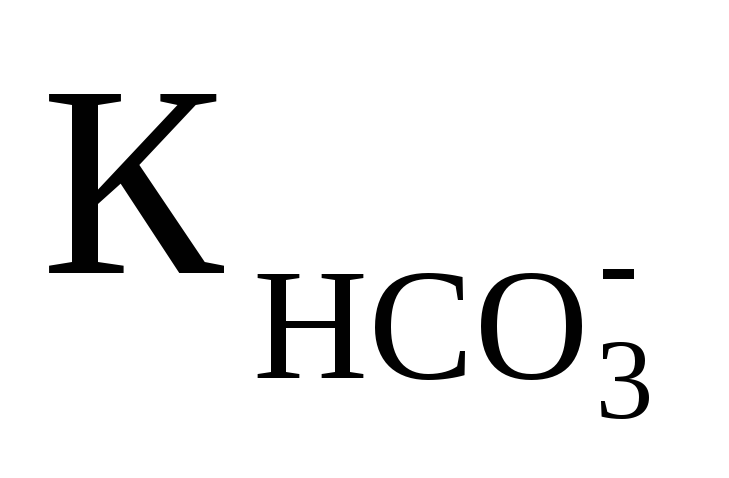 ═4,8·10-11;
═4,8·10-11;
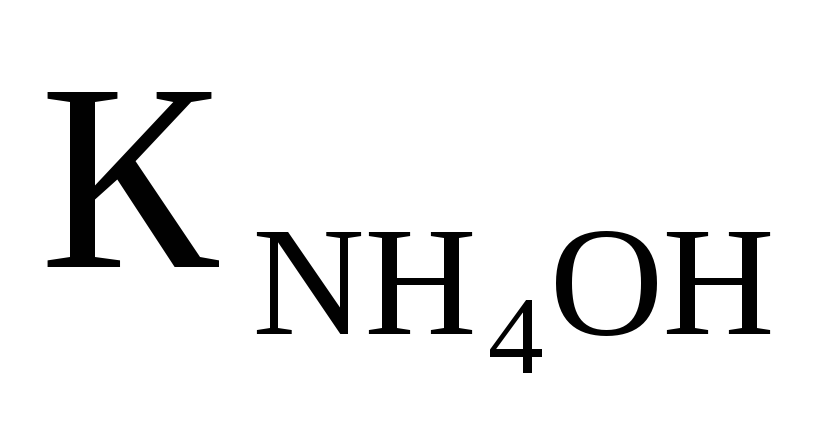 ═1,76·10-5
Ответ:9,19
═1,76·10-5
Ответ:9,19 -
Вычислить рН 0,1M раствора CH3COONH4, если
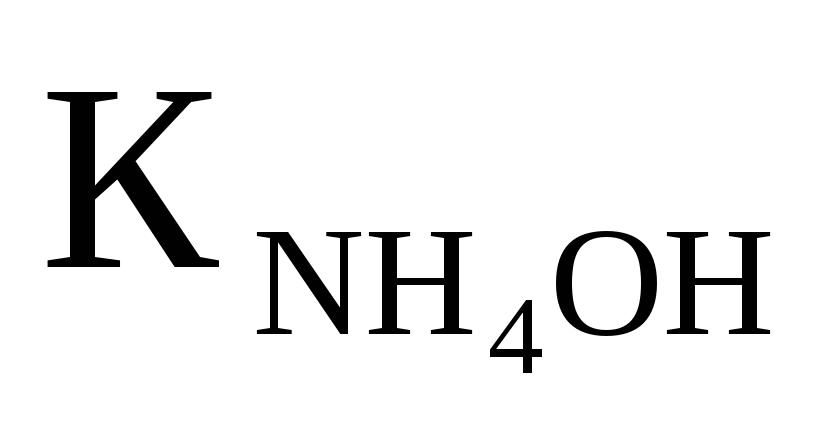 ═1,76·10-5;
═1,76·10-5;
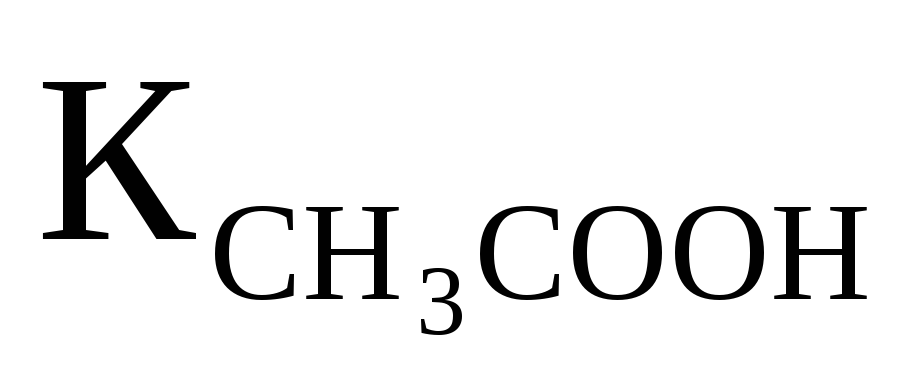 ═1,74·10-5.
Ответ:7,0
═1,74·10-5.
Ответ:7,0
-
Вычислить рН 0,1M раствора Na3PO4, если
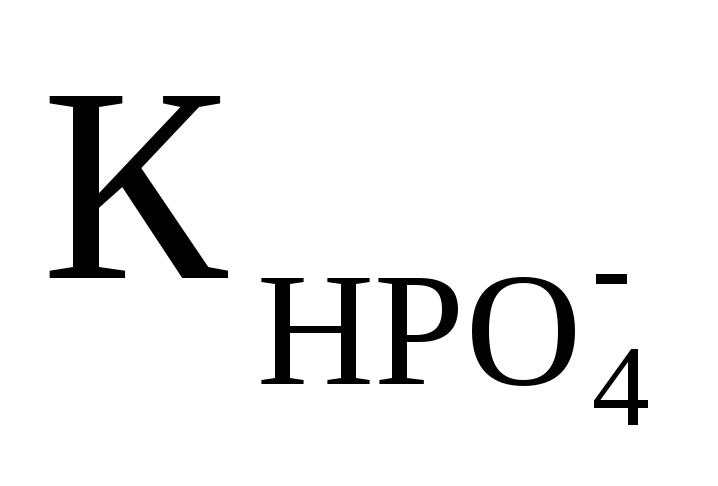 ═5,0·10-3.
Ответ:12,5
═5,0·10-3.
Ответ:12,5 -
Вычислить рН 0,1M раствора NaClO, если КHClO═5,0·10-8.Ответ:10,26
-
Вычислить рН 0,1M раствора NaHS, если
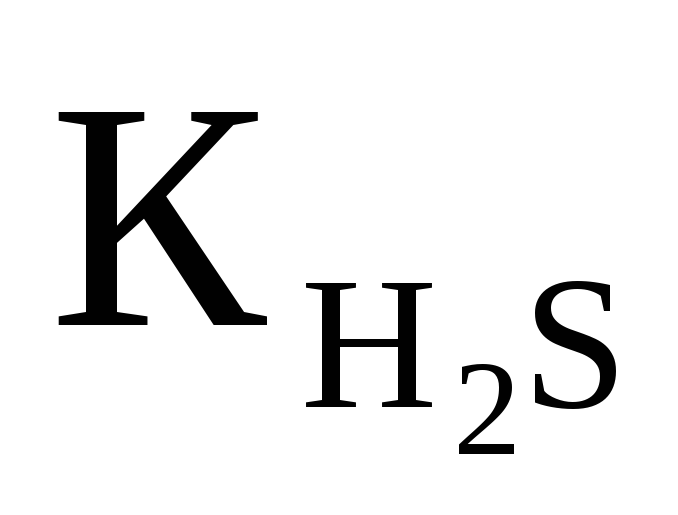 ═1,0·10-7.Ответ:
9,99
═1,0·10-7.Ответ:
9,99 -
Вычислить рН 0,1M раствора K2S, если КHS-═2.5·10-3. Ответ: 12,80
-
Вычислить рН 0,1M раствора HCOONa, если КHCOOH═4,0·10-13. Ответ:8,37
-
Какую навеску хлорида аммония следует растворить в 100 см3 раствора, чтобы рН раствора был равен 6? Ответ:9,36 мг
-
В каком объеме следует растворить навеску ацетата натрия 0,03 г , чтобы получить раствор с рН═8? Ответ: 209 см3
-
Навеску Na2CO3 0,1 г растворили в 500 см3 раствора. Вычислить рН. Ответ:10,80
-
Навеску NaHCO3 0,05 г растворили в 100 см3 раствора. Вычислить рН. Ответ: 9,06
-
Какую навеску нитрата аммония следует растворить в 150 см 3 раствора, чтобы рН раствора стал равен 5? Ответ:2,1 г
-
В каком объеме следует растворить навеску соды Na2CO3 0,005 г , чтобы получить раствор с рН═9? Ответ: 9,92 см3
-
Какую навеску ацетата калия следует растворить в 500 см3 раствора, чтобы рН раствора стал равен 9? Ответ:8,59 г
-
Навеску хлорида аммония NH4 Cl 0,1 г растворили в 250 см3 раствора. Вычислить рН. Ответ:5,69
-
Вычислить рН буферной смеси, состоящей из равных объемов 1,0% растворов муравьиной кислоты и ее натриевой соли. Ответ:3,55
-
Вычислить рН буферной смеси, состоящей из равных объемов 5,0% растворов гидроокиси аммония и хлорида аммония. Ответ:9,41
-
Вычислить рН буферной смеси, состоящей из равных объемов 10,0% растворов йодноватистой кислоты и ее натриевой соли. Ответ:10,57
-
Вычислить рН буферной смеси, состоящей из 0,01 М раствора уксусной кислоты и 0,1 М раствора ее калиевой соли. Ответ:5,76
-
Вычислить рН буферной смеси, состоящей из 0,01 М раствора синильной кислоты и ее 1,0 М раствора калиевой соли. Ответ: 11,30
-
Вычислить рН буферной смеси, состоящей из 0,02 М раствора гидроксида аммония и 0,2 М раствора хлорида аммония. Ответ: 8,24
-
Вычислить рН буферной смеси, состоящей из равных объемов 5,0% растворов азотистой кислоты и ее натриевой соли: Ответ:3,12
-
Вычислить рН буферной смеси, состоящей из равных объемов 0,5% растворов бензойной кислоты и ее натриевой соли.Ответ: 4,13
-
Вычислить рН буферной смеси, состоящей из равных объемов1,0% растворов бромноватистой кислоты и ее натриевой соли: Ответ:8,53
-
Вычислить [Н+] и рН в 1н растворе СН3СООН. Ответ: 4,24∙10-3 ; 2,37
-
Вычислить [Н+] и рН в 0,01н растворе NH4ОН. Ответ: 2,37 ∙10-11; 10,625
-
Вычислить [Н+] и рН в 0,1н растворе Н2С2О4. Ответ: 5,2∙10-3; 1,284
-
рН раствора равно 2,63. Чему равны в нем концентрации [Н+] и [OН+]? Ответ: 2,34 ∙10-3; 4,27∙10-12
-
рН раствора равно 12,45. Чему равны в нем концентрации [Н+] и [OН+]? Ответ: 3, 55 ∙10-13; 2,8 ∙10-3
-
Раствор содержит 0,056 моль/л NH4OH и 0,1 моль/л NH4Cl. Чему равен рН этого раствора и как он изменится при прибавлении к 1л этого раствора: а) 0,001 моль NaOH; б) 0,001 моль HCl ? Ответ:8,99; 9,0102; 8,986.
-
На сколько единиц изменится рН раствора, содержащего NаОН в концентрации 2·10-5 М при прибавлении к 1л его 0,001 моль: а) NаОН б) НСl? Ответ :на 2; на 6.
