2 сем / Лабораторный журнал
.docx

МИНОБРНАУКИ РОССИИ
Федеральное государственное бюджетное образовательное учреждение высшего образования
«МИРЭА – Российский технологический университет»
РТУ МИРЭА
|
|
Институт тонких химических технологий им. М.В. Ломоносова |
|
(наименование Института)
|
|
Кафедра Физической химии им. Я.К. Сыркина |
|
(наименование кафедры)
Лабораторный журнал по физической химии
Раздел «Кинетическая химия»
Работу выполнила
Студентка группы ХББО-02-16
Иванова Елена Анатольевна
Работу проверила
Зобнина Аэлита Николаевна
Москва, 2019
Лабораторная работа №1
Изучение кинетики омыления сложных эфиров щелочью
СН3СOOС3H7 + OH- = CH3COO- + C3H7OH
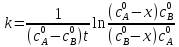
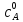 –
начальная
концентрация эфира, моль/л,
–
начальная
концентрация эфира, моль/л,
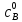 –
начальная
концентрация щелочи, моль/л,
–
начальная
концентрация щелочи, моль/л,
x – число молей прореагировавшего вещества в литре ко времени t.
|
Время, мин |
pH |
pOH |
моль/л |
x, моль/л |
|
|
|
k,
|
|
1 |
11,60 |
1,97 |
0,0107 |
0,0028 |
0,0276 |
2,577 |
0,947 |
7,96 |
|
2 |
11,40 |
2,17 |
0,0068 |
0,0067 |
0,0237 |
3,500 |
1,253 |
13,03 |
|
3 |
11,30 |
2,27 |
0,0054 |
0,0081 |
0,0223 |
4,147 |
1,422 |
12,03 |
|
4 |
11,16 |
2,41 |
0,0039 |
0,0096 |
0,0208 |
5,345 |
1,676 |
12,78 |
|
5 |
11,06 |
2,51 |
0,0031 |
0,0104 |
0,0200 |
6,470 |
1,867 |
12,48 |
|
6 |
11,00 |
2,57 |
0,0027 |
0,0108 |
0,0196 |
7,280 |
1,985 |
11,56 |
|
7 |
10,86 |
2,71 |
0,0019 |
0,0115 |
0,0189 |
9,669 |
2,269 |
12,31 |
|
8 |
10,76 |
2,81 |
0,0015 |
0,0119 |
0,0185 |
11,913 |
2,478 |
12,32 |
|
9 |
10,68 |
2,89 |
0,0013 |
0,0122 |
0,0182 |
14,121 |
2,648 |
12,07 |
|
10 |
10,60 |
2,97 |
0,0011 |
0,0124 |
0,0180 |
16,774 |
2,820 |
11,88 |
pKw=13,57 (T=35°C)

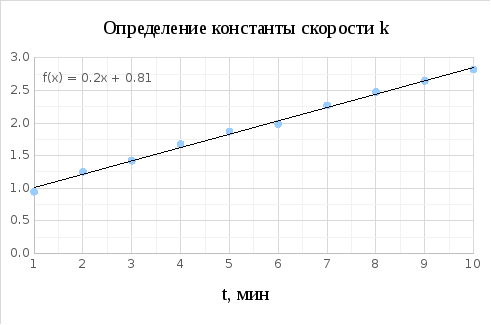
По графику определяем
pH0=11,7,
откуда

mколба+вода=66,62 г, mколба+раствор=66,94 г
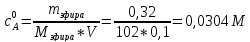
Графическое определение константы скорости.

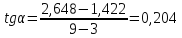
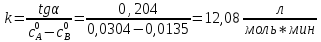
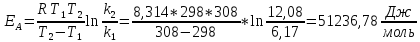
Лабораторная работа №2
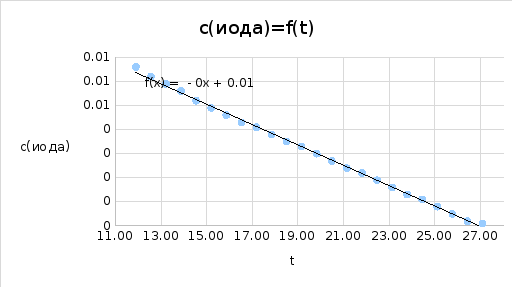
Кинетика реакции иодирования ацетона
СН3СOСH3 + I2 + H2O = CH3COCH2I + H3O+ + I-
Данная реакция является многостадийной, причем первая стадия – лимитирующая, поэтому скорость реакции определяется скоростью этой стадии:
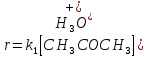
Опыт №2. T=298 K,
с(HCl)=0,12 моль/л (3 мл 1М в 25 мл),
с(ацетона)=1,088 моль/л (2 мл, ρ=0,7899 г/см3, М=58,08 г/моль в 25 мл)
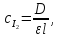

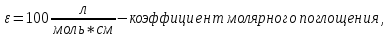
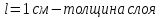
|
Время, мин |
Оптическая плотность, D |
Концентрация иода, с |
|
11,89 |
0,66 |
0,0066 |
|
12,55 |
0,62 |
0,0062 |
|
13,22 |
0,59 |
0,0059 |
|
13,88 |
0,56 |
0,0056 |
|
14,54 |
0,52 |
0,0052 |
|
15,20 |
0,49 |
0,0049 |
|
15,86 |
0,46 |
0,0046 |
|
16,52 |
0,43 |
0,0043 |
|
17,18 |
0,41 |
0,0041 |
|
17,84 |
0,38 |
0,0038 |
|
18,50 |
0,35 |
0,0035 |
|
19,16 |
0,33 |
0,0033 |
|
19,82 |
0,3 |
0,003 |
|
20,48 |
0,27 |
0,0027 |
|
21,15 |
0,24 |
0,0024 |
|
21,81 |
0,22 |
0,0022 |
|
22,47 |
0,19 |
0,0019 |
|
23,13 |
0,16 |
0,0016 |
|
23,79 |
0,13 |
0,0013 |
|
24,45 |
0,11 |
0,0011 |
|
25,11 |
0,08 |
0,0008 |
|
25,77 |
0,05 |
0,0005 |
|
26,43 |
0,02 |
0,0002 |
|
27,09 |
0,01 |
0,0001 |

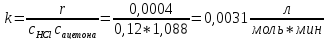
Лабораторная работа №3
Изучение кинетики гидролиза уксусного ангидрида
(CH3CO)2 + H2O = 2CH3COOH
|
Время, мин |
к, мкСм/см |
|
|
ln( |
kcк, мин-1 |
|
|
0 |
184,7 |
0,341 |
1,098E-07 |
-16,025 |
- |
|
|
1 |
217,4 |
0,473 |
9,661E-08 |
-16,153 |
0,992 |
|
|
2 |
245,3 |
0,602 |
8,370E-08 |
-16,296 |
0,492 |
|
|
3 |
267,7 |
0,717 |
7,221E-08 |
-16,444 |
0,325 |
|
|
4 |
285,6 |
0,816 |
6,230E-08 |
-16,591 |
0,241 |
|
|
5 |
300 |
0,9 |
5,387E-08 |
-16,737 |
0,191 |
|
|
6 |
311,8 |
0,972 |
4,665Е-08 |
-16,881 |
0,158 |
|
|
7 |
321,9 |
1,04 |
4,025E-08 |
-17,028 |
0,134 |
|
|
8 |
330,3 |
1,09 |
3,477E-08 |
-17,174 |
0,117 |
|
|
9 |
337,7 |
1,14 |
2,983E-08 |
-17,328 |
0,103 |
|
|
10 |
344 |
1,18 |
2,553E-08 |
-17,483 |
0,092 |
|
|
11 |
349,1 |
1,22 |
2,200E-08 |
-17,632 |
0,083 |
|
|
12 |
353,3 |
1,25 |
1,905E-08 |
-17,776 |
0,075 |
|
|
13 |
356,9 |
1,27 |
1,649E-08 |
-17,920 |
0,069 |
|
|
14 |
360 |
1,3 |
1,427E-08 |
-18,065 |
0,063 |
|
|
15 |
362,5 |
1,31 |
1,246E-08 |
-18,201 |
0,059 |
|
|
16 |
364,7 |
1,33 |
1,086E-08 |
-18,338 |
0,055 |
|
|
17 |
366,7 |
1,34 |
9,399E-09 |
-18,483 |
0,051 |
|
|
18 |
368,3 |
1,36 |
8,224E-09 |
-18,616 |
0,048 |
|
|
19 |
369,8 |
1,37 |
7,116E-09 |
-18,761 |
0,045 |
|
|
20 |
371 |
1,38 |
6,227E-09 |
-18,894 |
0,042 |
|
|
21 |
372,1 |
1,385 |
5,410E-09 |
-19,035 |
0,040 |
|
|
22 |
373 |
1,391 |
4,739E-09 |
-19,167 |
0,038 |
|
|
23 |
373,8 |
1,397 |
4,142E-09 |
-19,302 |
0,036 |
|
|
24 |
374,5 |
1,403 |
3,618E-09 |
-19,437 |
0,034 |
|
|
25 |
375 |
1,406 |
3,243E-09 |
-19,547 |
0,033 |
|
|
26 |
375,5 |
1,41 |
2,868E-09 |
-19,670 |
0,031 |
|
|
27 |
376 |
1,414 |
2,492E-09 |
-19,810 |
0,030 |
|
|
28 |
376,4 |
1,417 |
2,192E-09 |
-19,939 |
0,029 |
|
|
29 |
376,7 |
1,419 |
1,966E-09 |
-20,047 |
0,028 |
|
|
30 |
377 |
1,421 |
1,739E-09 |
-20,170 |
0,026 |
|
|
31 |
377,2 |
1,423 |
1,589E-09 |
-20,260 |
0,026 |
|
|
32 |
377,5 |
1,425 |
1,362E-09 |
-20,414 |
0,025 |
|
|
33 |
377,7 |
1,427 |
1,211E-09 |
-20,532 |
0,024 |
|
|
34 |
377,8 |
1,427 |
1,136E-09 |
-20,596 |
0,023 |
|
|
35 |
378 |
1,429 |
9,845E-10 |
-20,739 |
0,022 |
|
|
36 |
378,2 |
1,430 |
8,333E-10 |
-20,906 |
0,021 |
|
|
37 |
378,3 |
1,431 |
7,576E-10 |
-21,001 |
0,021 |
|
|
38 |
378,4 |
1,432 |
6,819E-10 |
-21,106 |
0,020 |
|
|
39 |
378,5 |
1,433 |
6,062E-10 |
-21,224 |
0,019 |
|
|
40 |
378,6 |
1,433 |
5,305E-10 |
-21,357 |
0,019 |
|
|
41 |
378,7 |
1,434 |
4,548E-10 |
-21,511 |
0,018 |
|
|
42 |
378,8 |
1,435 |
3,791E-10 |
-21,693 |
0,018 |
|
|
43 |
378,9 |
1,436 |
3,033E-10 |
-21,916 |
0,017 |
|
|
44 |
379,1 |
1,437 |
1,517E-10 |
-22,609 |
0,016 |
|
|
45 |
379,2 |
1,438 |
7,585E-11 |
-23,302 |
0,015 |
|
|
46 |
379,3 |
1,439 |
0 |
- |
- |
|
|
kcр |
0,09 |
|||||
Для упрощения
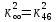
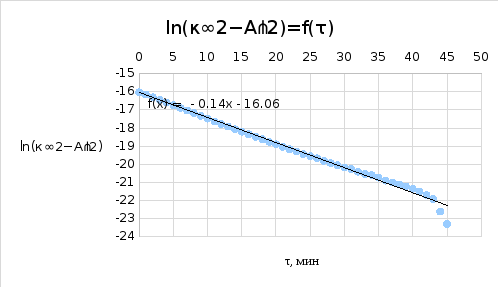
 (по тангенсу угла
наклона)
(по тангенсу угла
наклона)
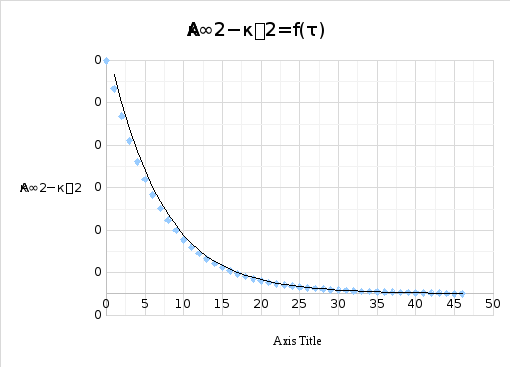
Концентрация уменьшится в два раза примерно через 5,3 мин, следовательно:
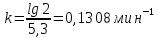

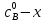 ,
,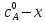 ,
моль/л
,
моль/л
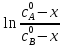

 *107
*107