
- •МИКРОБНЫЕ
- •Сферы применения микробных полисахаридов
- •Структура ксантана
- •ксантан Е415
- •род Xanthomonas
- •Состав питательной среды для культивирования Xanthomonas сampestris
- •Условия культивирования
- •ТЕХНОЛОГИЧЕСКАЯ СХЕМА ПОЛУЧЕНИЯ КСАНТАНА
- •Диализ
- •Декстраны — (С6Н10О5)n — полисахариды бактериального происхождения, построены из ,D-
- •Использование декстранов
- •ПОЛУЧЕНИЕ ДЕКСТРАНОВ
- •Декстрансахараза является экзоферментом, и ее концентрация в культуральной среде значительна. Поэтому возможен процесс
- •БИОРАЗЛАГАЕМЫЕ ПОЛИМЕРЫ
- •Цены на некоторые биодеградируемые и традиционные полимеры, выраженные по отношению к полиэтилену
- •Поли-3-гидроксибутират – биоразлагаемый полимер
- •Alcaligenes eutrophus (Ralstonia eutropha)
- ••Электронно-микроскопический снимок срезов клеток M. extorquens G10 на стадии синтеза ПГБ
- •ТЕХНОЛОГИЧЕСКАЯ СХЕМА ПОЛУЧЕНИЯ ПОЛИ-3- ГИДРОКСИБУТИРАТА
- •БИОГЕОТЕХНОЛОГИЯ
- •Использование бактериального выщелачивания в биотехнологии
- •Выщелачивающая среда
- •ПИРИТ FeS2
- •Механизм бактериального окисления сульфидов
- •При благоприятных условиях из концентратов в раствор за 1 ч переходит Cu до
- •II. Электрохимическая модель. Процесс окисления вещества связан с биохимическими реакциями в живой клетке
- •Схема бактериального выщелачивания меди из куч или отвалов руды
- •Кучное
- •Схема подземного бактериального выщелачивания медной руды
- •Полупромышленная установка чанового бактериального выщелачивания
- ••Пульпа с соотношением твердого и жидкого компонентов 1 : 5 вместе с биомассой
- •Современный карьер на предприятии, добывающем рудное золото
- •Технологии бактериального выщелачивания упорных золотосодержащих концентратов
- •Олимпиадинский горнообогатительный комбинат (Россия, Красноярский край)
- •Технология бактериального выщелачивания концентратов BIONORD®
- •Технология бактериального выщелачивания концентратов BIONORD®
- ••Карьер «Восточный» Олимпиадинского месторождения. Самый крупный в России и один из крупнейших в
- ••Цех бактериального выщелачивания - технологии биологического окисления сульфидных золотосодержащих руд. Этот метод является
- •Кучное выщелачивание золота
МИКРОБНЫЕ
ПОЛИСАХАРИДЫ
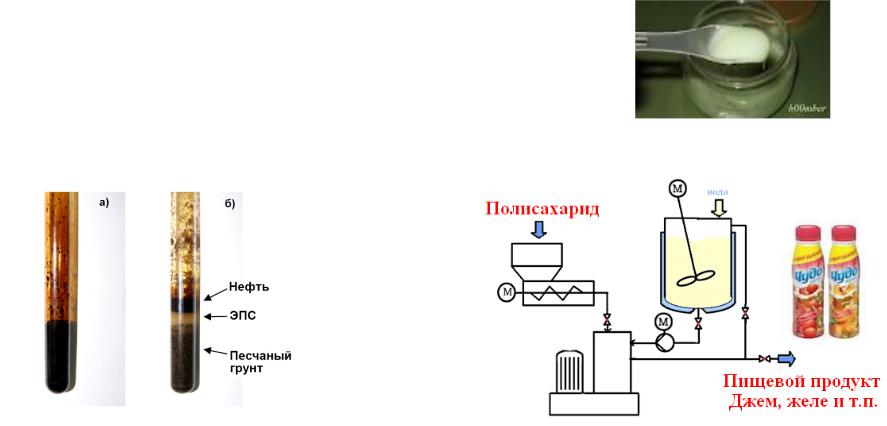
Сферы применения микробных полисахаридов
Пищевая промышленность Фармацевтическая промышленность Химическая промышленность Лакокрасочная промышленность Косметическая промышленность
Нефтегазо- и горнодобывающая промышленность
Песчаный грунт, пропитанный нефтью: |
Установка для получения |
|
а) без обработки (контроль), б) после |
||
пищевых продуктов, содержащих |
||
обработки полисахаридом метилотрофной |
||
микробные полисахариды |
||
бактерии (Ю.А.Троценко и др., 2009). |
||
|

Структура ксантана
Xanthomonas сampestris
фитопатоген
Основная цепь ксантана (кор) построена аналогично целлюлозе (1-4–β- глюкопираноза), а в ответвлениях кора — трисахарид, состоящий из β-D-маннозы, β- D-глюкуроновой кислоты и α-D-маннозы. Остатки глюкуроновой кислоты и кислые пировиноградные группы придают молекулам ксантана анионный характер.
Повышение нефтедобычи, буровые работы. Стабилизатор и загуститель в косметической
и пищевой промышленности Е 415
ксантан Е415
•Ксантановая смола –(USD 5 000.- за тонну) - оптимизатор буровых растворов
•Физические свойства:
•1. Высокая вязкость при очень низкой концентрации (до 2%). Высокоэффективный загуститель
•2. Псевдопластичность. Вязкость раствора снижается с возрастающей скоростью сдвига. Вязкость раствора восстанавливается при прекращении перемешивания, что идеально подходит для промышленного использования
•3. Температурная толерантность. Вязкость раствора практически не изменяется в широком диапазоне температур от -4 до 120оС, в присутствии соли (например: 0.1 NaCl)
•4. Солевая толерантность. Ксантан обычно сохраняет свои свойства в присутствии солей (таких, как NaCl)
•5. Кислотно-щелочная толерантность. Вязкость раствора практически не изменяется в широком диапазона рН от 2 до 12 ед. рН
•6. Устойчивость к окислению и ферментативному гидролизу.
•7. Эмульгирующие свойства (масло в воде)

род Xanthomonas
•Клетки бактерий рода Xanthomonas имеют вид палочек; (0,4–0,7)х(0,7–1,8) мкм. Грамотрицательные, неспороносные, подвижные Колонии бактерий на мясо-пептонном агаре и картофельном агаре округлые, диаметром около 3–5 мм, выпуклые, маслянистой консистенции, край ровный,цвет желтый.
•Характерной чертой рода является потребность бактерий в факторах роста (аминокислотах).
•Неорганические источники азота и серы плохо усваиваются бактериями.
Состав питательной среды для культивирования Xanthomonas сampestris
•Источник углерода - углеводы - глюкоза и сахароза 2,5–4 %, гидролизат кукурузного крахмала (избыток углерода);
•Источник азота – органические вещества - дрожжевые препараты, экстракт соевой муки, кукурузный экстракт, мясной пептон, молочная сыворотка, мочевина;
•Источник фосфора K2HPO4 (не более 0,1 %);
•микроэлементы.
Условия культивирования
•Обеспечение асептических условий.
•Оптимальная температура 28 °С. Оптимальный рН 6,5–7,5 (подтитровка 5 М NaOH).
•Высокий уровень аэрации необходим в экспоненциальной фазе роста и нежелателен в начале стационарной фазы — периоде образования ксантана.
•Интенсивное перемешивание ферментационной среды. Синтез ксантана идет в течение 72 ч. Конверсия углеводов в ЭПС 67%.
•Двухступенчатый глубинный способ культивирования.
•1).накопление клеток микроорганизма в среде следующего состава, г/л: K2НРО4 — 5, сульфат аммония — 2, лимонная кислота — 1, борная кислота — 0,6, сульфат магния — 0,2, хлорид железа — 0,24, сульфат цинка — 0,212, хлорид кальция
— 0,438, глицерин — 20. На данном этапе бактерии растут до полного исчезновения азота в среде.
•2).Добавляют концентрированный раствор глюкозы (фруктозы, сахарозы или другой источник углерода), и на второй ступени происходит накопление ЭПС.
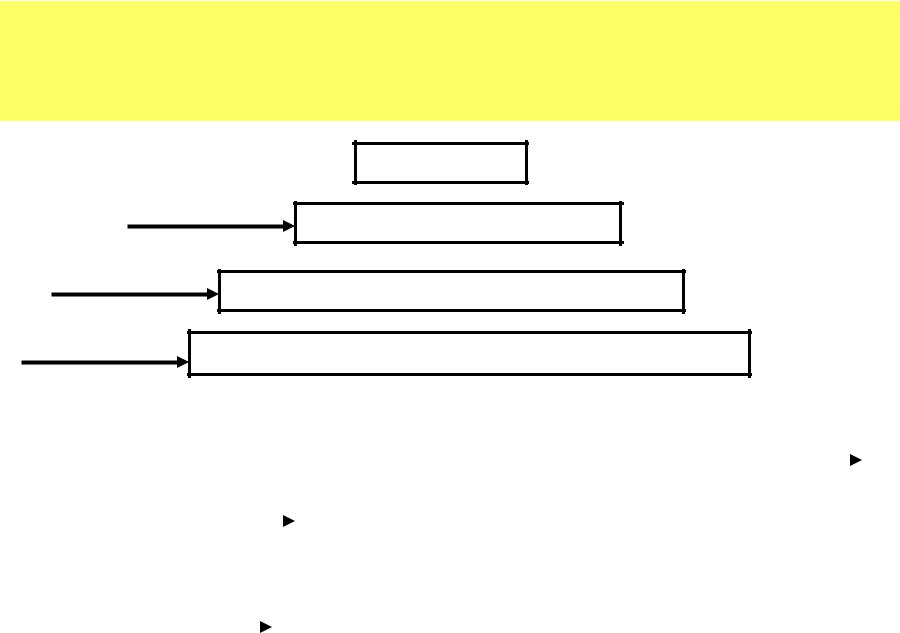
ТЕХНОЛОГИЧЕСКАЯ СХЕМА ПОЛУЧЕНИЯ КСАНТАНА
Ферментация
бактерицид
Химическая стерилизация
гексахлоран, формальдегид
этанол |
разбавление водным спиртом (33–40%) |
|
NaCl или CaCl2 |
добавление соли (2 % NaCl или 0,2 % CaCl2) |
|
|
|
|
|
|
|
|
нагревание |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
биомасса |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
этанол |
центрифугирование или фильтрация |
|||||||||||||
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Осаждение этанолом 55%об. |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
диализ |
|
|
||||
|
этанол |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
переосаждение этанолом 55%об. |
|
|
||||||||||
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Сушка |
|
|
|
|||
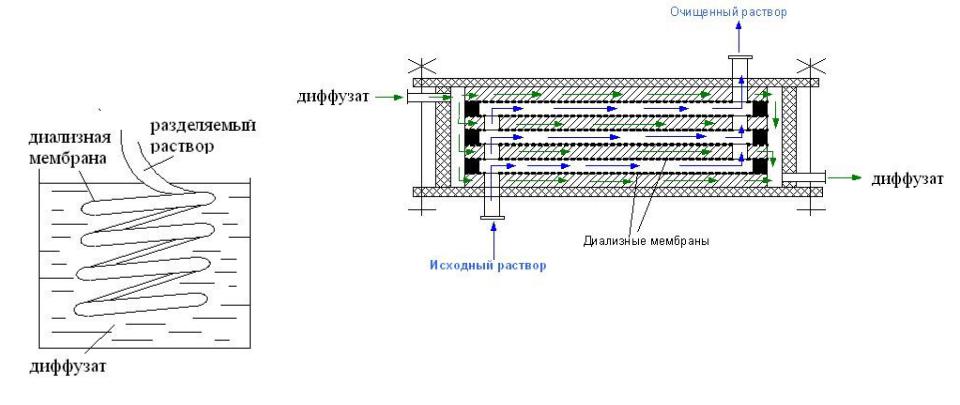
Диализ
освобождение растворов высокомолекулярных веществ от низкомолекулярных соединений при помощи полупроницаемой мембраны.
Конструкция диализатора типа «фильтр-пресс»
Конструкция диализатора змеевикового типа
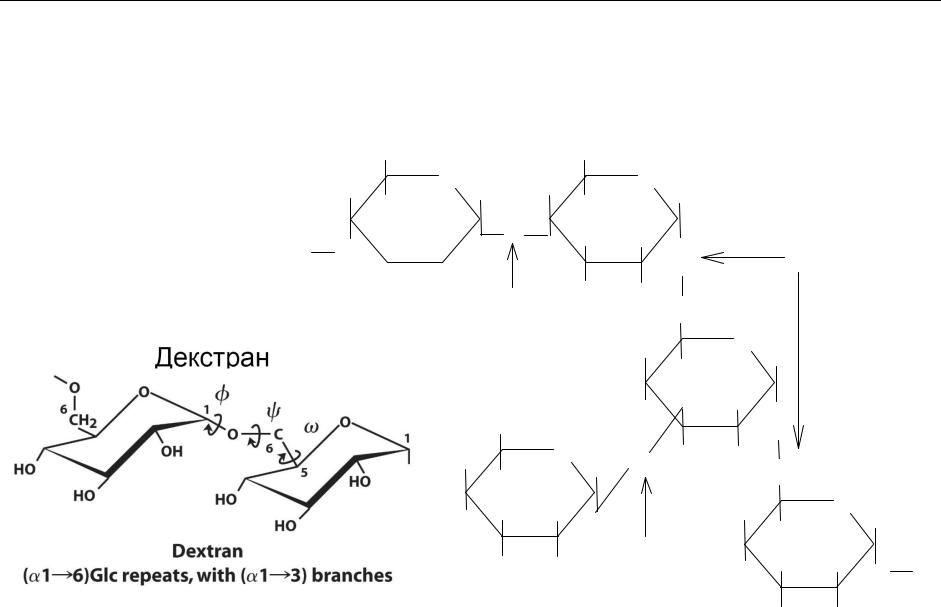
Декстраны — (С6Н10О5)n — полисахариды бактериального происхождения, построены из ,D-
глюкопиранозы. Их макромолекулы сильно разветвлены. Основным типом связи является (1 6), а в местах разветвлений — (1 4)-, (1 3)- и реже (1 2)-гликозидные связи.
300 тысяч остатков глюкозы с Мr до 500 кДа
CН2ОН
O
ОН
O 
 ОН
ОН
HO
|
|
CН2ОН |
|
|
|
|
|
|
|
O |
|
|
|
O |
|
ОН |
|
|
|
|
|
|
|
|
|
O |
|
|
|
4)- |
HO |
|
|
|
(1 |
|
|
|
CН2 |
|
|
гликозидная |
|
|
|
|||
|
|
|
O |
|||
связь |
|
|
|
|||
CН2OH |
НО |
|
|
|||
|
|
|
|
|||
|
|
O |
O |
|
HO |
|
ОН |
|
|
|
|
|
|
|
|
OH |
|
|
3)- |
HO |
|
|
(1 |
|
|||
|
|
|
гликозидная |
|
||
связь
(1 6)-гликозидны
O
CН2
O
ОН
O
OH
