
- •Биохимия межклеточного матрикса, коллагеновые белки, синтез, роль аскорбиновой кислоты. Неколлагеновые белки. Металлопротеиназы. Гликозаминогликаны.
- •Основные вопросы лекции:
- •Соединительная ткань составляет до 50% от массы тела человека.
- •Соединительная ткань
- •Функции клеток соединительной ткани:
- •Межклеточный (внеклеточный) матрикс
- •Структура и свойства коллагеновых белков
- •Типы коллагенов:
- •Коллаген – сложный внеклеточный белок. Синтезируют фибробласты, хондробласты, остеобласты,
- •Трансляция полипептидной цепи коллагена на рибосомах. Особенности первичной структуры.
- •Посттрансляционная внутриклеточная модификация коллагена включает процессы:
- •Гидроксилирование аминокислот. Гидроксипролин необходим для стабилизации тройной
- •Гидроксилизин необходим для стабилизации тройной спирали коллагена.
- •Роль аскорбиновой кислоты (витамин С).
- •Дефицит витамина С в рационе приводит
- •Гликозилирование остатков гидроксилизина
- •Образование тропоколлагена и фибриллогенез
- •Самосборка коллагеновых фибрилл фиксируется межмолекулярными связями (сшивками).
- •Дефицит ЛАО (ферментопатия) приводит к развитию наследственного заболевания (синдром Элерса - Данло V),
- •Необычные механические свойства коллагена связаны с первичной и пространственной структурами.
- •Ускоренный синтез коллагена происходит
- •Эластин
- •Эластин
- •При снижении образования десмозинов поперечные сшивки образуются в недостаточном количестве или не образуются
- •Эластин в косметологии
- •Катаболизм белков матрикса.
- •Активность ММП находится под постоянным контролем:
- •Катаболизм коллагена.
- •Катаболизм коллагена
- •Протеогликаны - класс сложных белков внеклеточного матрикса.
- •Протеогликаны - класс сложных белков внеклеточного матрикса.
- •Связь участка ГАГ с серином корового белка
- •Гликозаминогликаны относятся к гетерополисахаридам.
- •Гликозаминогликаны (ГАГ)
- •Гиалуроновая кислота несет большой отрицательный заряд, высоко гидрофильна, обладает вытянутой конформацией
- •Физико-химические свойства ГАГ
- •Катаболизм гликозаминогликанов
- •Распад ГАГ происходит в лизосомах.
- •Мукополисахаридозы
- •Катаболизм гиалуроновой кислоты ( ГК )
- •Применение гиалуронидазы в терапии
- •Применение ГАГ
- •Неколлагеновые белки (НКБ) – белки адгезии
- •Фибронектин
- •На молекуле фибронектина имеется центр связывания трансглутаминазы.
- •Ламинин - основной белок базальной мембраны.
- •Интегрины–трансмембранные белки, имеют α, β –димеры
- •Сиаловые кислоты встречаются в составе гликопротеидов и гликолипидов на наружной поверхности мембран клеток
- •Регуляция метаболизма соединительной ткани
- •Коллагенозы (коллагеновые болезни) -
- •Изменения метаболизма соединительной ткани в онтогенезе
- •Старение коллагена:
- •Возрастные изменения обусловлены нарушением метаболизма ткани:
- •Благодарю за внимание!

Биохимия межклеточного матрикса, коллагеновые белки, синтез, роль аскорбиновой кислоты. Неколлагеновые белки. Металлопротеиназы. Гликозаминогликаны.
Лекция для специальности 31.05.01 Лечебное дело подготовлена доцентом кафедры общей и биологической химии ТГМУ Артюковой О. А.
2016 –2017 учебный год

Основные вопросы лекции:
Биохимия соединительной ткани и межклеточного матрикса. Организация межклеточного матрикса.
Общие сведения о структуре коллагеновых белков.
Синтез коллагена. Этапы внутриклеточного синтеза: транскрипция, трансляция, посттрансляционная модификация, роль аскорбиновой кислоты, формирование коллагеновых фибрилл вне клетки.
Нарушения синтеза коллагеновых белков у человека.
Катаболизм белков межклеточного матрикса. Регуляция активности матриксных металлопротеиназ.
Неколлагеновые белки межклеточного матрикса. Эластин. Синтез и распад эластина. Изменения в структуре эластина при патологических процессах.
Протеогликаны и гликозаминогликаны. Протеогликаны базальных мембран.
Распад гликозаминогликанов. Мукополисахаридозы.
Неколлагеновые белки со специальными свойствами. Адгезивные белки.
Изменение соединительной ткани в онтогенезе и при заболеваниях.
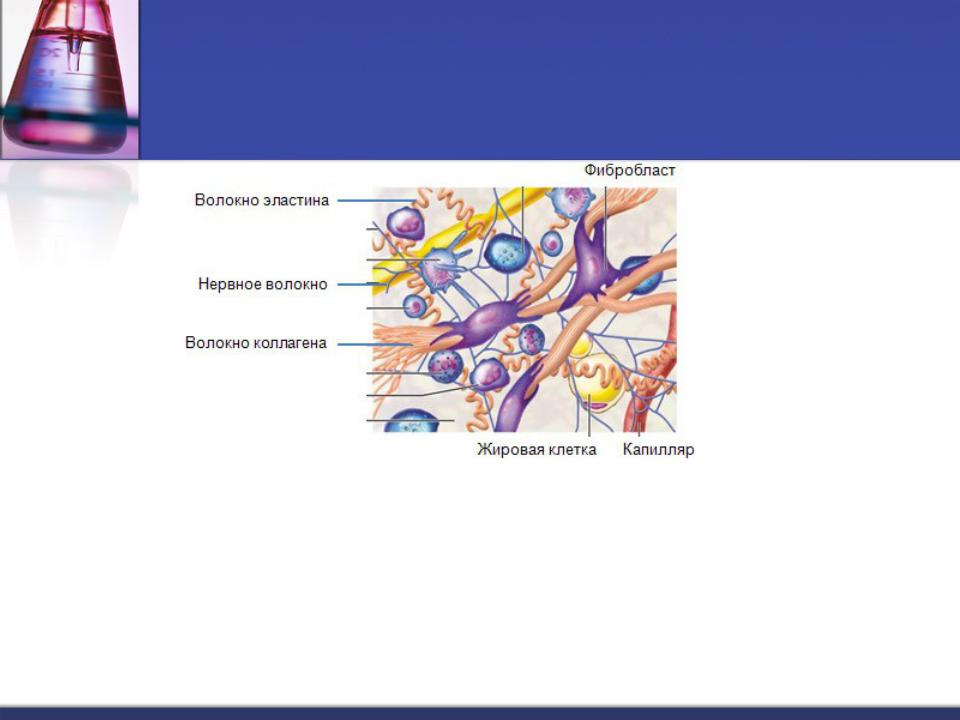
Соединительная ткань составляет до 50% от массы тела человека.
Функции соединительной ткани:
Механическая, опорная (хрящевая, костная ткани)
Трофическая (метаболическая)
Депонирование (подкожная жировая клетчатка)
Защитная (кожа, подвижность трущихся поверхностей суставов)
Репаративная (регенерация и замещение дефектов тканей)
Формирование структуры органов и тканей (базальная мембрана)

Соединительная ткань
Особенности
структуры
ткани
Клетки |
Внеклеточный |
|
(мало!) |
матрикс |
|
Фибробласты, |
(много!) |
|
макрофаги и др. |
||
|
Внеклеточный матрикс (ВКМ) составляет основу соединительной ткани, обеспечивает механическую поддержку клеток и транспорт химических веществ.
Клетки соединительной ткани образуют с веществами ВКМ межклеточные контакты, которые могут выполнять сигнальные функции и участвовать в локомоции клеток.

Функции клеток соединительной ткани:
|
Фибробласты |
синтез органических и |
|
Остеобласты |
неорганических |
|
|
компонентов ВКМ. |
|
Макрофаги |
синтез ферментов, |
|
Тучные клетки |
разрушающих компоненты ВКМ. |
ВКМ содержит молекулы, способные путём самосборки образовывать комплексы, при этом формируется высокоупорядоченная трёхмерная структура, определяющая функциональные свойства ткани.
Синтез компонентов ВКМ и их разрушение обеспечивают процессы обмена внеклеточных структур (метаболизм).
Межклеточный (внеклеточный) матрикс
Компоненты
матрикса
Белки |
Протеогликаны |
Неорганические |
|
вещества |
|||
|
|
Коллаген |
НКБ |
Коровый |
ГАГ |
Н2О, ГАП, |
Эластин |
(адгезивные) |
белок 5% |
95% |
Na, K |
Взависимости от соотношения компонентов матрикса, соединительная ткань может представлять собой:
вязкую жидкость (суставная жидкость) гель (стекловидное тело глаза) хрящ (упругость, эластичность) кость (жесткость)
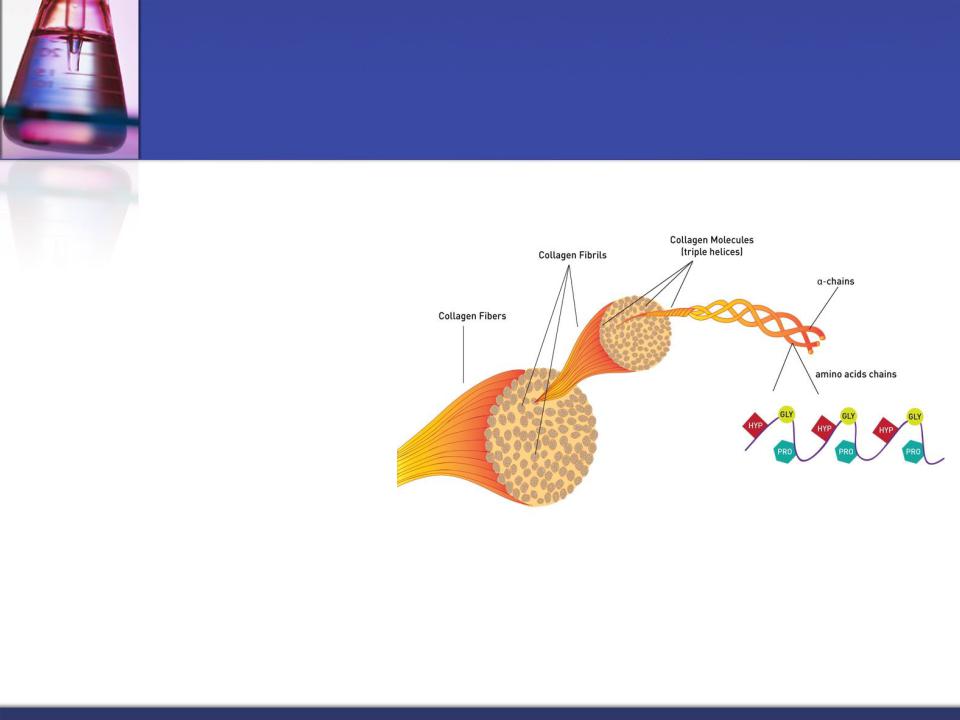
Структура и свойства коллагеновых белков
На долю коллагеновых белков приходится:
30% общего белка организма
6% массы тела
20% массы костной ткани.
В настоящее время описано 28 типов коллагена, которые кодируются > 40 генами.
90% всего коллагена высших организмов приходится на коллагены
I, II, III и IV типов.

Типы коллагенов:
Фибриллообразующие коллагены (I, II, III, V, XI тип) имеют форму фибрилл и построены из структурных единиц (тропоколлагены).
Коллагены, ассоциированные с фибриллами ( IX, XII, XIV тип)
не способны формировать фибриллы, но связаны с фибриллярными коллагенами I и II типов. Особенность - наличие в их структуре как глобулярных, так и фибриллярных доменов.
Нефибриллярные (сетевидные) типы коллагена ( IV, VIII и X тип) формируют сетевидные структуры. Наиболее распространен коллаген IV типа - основной структурный белок базальных мембран.
Коллагены, образующие микрофибриллы (VI тип) - короткоцепочечные белки, располагаются между фибриллами интерстициальных коллагенов, обеспечивают клеточную адгезию.
Коллаген – сложный внеклеточный белок. Синтезируют фибробласты, хондробласты, остеобласты,
одонтобласты, цементобласты, кератобласты и др.
Синтез коллагена
проходит в 8 этапов:5 внутриклеточных,
3
внеклеточных.
Синтез коллагена включает основные стадии:
-трансляция полипептидной цепи на рибосомах
-внутри – и внеклеточная модификация
-образование коллагеновых волокон

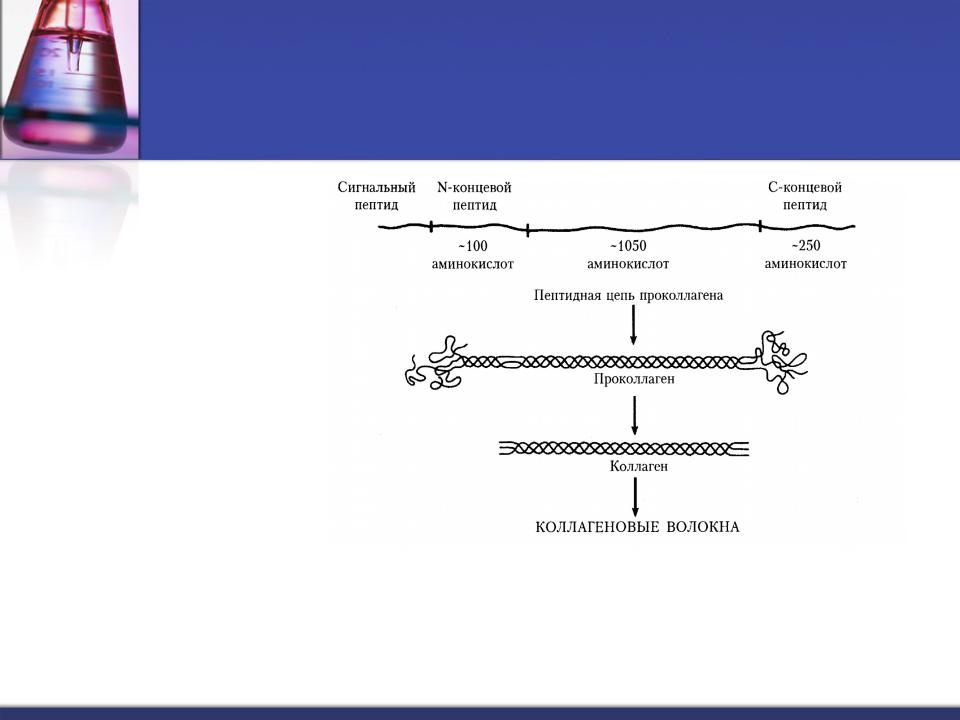
Трансляция полипептидной цепи коллагена на рибосомах. Особенности первичной структуры.
Имеет самую длинную полипептидную цепь – 1050 аминокислот.
Содержит заменимые аминокислоты (неполноценный белок)
Не содержит ТРИ, ЦИС, мало МЕТ,ТИР, ГИС
В составе много ПРО (гидроксипро), ЛИЗ (гидроксилиз)
Полипептидная цепь состоит из повторяющихся триплетов ( ГЛИ - X – Y )n
- Гли – Лей - Про - Гли- Про - Оксипро – Гли – Ала - Оксилиз-
Известно > 400 мутаций разных коллагенов, связанных с развитием патологии ткани (дисплазия соединительной ткани, несовершенный остеогенез и др.).
