3 КУРС / Разобранные билеты на экзамен по биологии микроорганизмов
.pdf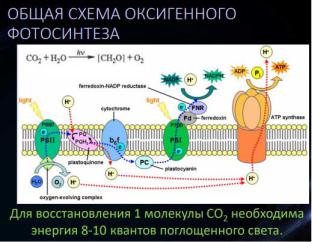
хлорофитов спаренные, у них отсутствуют фикобилисомы и фикобилипротеиды и имеется хлорофилл b.
Цианобактерии обладают полноценным фотосинтетическим аппаратом. Фотосинтетическая электронтранспортная цепь включает фотосистему (ФС) II, b6f- цитохромный комплекс и ФСI. Конечным акцептором электронов служит ферредоксин, донором электронов — вода, расщепляемая в системе окисления воды, аналогичной у высших растений. Светособирающие комплексы представлены особыми пигментами — фикобилинами, собранными в фикобилисомы. При отключении ФСII способны к использованию других, экзогенных доноров электронов: восстановленных соединений серы, органических соединений в рамках циклического переноса электронов с участием
ФСI.
29. Характеристика аноксигенных фототрофных бактерий.
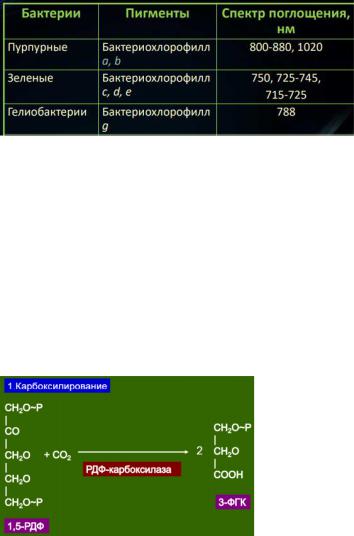
К аноксигенным фототрофным бактериям относят - пурпурные и зеленые бактерии(бактериохлорофилл), гелиобактерии (бактериородопсин-светочувствительный белок, осуществляет перенос протона через плазматическую мембрану с помощью кофактора –ретиналя. Светозависимый протонный насос откачивает ионы H+ из клетки. Освобождающаяся энергия ΔμH+ используется для синтеза АТФ.). Фотосинтез не сопровождается выделением кислорода, так как донорами водорода при ассимиляции углекислоты служит не вода, а другие вещества: сероводород, молекулярная сера, тиосульфат, сульфит, молекулярный водород, органические соединения.
Зеленые серные бактерии осуществляют нециклическое фотофосфорилирование (ФС 1). Синтезируется АТФ и восстановитель (НАД Н).
Но нужны экзогенные доноры электронов:
–органические вещества (сукцинат),
–неорганические соединения серы (H2S, сульфит, сера, тиосульфат и др.),
–молекулярный водород.
Из переносчиков электронов у них обнаружены цитохромы с и b, а также менахиноны. Синтез восстановительных эквивалентов осуществляется за счёт электронов окисленной серы, которые поступают в цикл при помощи фермента тиосульфатредуктазы, который окисляет тиосульфат и восстанавливает цитохром с.
Пурпурные бактерии осуществляют циклическое фотофосфорилирование (ФС 2, комплекс 3). Синтезируется АТФ, не нужен экзогенный донор электронов, но восстановитель не образуется.
30. Автотрофная ассимиляция соединений углерода бактериями: Восстановительный цикл Кальвина.
Цикл Кальвина, или восстановительный пентозофосфатный цикл. Он является основным путем фиксации CO2 у всех высших фотосинтезирующих организмов. Акцептор CO2 – активированная молекула пентозы (рибулозо-1,5-дифосфат). Три этапа:
1). Фиксация СО2 происходит в реакции, катализируемой ключевым ферментом рибулозодифосфаткарбоксилазой, при этом образуются две молекулы 3- ФосфоГлицериноваяКислота.
2). Восстановление фиксированного СО2. Молекулы 3-ФГК подвергаются превращениям, которые включают реакции, известные в гликолитическом пути, но идущие в обратном направлении:
3-ФГК + АТФ → 1,3-ФГК + АДФ
1,3-ФГК + НАД(Ф)-Н2 → 3-ФГА + НАД(Ф) + ФН
3)Регенерация акцептора СО2. 3-ФГА превращается во фруктозо-1,6-дифосфат под действием двух ферментов гликолиза. Однако чтобы функционировал этот механизм, необходимо постоянное воспроизведение молекул-акцепторов CO2. Остальные реакции цикла служат для регенерации рибулозо-1,5-дифосфата и катализируются большинством ферментов окислительного пентозофосфатного пути:
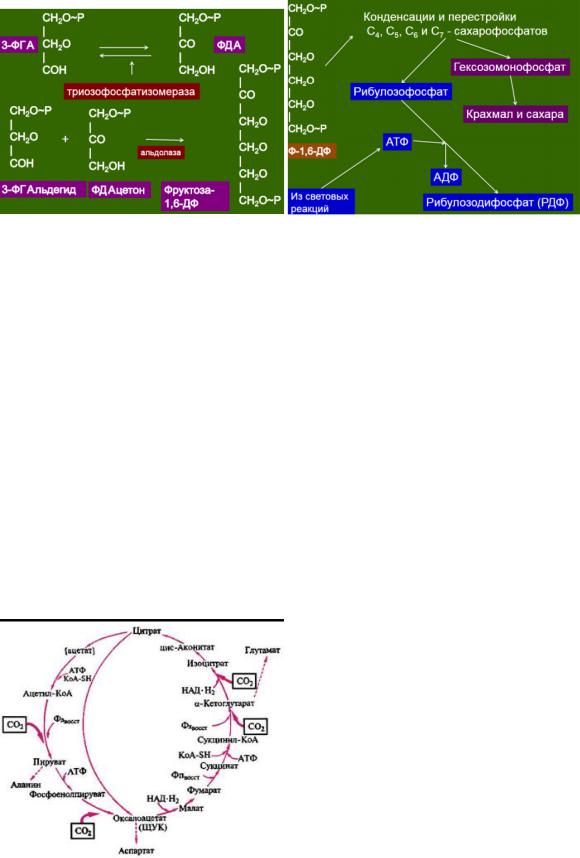
Фруктозо-6-фосфат + 2 ФГА + диоксиацетонфосфат → 2 ксилулозо-5-фосфат + рибозо-5- фосфат
Затем пентозофосфаты превращаются в рибулозо-5-фосфат, который фосфорилируется вторым ключевым ферментом цикла Кальвина фосфорибулокиназой, и таким образом регенерируется акцептор СО2.
Суммарное уравнение восстановительного пентозофосфатного цикла:
6СО2 + 18АТФ + 12НАД(Ф)-Н2 → С6Н12О6 + 18Фн + 18АДФ + 12НАД(Ф)+
Для синтеза 1 молекулы глюкозы из CO2 необходимо 6 оборотов цикла.
31. Автотрофная ассимиляция соединений углерода бактериями: Цикл Арнона.
Цикл Арнона, или восстановительный цикл трикарбоновых кислот. Был обнаружен у зеленых серобактерий. В его основе - карбоксилирование органических кислот( ацетилкоа, ФЕП, а-кетоглутарат). В цикле углекислота фиксируется в четырех ферментативных реакциях, две из которых идут при участии фотохимически восстановленного ферредоксина, а одна –путем образованного НАД-H2. В результате одного оборота из 4 молекул CO2, 10 [Н]+ с использованием энергии (3 молекулы АТФ) синтезируется молекула ЩУК – конечный продукт цикла.
32. Ассимиляция органических соединений азота бактериями: ассимиляция аммиака/аммония.
Нитрификация — микробиологический процесс окисления аммиака до азотистой кислоты
или её самой далее до азотной кислоты, что связано с получением энергии. Нитрификация проходит в две стадии, которые осуществляются разными микроорганизмами:
1. Nitrosomonas окисляет аммиак до нитрит-аниона по следующему механизму (аммиак → гидроксиламин → нитриты):
NH3 + O2 + НАДН2 → NH2OH + H2O + НАД+
NH2OH + H2O → HNO2 + 4H+ + 4e−
1/2O2 + 2H+ + 2e− → H2O
Фермент первой реакции - аммиакмонооксигеназа. Гидроксиламин ингибирует работу фермента. Следующую реакцию осуществляет гидроксиламиноксидоредуктаза, расположенная в периплазме. Окислителем в них служит цитохром c, с него электрон передаётся на убихинон и далее в дыхательную цепь, на цитохромоксидоредуктазу и, в конечном итоге, на кислород. При этом запасается энергия в виде трансмембранного протонного потенциала.Суммарно: 2NH3 + 3O2 → 2HNO2 + 2H2O + Q
2. Nitrobacter - окисление аниона азотистой кислоты до аниона азотной. Процесс протекает в одну реакцию:
NO2− + H2O → NO3− + 2H+ + 2e−
катализируемую нитрит: нитрат-оксидоредуктазой, локализованной в ЦПМ. Далее электроны передаются на цитохромы дыхательной цепи, в которой единственным пунктом транслокации протонов является цитохромоксидаза.
Образование НАД(Ф)·H для фиксации углекислого газа также происходит путём обратного переноса электронов.
33. Ассимиляция неорганических соединений азота бактериями: азотфиксация.
Фиксация азота из воздуха с участием нитрогеназного комплекса.
Нитрогеназа – двухкомпонентный ферментный комплекс, каждый компонент которого неактивен в отдельности (слайд 13.13). Молекулярные массы компонентов различны: у большого компонента – 150...270 кДа, малого – 50...70 кДа. Большой компонент – железо- молибден-протеин (молибдоферредоксин), малый – железо-протеин (азоферредоксин).
Восстановление N2 до NН3 с участием нитрогеназы происходит по суммарной реакции:
N2 + 6Fe2+ + 6H+ + 12АТФ → 2NH3 + 6Fe3+ + 12АДФ + 12Фн
Кислород репрессирует синтез нитрогеназы . Клубеньки, где происходит фиксация азота бактериями рода Rhizobium, ограничивают доступ молекулярного кислорода.
34. Ассимиляция неорганических соединений азота бактериями: ассимиляционная нитратредукция.
Большинство микроорганизмов ассимилирует минеральный азот в виде аммиака, который образуется в реакции:
Ассимиляционная нитратредукция с участием нитратредуктазы.
Микроорганизмы способны восстанавливать нитраты до аммиака – ассимиляционная нитратредукция. В этом случае нитрат вначале восстанавливается в нитрит с помощью фермента нитратредуктазы. Донором электронов у бактерий выступает НАД-Н2. Нитратредуктаза (М = 800 кДа) – тетрамер, состоящий из двух димеров. Это также молибденсодержащий фермент. Реакция восстановления нитратов в присутствии нитратредуктазы протекает в две стадии:
НАДФ·Н + Н++ NO3- → NO2- + НАДФ+ + Н2О
NO2-+ 8H + 6e- → NH4 - + 2H2O
Аммиак, образующийся различными путями в природе, включается в состав органических соединений, и прежде всего – аминокислот, благодаря трем главным реакциям: аминирования, амидирования и переаминирования.
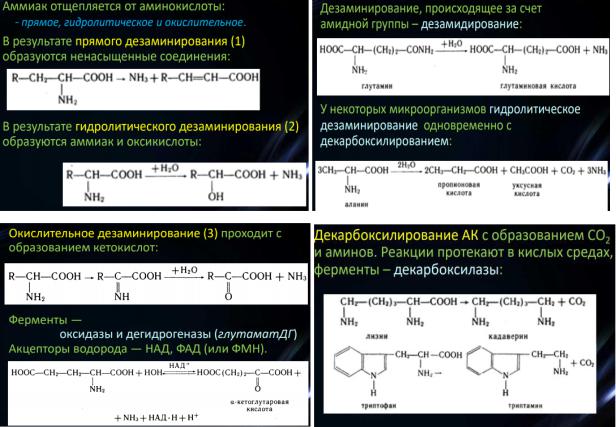
35. Катаболизм аминокислот.
Катаболизм начинается с отщепления аминогруппы: дезаминирование или переаминирование.

36. Пути биосинтеза аминокислот. Биосинтез белков.

В биосинтезе белка (трансляции) выделяют два основных этапа: синтез цепи из аминокислот, происходящий на рибосомах с участием молекул мРНК и тРНК, и посттрансляционные модификации полипептидной цепи.
У прокариот мРНК может считывается рибосомами в аминокислотную последовательность сразу после транскрипции. Траснляция начинается, когда рибосомная 30S-частица присоединяется к участку мРНК, содержащему инициирующий кодон AUG. Затем присоединяется 50 S частица и начинается процесс наращивания цепи белка.