
- •1. Элементарная ячейка кристаллической решетки и ее характеристики. Полиморфизм, анизотропия, их использование в технике.
- •2 Конструкционные стали нормальной прочности: углеродистые конструкционные стали обыкновенного качества и качественные стали. Состав, маркировка, упрочняющая обработка и применение.
- •2. Способы повышения упругих характеристик конструкционных материалов. Стали для пружин и рессор, их состав, марки, упрочняющая обработка.
- •1. Пластическая деформация и рекристаллизация металлов. Сдвигово-дислокационный механизм пластической деформации. Изменение структуры и свойств при холодной и горячей деформациях.
- •1. Диаграммы состояния двойных сплавов. Правило концентраций и отрезков. Использование диаграмм состояния для определения свойств сплавов и возможных видов их термической обработки.
- •1.Диаграмма Fe-Fe3c, ее фазовый и структурный анализ. Влияние углерода на структуру и свойства сталей.
- •1. Цели легирования конструкционных сталей. Влияние легирующих элементов на структуру сталей в отожженном и нормализованном состоянии.
- •2. Конструкционные материалы малой плотности: алюминиевые деформируемые сплавы, их состав, марки, термообработка, применение. Преимущества и недостатки алюминиевых сплавов по сравнению со сталями.
- •1. Фазовый и структурный анализ диаграммы Fe-FeзС. Использование полиморфизма железа при термической обработке сталей.
- •2. Конструкционные материалы малой плотности: пластмассы, их состав, применение. Преимущества и недостатки пластмасс как конструкционных материалов.
- •1. Формирование структуры литых сплавов. Влияние скорости охлаждения на степень переохлаждения и величину кристаллов. Модифицирование. Получение монокристаллов, аморфных сплавов.
- •2. Конструкционные материалы высокой удельной прочности: композиционные материалы (к.М.). Зависимость свойств к.М. От вида, количества, формы упрочнителей. Волокнистые и дисперсноупрочненные к.М.
- •1. Виды термической обработки: отжиг, закалка, отпуск, старение;их назначение. Связь диаграмм состояния двойных сплавов и возможных видов их термической обработки.
- •1. Химико-термическая обработка сталей. Цементация, азотирование, нитроцементация; режимы и цели проведения. Цементуемые стали, азотируемые стали.
- •1. Виды термической обработки сталей: отжиг, нормализация, закалка, отпуск. Цели и режимы их проведения. Свойств а отожженных, нормализованных и термически улучшенных сталей.
- •2. Преимущества и недостатки конструкционных сплавов на основе меди. Латуни, бронзы, их состав, марки, свойства, применение.
- •1. Закалка сталей. Оптимальная температура закалки углеродистых сталей. Влияние легирующих элементов на критическую скорость закалки. Внутренние напряжения в закаленных сталях.
- •2.Антифрикционные материалы, используемые в узлах скольжения. Факторы, влияющие на коэффициент трения и пути его уменьшения.
- •1. Распад переохлажденного аустенита. Формирование структуры при перлитном, мартенситном и промежуточном превращениях. Строение и свойства продуктов распада.
- •2. Сплавы для чувствительных элементов точных приборов. Fe-Ni-сплавы, бериллиевые бронзы, их состав, свойства, упрочняющая обработка, применение.
- •1. Превращения в закаленной стали при отпуске. Выбор вида отпуска (низкий, средний, высокий) в зависимости от назначения деталей и инструмента.
- •2. Материалы вакуумной техники. Влияние давления и температуры на фазовое состояние материала. Сравнительная оценка вакуумной стойкости металлических и неметаллических материалов.
- •2. Высокопрочные стали. Легированные стали, мартенситностареющие стали: их состав, марки, упрочняющая обработка, применение.
- •2. Легированные низкоуглеродистые и среднеуглеродистые конструкционные стали. Принцип легирования, упрочняющая обработка, марки, применение.
- •1. Формирование структуры литых сплавов. Влияние скорости охлаждения на степень переохлаждения и размер кристаллов. Модифицирование. Получение монокристаллов, аморфных сплавов.
- •2. Жаропрочные материалы. Изменение механических свойств металлов при нагреве. Механизм ползучести. Пути создания оптимальной структуры жаропрочных материалов.
- •1. Распад переохлажденного аустенита. Формирование структуры при перлитном, мартенситном и промежуточном превращениях. Строение и свойства продуктов распада.
- •2. Бериллий и сплавы на его основе. Механические и технологические свойства бериллия.
- •2. Коррозионно-стойкие стали устойчивы к электрохимической коррозии.
- •1. Теория и практика отпуска сталей. Влияние легирующих элементов на превращения закаленных сталей при нагреве. Структура и свойства отпущенных сталей.
- •2. Материалы, устойчивые против химической коррозии. Способы повышения жаростойкости металлов и сплавов
- •1. Закалка сталей. Выбор температур нагрева и охлаждающих сред при закалке. Влияние легирующих элементов на критическую скорость охлаждения, прокаливаемость и закаливаемость сталей.
- •2. Кристаллофизические методы очистки полупроводников, легирование полупроводников.
- •2. Вопрос не входит в билеты
- •1. Распад переохлажденного аустенита. Формирование структуры при перлитном, мартенситом и промежуточном превращениях. Строение и свойства продуктов распада.
- •1. Превращение в закаленной стали при отпуске. Влияние температур отпуска на свойства сталей. Выбор видов отпуска (низкий, средний, высокий) в зависимости от назначения деталей и инструмента.
- •2. Радиационностойкие материалы. Причины образования радиационных дефектов, Радиационная стойкость. Основные группы радиационных конструкционных материалов.
- •2. Вопрос не входит в билеты
Билет 1
1. Элементарная ячейка кристаллической решетки и ее характеристики. Полиморфизм, анизотропия, их использование в технике.
Кристаллическое тело характеризуется правильным расположением атомов в пространстве. У аморфных веществ расположение атомов случайно. Кристаллические вещества образуют кристаллическую решётку. 14 типов кристаллических решёток. Крист. решётка характеризуется элементарной ячейкой. Эл. ячейка – кристаллич. решётка наименьшего объёма, воспроизведение которой в пространстве множество раз создаёт пространственную крист. решётку. Атомы в пространстве располагаются упорядоченно, образуя кристаллическую решётку. Основные типы:
1. Простая кубическая решётка: в узлах кубика атомы касаются друг друга. Параметры: Период решётки (расстояние между атомами a =d), d – диаметр атома. 1/8·8 =1 атом на элемент, ячейку. Для химического соединения данный тип решётки.
2. Кубическая
объёмно-центрированная решётка
![]() характерна для тугоплавких металлов.a
=1,21·d.
1/8·8 +1 =2. Feα,
Ti,
W,
Nb.
характерна для тугоплавких металлов.a
=1,21·d.
1/8·8 +1 =2. Feα,
Ti,
W,
Nb.
3. Кубическая
гранецентрированная решётка
 .
1/8·8 +1/2·6 =4. Характерна для пластичных
металлов.Cu,
Feγ,
Au.
.
1/8·8 +1/2·6 =4. Характерна для пластичных
металлов.Cu,
Feγ,
Au.
3. Анизотропия кристалла и изотропия кристаллических тел.
Анизотропия – это различие свойств в разных направлениях в кристалле. В монокристалле – анизотропия. Поликристаллические вещества – где много кристаллов. В поликристаллическом теле – изотропия (одинаковые свойства по разным направлениям).
2. Конструкционные стали повышенной прочности: легированные стали. Принципы легирования, маркировка. Термическая обработка, свойства и применение легированных сталей в зависимости от содержания углерода.
Легированной называется сталь, содержащая в своем составе один или несколько специально введенных легирующих элементов в количестве, заметно изменяющем свойства стали.
Принципы маркировки стали:
Марка легированной стали – буквенно-цифровой код ее химического состава.Каждый элемент обозначается заглавной буквой русского алфавита:
а) по первой букве русского названия Н – Ni; В – W; Т – Ti; Х – Cr; М – Mo; Г – Mn; Д – Cu; Ю – Al; А – N; Б – Nb;
б) по первой букве латинского названия С – Si;
в) просто условное обозначение Ф – V;
Марка
легированной стали: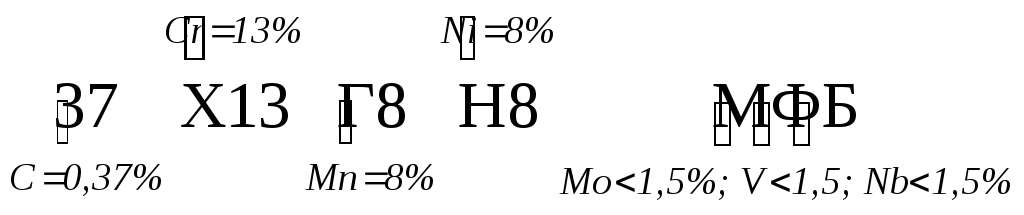
Если число соответствующее содержанию углерода двухзначное, то это содержание углерода в сотых долях процента, если в единицах, то это содержание углерода в десятых долях процента.
низколегированные

среднелегированные

высоколегированные

Влияние некоторых основных легирующих элементов на свойства сталей.
1. Никель. Никель образует твердые растворы внутри легированных сталей, повышается прочность стали, ее устойчивость к высоким температурам (никель – сильный аустенизатор).
2. Хром. Если содержание в стали хрома больше 12%, то сталь – нержавеющая (при условии растворения хрома в кристаллической решетке железа). Хром – сильно карбидообразующий элемент. Из-за образования карбидов коррозионная стойкость стали может уменьшаться. В стали 12Х18Н10Т предотвращено образование карбидов хрома на зернах.
3. Вольфрам. Вольфрам повышает твердость и прочность стали. Сильно карбидообразующий элемент. Карбиды вольфрама устойчивы и действуют при температуре выше температуры применения. Вольфрам используют для изготовления инструментальных сталей.
4. Ванадий. Ванадий повышает устойчивость к циклическим нагружениям и высоким температурам.
5. Марганец. Марганец способствует повышению твердости и прочности, обеспечивает высокую вязкость сталей.
6. Кремний. Кремний – ферритизатор – повышает устойчивость феррита при высоких температурах, то есть такая сталь обладает хорошими электро-магнитными свойствами (феррит – сильный ферромагнетик). Стали с высоким содержанием кремния используются для изготовления сердечников для электроприборов.
Билет 2
1 Фазы сплавов: твердые растворы и промежуточные фазы. Влияние состава на свойства твердых растворов. Промежуточные фазы постоянного и переменного составов, их строение и свойства (фазы внедрения, карбиды, нитриды, электронные соединения и т.д.).
1. Сплав – вещество, содержащее в своем составе два или более компонентов, по крайней мере один из которых – металл.
Получают их с помощью спекания или сплавлением. Компонент – вещество, образующее сплав.
Фаза – пространственно ограниченная и отличная от других часть системы, имеющая свою кристаллическую решётку и свои свойства. Гомогенные вещества имеют одну фазу, а гетерогенные – несколько фаз.
Структура – строение металла, в котором можно различать отдельные фазы, их форму, размеры и взаимное расположение. Структура влияет на свойства.
Равновесное состояние – когда в сплаве все фазы, присущие этой системе оформлены. Это состояние обеспечивается при медленном охлаждении, можно различать размеры и формы фаз.
Неравновесное состояние – процесс образования и обособления фаз не закончился, образуется при быстром охлаждении.
Компонент – химическое вещество, входящее в состав сплава.
В дальнейшем будем рассматривать двойные сплавы.
Различные типы кристаллических сплавов.
1. Твердые растворы – кристаллы, у которых один из компонентов образует собственную кристаллическую решетку, а второй присутствует в виде отдельных атомов, то есть собственной кристаллической решетки не имеет. Первый компонент называют растворителем, а второй – растворенным компонентом.
Выделяют твердые растворы внедрения и твердые растворы замещения.
В твердых растворах внедрения – атомы растворенного вещества находятся в межатомных промежутках растворителя.

Особенности:
растворенные вещества должны иметь малый атомный радиус (обычно это неметалл);
ограниченная растворимость;
В твердых растворах замещения – атомы растворенного вещества замещают атомы растворителя в узлах кристаллической решетки.

Особенности
растворенное вещество такого же типа, как и растворитель (атомы близки по размеру);
часто имеют неограниченную растворимость;
