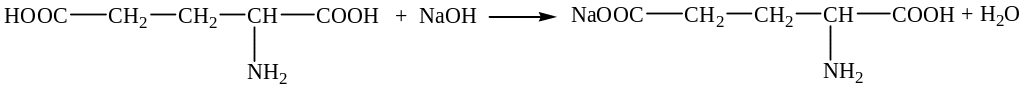- •Лабораторно-практическое занятие № 2 Фармацевтический анализ лекарственных средств группы аминокислот алифатического ряда
- •Кислота глутаминовая (Acidum glutaminicum)
- •Метионин (Methioninum)
- •Ацетилцистеин (Acetylcysteinum)
- •Пеницилламин (Penicillaminum)
- •Пирацетам (Piracetamum, Pyracetamum)
- •Натрия кальция эдетат (Sodium calcium edetate)
- •Аминокапроновая кислота (Aminocaproic acid)
- •Мелфалан (Melphalan)
- •Каптоприл (Captoprilum)
- •Эналаприла малеат (Enalapril maleate)
- •1. Семинар - 90 мин
- •2. Контрольный тест – 15 мин
- •3. Лабораторная работа – 45 мин Фармацевтический анализ лекарственных средств группы аминокислот алифатического ряда
- •2.2. Подлинность. Определение удельного вращения.
- •4. Защита лабораторной работы – 30 мин.
Лабораторно-практическое занятие № 2 Фармацевтический анализ лекарственных средств группы аминокислот алифатического ряда
Цель: Освоить методы контроля качества лекарственных средств группы аминокислот алифатического ряда и их производных по показателям «описание», «подлинность», «чистота», «содержание действующего вещества».
Структура занятия:
1. Семинар - 90 мин
2. Контрольный тест - 15 мин
3. Лабораторная работа – 45 мин
4. Защита лабораторной работы – 30 мин.
Аминокислоты представляют собой производные карбоновых кислот, содержащие в молекуле одну или несколько аминогрупп. a - Аминокислоты являются структурными элементами белков и широко распространены в природе.
Аминокислоты являются амфотерными соединениями и способны образовывать внутренние соли в виде биполярного иона (цвиттер-иона):
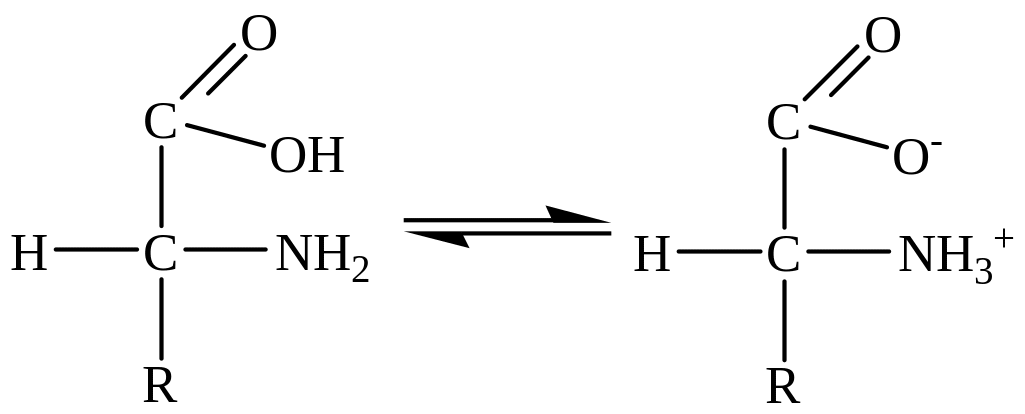
Их оснóвные свойства обусловлены присутствием NН2-группы, а кислотные – СООН-группы:
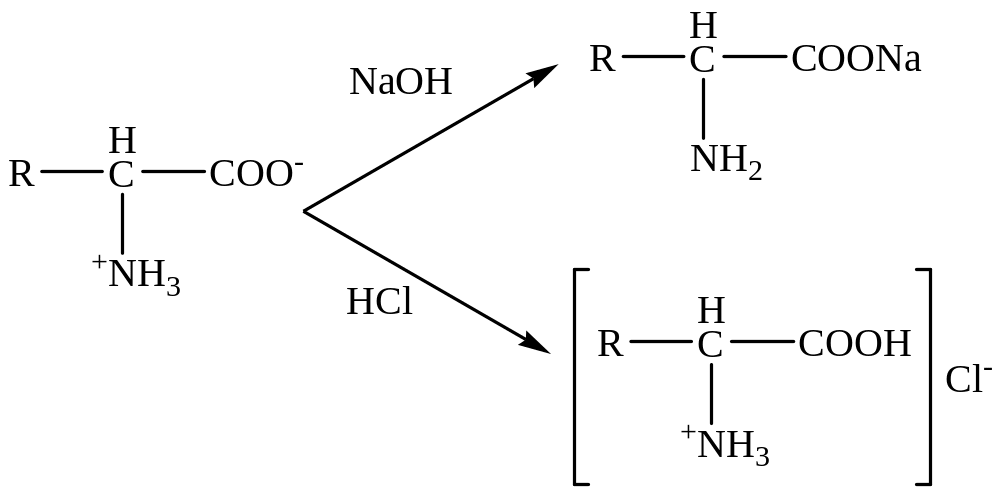
Общегрупповыми реакциями являются:
1) Реакция образования комплексной соли меди(II):
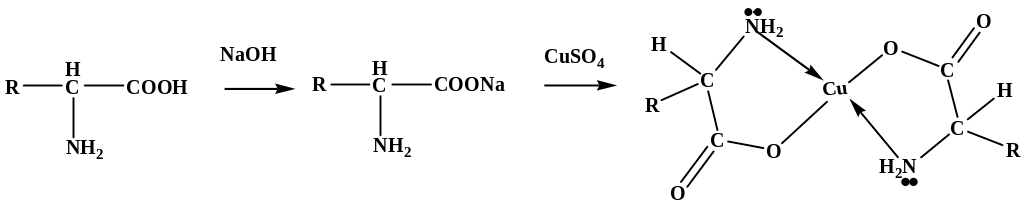
темно-синий
Это координационное соединение мало растворимо в воде, что позволяет выделять аминокислоты из смеси с другими веществами.
2) Нингидриновая реакция является одной из старейших (1910), но широко применяемых и до сих пор, цветных реакций на a-аминокислоты (Н.А.Тюкавкина, 2008). Тем не менее природа всех образующихся окрашенных продуктов до сих пор окончательно не установлена. Упрощённо схема реакции может быть представлена следующим образом:
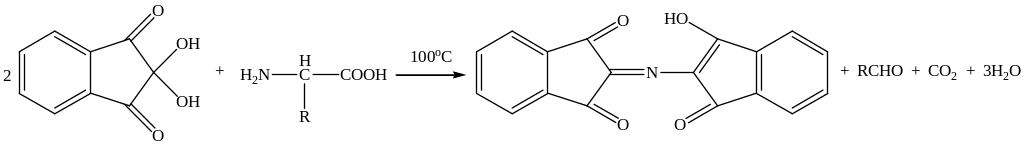
Продукт нингидриновой реакции имеет сине-фиолетовый цвет, что используется для визуального обнаружения аминокислот на хроматограммах (на бумаге, в тонком слое сорбента), а также спектрофотометрического определения на аминокислотных анализаторах (продукт поглощает свет в области 550-570 нм). Эта реакция неспецифична, так как окрашенные продукты с нингидрином дают b-аминокислоты, аммиак, первичные и вторичные амины, мочевина, белки и ряд других соединений, содержащих аминогруппу.
Программа по дисциплине «Фармацевтическая химия» включает следующие ЛС: кислота глутаминовая, , цистеин, ацетилцистеин, метионин, пеницилламин; натрия кальция эдетат (кальций-динатриевая соль этилендиаминтетрауксусной кислоты, тетацин-кальций); пирацетам (Ноотропил) как аналог гамма-аминомасляной кислоты; кислота g-аминомасляная (Аминалон); производные пролина: каптоприл, эналаприл; кислота аминокапроновая; мелфалан – производное фенилаланина.
Кислота глутаминовая (Acidum glutaminicum)
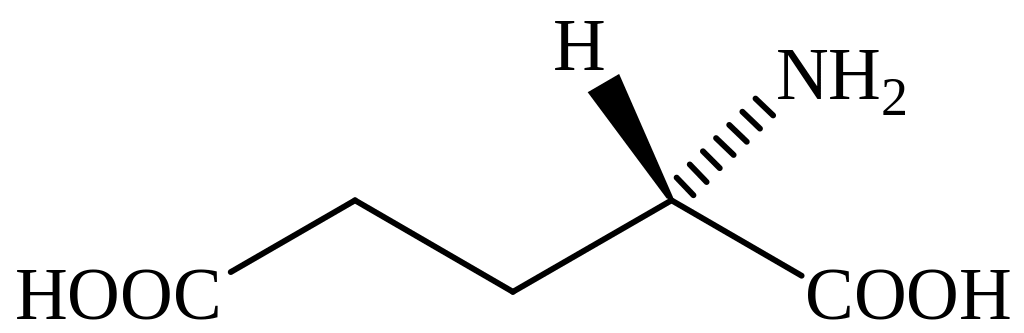
(S)-2-аминопентан-1,5-диовая кислота
С5Н9NО4 Мr 147,1
Глутаминовая кислота относится к фармакологической группе психостимуляторы и ноотропы. Применяется при лечении заболеваний центральной нервной системы: эпилепсии, психозов, реактивных состояний, протекающих с явлениями истощения, депрессии.
Описание. Глутаминовая кислота представляет собой белый кристаллический порошок, легко растворимый в горячей воде, мало растворимый в холодной воде, практически нерастворимый в уксусной кислоте, ацетоне и спирте.
Определение подлинности проводят физическими, физико-химическими и химическими методами:
Методом
поляриметрии определяют удельное
вращение 10%
раствора глутаминовой кислоты в
разведенной HCl: [α]![]() от +30,5 до +32,5о.
от +30,5 до +32,5о.
ИК-спектр субстанции, полученный методом прессования с KBr, по интенсивностям и частотам полос должен быть идентичен спектру стандартного образца кислоты глутаминовой.
Метод ТСХ: пятно на хроматограмме, полученное для субстанции, должно быть идентично по положению, цвету и размеру пятну, полученному для стандартного образца глутаминовой кислоты. Для проявления пятен хроматограммы опрыскивают раствором нингидрина.
Один из методов определения подлинности кислоты глутаминовой заключается в следующем: к 2 мл 10% раствора глутаминовой кислоты в 1 моль/л HCl добавляют 0,1 мл фенолфталеина (раствор остается бесцветным). При добавлении 3,0 мл того же раствора глутаминовой кислоты к 3,5 мл раствора 1 моль/л NaOH в присутствии фенолфталеина появляется красное окрашивание. К нему добавляют смесь, состоящую из 3 мл раствора формальдегида и 3 мл дистиллированной воды. Красная окраска постепенно переходит в розовую, а затем совсем исчезает.
Наблюдаемые явления объясняются следующим образом.
Поскольку аминокислота – амфотерное соединение, добавление щелочи к ее раствору не приводит к полной нейтрализации раствора (нейтрализуется только одна из двух карбоксильных групп):
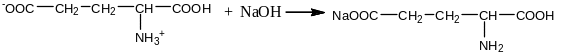
Окраска раствора остается красной (щелочь не полностью нейтрализована).
При добавлении раствора формальдегида протекает реакция Серенсена:
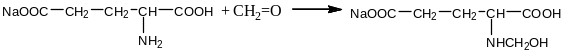
При блокировании аминогруппы глутаминовой кислоты увеличиваются ее кислотные свойства. Это приводит к полной нейтрализации щелочи за счет протекания реакции со второй карбоксильной группой:
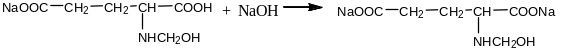
При этом окраска раствора исчезает полностью.
Оценка чистоты. Раствор кислоты глутаминовой (10%) в 1 моль/л растворе HCl должен быть прозрачным и бесцветным.
Родственные примеси, дающие положительную нингидриновую реакцию определяют методом ТСХ.
Допустимыми примесями являются: хлориды, сульфаты, ионы аммония, железа, тяжелые металлы. Кроме того, определяют потерю в массе при высушивании и сульфатную золу.
Количественное определение проводят методом нейтрализации.
Глутаминовую кислоту титруют 0,1 моль/л раствором гидроксида натрия. Индикатор - бромтимоловый синий. В точке эквивалентности, соответствующей моменту нейтрализации одной карбоксильной группы, наблюдается переход окраски из желтой в голубую.
1 мл 0,1 моль/л раствора NaOH соответствует 14,71 мг С5Н9NО4.