
- •Практикум по механике и молекулярной физике
- •Содержание
- •10. Определение модуля сдвига из крутильных колебаний……….………..62
- •11. Определение коэффициента вязкости жидкости по методу Стокса……66
- •1.1. Правила работы в лаборатории, оформление результатов работы
- •Правила работы в лаборатории
- •Оформление отчетов
- •Графики
- •1.2. Обработка результатов физического эксперимента
- •Вычисление погрешностей прямых измерений
- •Погрешности косвенных измерений
- •1.3. Изучение измерительных приборов Нониусы
- •Ш тангенциркуль
- •Микрометр
- •1.4. Определение плотности твердых тел, имеющих правильную геометрическую форму
- •2. Гармонические колебания
- •Математический маятник
- •Физический маятник
- •Выполнение работы
- •Упражнение 2. Определение ускорения свободного падения при помощи оборотного маятника.
- •Работа n 2-2
- •Контрольные вопросы
- •3. Затухающие колебания
- •Работа № 3-1 определение логарифмического декремента затухания и коэффициента затухания крутильных колебаний
- •Описание прибора
- •Выполнение работы
- •Определение логарифмического декремента затухания и коэффициента затухания колебаний математического маятника
- •Контрольные вопросы.
- •Работа № 4 изучение законов динамики поступательного движения с помощью машины атвуда
- •К раткая теория
- •Описание установки и метода измерений
- •Выполнение работы
- •Контрольные вопросы
- •5. Кинематика и динамика вращательного движения
- •2. Момент силы и момент инерции
- •Работа № 5-1 определение моментов инерции твердых тел при помощи крутильных колебаний
- •Описание установки Общий вид крутильного маятника показан на рис. 1.Крутильный
- •Описание метода определения моментов инерции твердых тел.
- •Тогда период колебаний т будет равен: . (5)
- •Очевидно, что период колебания рамки с исследуемым телом
- •Выполнение работы
- •Контрольные вопросы
- •Работа № 5-2 определение моментов инерции твердых тел с помощью маятника максвелла
- •Описание установки и метода измерений
- •Выполнение работы
- •Контрольные вопросы
- •Работа № 5-3 Определение момента инерции тел с помощью трифилярного подвеса
- •О писание установки и метода определения момента инерции тел
- •Выполнение работы
- •Определение момента инерции j ненагруженной платформы
- •Определение момента инерции твердого тела
- •Изучение зависимости момента инерции системы (платформа плюс тело) от расположения тела на платформе
- •Контрольные вопросы
- •Работа № 5-4 исследование вращательного движения твердых тел с помощью маятника обербека.
- •Выполнение работы.
- •Выполнение работы.
- •Описание установки
- •Выполнение рабаты
- •Контрольные вопросы
- •Работа № 8
- •Краткая теория
- •Описание установки
- •Выполнение работы
- •Контрольные вопросы
- •Работа № 9 определение модуля юнга методом прогиба
- •Краткая теория
- •Описание установки
- •Выполнение работы
- •Контрольные вопросы
- •Работа № 10 определение модуля сдвига из крутильных колебаний
- •Краткая теория
- •Описание установки и вывод расчетной формулы
- •Выполнение работы
- •Краткая теория
- •Выполнение работы
- •Контрольные вопросы
- •Работа № 12 определение отношения удельных теплоемкостей газов методом клемана-дезорма
- •Краткая теория
- •Описание и теория метода
- •Выполнение работы
- •Контрольные вопросы
- •Работа № 13 определение скорости звука в воздухе и отношение удельных теплоемкостей ср/сv для воздуха методом стоячих звуковых волн
- •Подставляя (15) в (13), находим, что (16)
- •Описание установки
- •Выполнение работы
- •Контрольные вопросы
- •Работа №14 определение коэффициента поверхностного натяженияжидкости методом компенсации дополнительного давления
- •Краткая теория
- •Описание установки и вывод расчетной формулы
- •Выполнение работы Задание 1. Измерение диаметра капилляра
- •Задание 2. Определение коэффициента поверхностного натяжения жидкости
Описание и теория метода
Предлагаемый метод определения основан на применении уравнений адиабатического и изохорического процессов.
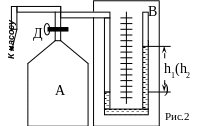 Установка
состоит из стеклянного баллона А,
соединенного с манометром В и насосом
(рис.2). Посредством крана Д баллон может
быть соединен с атмосферой, и будем
считать, что первоначально в нем было
атмосферное давление. Если с помощью
насоса накачать в баллон некоторое
количество воздуха и закрыть кран, то
давление в баллоне повысится; но если
это повышение было произведено достаточно
быстро, то манометрический столбик не
сразу займет окончательное положение,
так как сжатие воздуха было адиабатическим
и, следовательно, температура его
повысится. Окончательная разность
уровней в манометре h
установится только тогда, когда
температура воздуха внутри баллона
сравняется, благодаря теплопроводности
стенок, с температурой окружающего
воздуха.
Установка
состоит из стеклянного баллона А,
соединенного с манометром В и насосом
(рис.2). Посредством крана Д баллон может
быть соединен с атмосферой, и будем
считать, что первоначально в нем было
атмосферное давление. Если с помощью
насоса накачать в баллон некоторое
количество воздуха и закрыть кран, то
давление в баллоне повысится; но если
это повышение было произведено достаточно
быстро, то манометрический столбик не
сразу займет окончательное положение,
так как сжатие воздуха было адиабатическим
и, следовательно, температура его
повысится. Окончательная разность
уровней в манометре h
установится только тогда, когда
температура воздуха внутри баллона
сравняется, благодаря теплопроводности
стенок, с температурой окружающего
воздуха.
Обозначим через
Т1
термодинамическую температуру окружающего
воздуха и через р1
- давление газа внутри сосуда,
соответствующее показанию манометра
h1.
Очевидно, давление, установившееся в
баллоне, будет равно
![]() (15)
(15)
где р0 - атмосферное давление (конечно, при этом р0 и h1 должны быть выражены в одинаковых единицах). Эти два параметра Т1 и р1 характеризуют состояние газа, которое мы назовем первым состоянием газа.
Если теперь быстро открыть кран, то воздух в баллоне будет расширяться адиабатически, пока давление его не сделается равным р0; при этом он охладится до температуры Т2. Это будет второе состояние газа: Т2 и р0.
Если сразу после
открывания снова закрыть кран, то
давление внутри баллона начнет возрастать
вследствие того, что охладившийся при
расширении воздух в баллоне станет
снова нагреваться. Возрастание давления
прекратится, когда температура воздуха
в баллоне сравняется с внешней температурой
Т1.
Обозначим давление воздуха в баллоне
в этот момент через р2
и соответствующее показание манометра
- через h2.
Это будет третье состояние газа: Т1
и р2.
Ясно, что
![]() (16) Так как переход от второго состояния
(после закрытия крана) к третьему
произошел без изменения объема, то можно
применить здесь закон Гей-Люссака:
(16) Так как переход от второго состояния
(после закрытия крана) к третьему
произошел без изменения объема, то можно
применить здесь закон Гей-Люссака:
![]() (17)
(17)
К
переходу из первого состояния во второе
(процесс адиабатического расширения)
применяем уравнение Пуассона в форме:
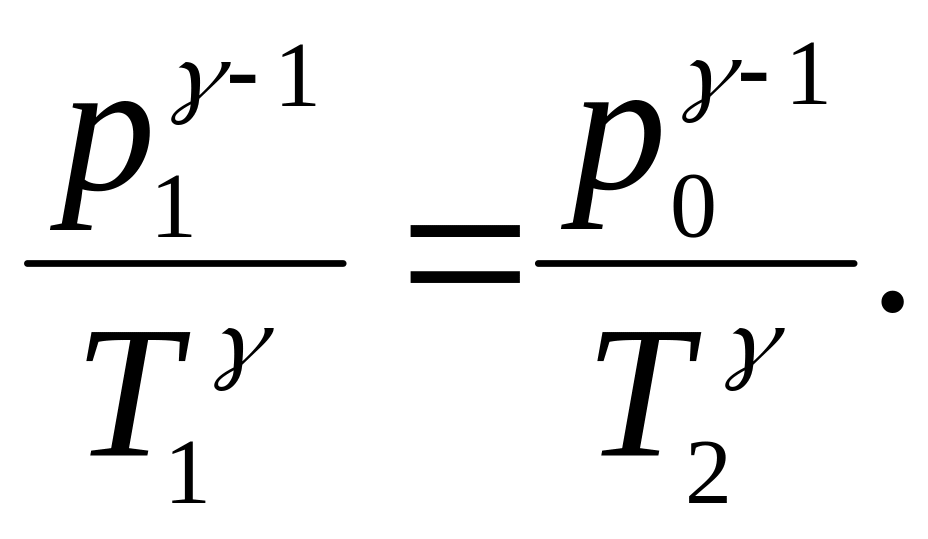 (18)
(18)
Эта
форма уравнения Пуассона может быть
легко получена из обычной (13)
![]() если
воспользоваться для этой цели уравнением
состояния газа
если
воспользоваться для этой цели уравнением
состояния газа
![]() Возводя последнее уравнение в степень
и разделив его почленно на уравнение
Пуассона, получим:
Возводя последнее уравнение в степень
и разделив его почленно на уравнение
Пуассона, получим:
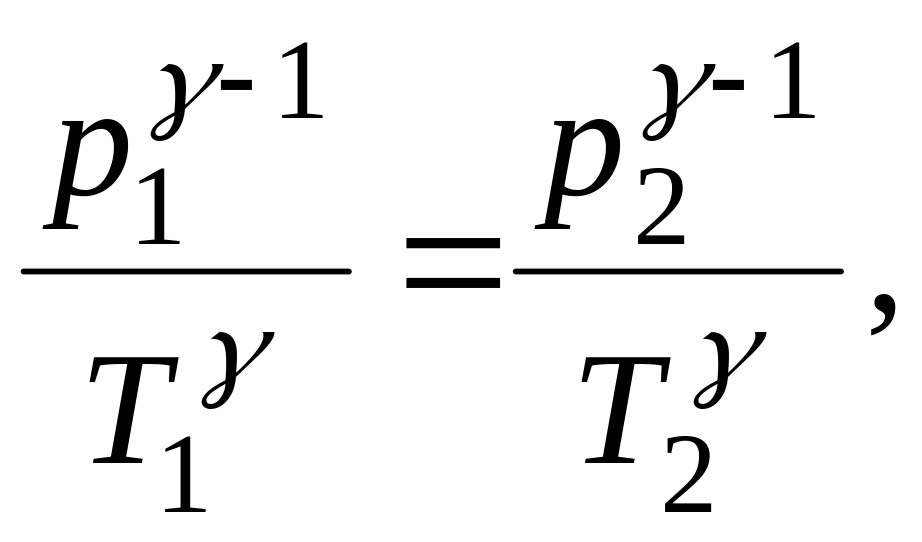 т.е.
уравнение, аналогичное (18).
т.е.
уравнение, аналогичное (18).
Подставляя в уравнение (18) значение р1 из (15) и переставляя члены, получаем:

Разлагая оба двучлена по биному Ньютона и ограничиваясь членами первого порядка малости, получаем:
![]() откуда
откуда
![]()
Но
выражение, стоящее в левой части этого
уравнения, есть не что иное, как h2;
действительно, подставив в уравнение
( 17) значение р1
из уравнения (16) и разрешив его относительно
h2,
получим:
![]()
Следовательно,
можно записать:
![]() откуда
окончательно находим:
откуда
окончательно находим:
![]() (19)
(19)
