
- •Часть II
- •1. Введение
- •1.1. Многообразие углеводородов
- •1.2. Классификация углеводородов
- •2.1. Гомологический ряд алканов
- •2.2. Строение алканов
- •2.3. Изомерия алканов
- •2.3.1. Структурная изомерия алканов
- •2.3.2. Поворотная изомерия алканов
- •2.3.3. Зеркальная (оптическая) изомерия
- •2.4. Номенклатура
- •2.4.1. Радикалы в ряду алканов
- •2.4.2. Правила построения названий алканов по систематической международной номенклатуре июпак
- •2.4.3. Назовем соединение по номенклатуре июпак
- •2.5. Химические свойства алканов
- •2.5.1. Крекинг алканов
- •2.5.2. Изомеризация алканов
- •2.5.3. Дегидрирование алканов
- •2.5.4. Реакции окисления алканов
- •2.5.5. Реакции замещения
- •2.6. Галогеналканы
- •2.7. Получение алканов
- •2.8. Применение алканов
- •3.1. Изомерия циклоалканов
- •3.2. Свойства циклоалканов
- •3.3. Получение циклоалканов
- •I. Br2, h; II. Br2 (вода); III. HCl; IV. KMnO4 (водн. Р-р).
- •6. Какие соединения образуются при действии металлического натрия на следующие вещества:
- •4. Алкены
- •Vrml-модель (2 камеры, 109300 байт).
- •Vrml-модель (37448 байт)
- •4.2. Номенклатура алкенов
- •2 Атома с этан этен; 3 атома с пропан пропен и т.Д.
- •4.3. Изомерия алкенов
- •4.3.1. Структурная изомерия алкенов
- •4.3.2. Пространственная изомерия алкенов
- •Vrml-модель
- •4.4. Свойства алкенов
- •4.4.1 Реакции присоединения к алкенам
- •4.4.1.1. Гидрирование (присоединение водорода)
- •4.4.1.2. Галогенирование (присоединение галогенов)
- •4.4.1.3. Гидрогалогенирование (присоединение галогеноводородов)
- •4.4.1.5. Полимеризация алкенов
- •4.4.2. Реакции окисления алкенов
- •4.4.3. Изомеризация алкенов
- •4.5. Получение алкенов
- •4.6. Применение алкенов
- •4.7. Контрольные вопросы
- •1. Какие модели соответствуют молекулам алкенов?
- •Тройная связь в ацетилене
- •6.2. Номенклатура алкинов
- •6.3. Изомерия алкинов
- •6.4. Свойства алкинов
- •6.4.2. Образование солей
- •6.4.3. Окисление алкинов
- •6.5. Получение алкинов
- •7.1. Строение бензола
- •Cтроение бензола
- •7.2. Гомологи бензола. Номенклатура и изомерия
- •7.3. Свойства аренов
- •7.3.1. Реакции замещения в бензольном кольце
- •1. Галогенирование
- •2. Нитрование
- •7.3.2. Замещение в алкилбензолах
- •7.3.3. Реакции присоединения к аренам
- •7.3.4. Реакции окисления аренов
- •7.4. Получение ароматических углеводородов
- •7.5. Применение ароматических углеводородов
- •9. Заключение. Генетическая связь между углеводородами
- •4.5. Получение алкенов
1.1. Многообразие углеводородов
В силу особенностей строения и свойств углерода (часть I, раздел 1.1) его соединения с водородом весьма многочисленны и разнообразны. Это обусловлено рядом структурных факторов:
атомы углерода способны соединяться между собой в цепи различного строения:
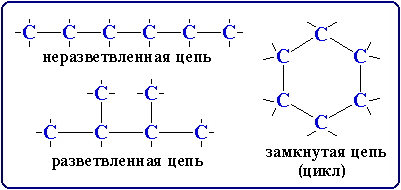 см.
также рис.1.1.2.
(52573 байт)
см.
также рис.1.1.2.
(52573 байт)
даже при одинаковом количестве атомов углерода в молекулах углеводороды могут отличаться числом атомов водорода, например: C6H14, C6H12, C6H10, C6H8, C6H6; или другой пример: молекулы с 4-мя атомами углерода могут содержать от 10-ти до 2-х атомов водорода:
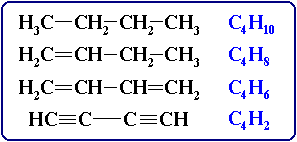
одному и тому же элементному составу молекул (одной молекулярной формуле) может соответствовать несколько различных веществ – изомеров. Например:
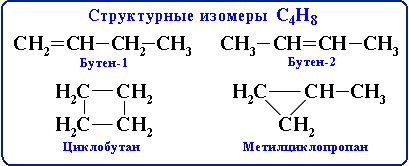
Многочисленность и разнообразие углеводородов требуют их классификации.
 Рис.1.1.2.
Многообразие углеродных цепей
Рис.1.1.2.
Многообразие углеродных цепей
1.2. Классификация углеводородов
Классификацию углеводородов проводят по следующим структурным признакам, определяющим свойства этих соединений:
строение углеродной цепи (углеродного скелета);
наличие в цепи кратных связей С=С и С
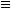 C
(степень насыщенности).
C
(степень насыщенности).
1. В зависимости от строения углеродной цепи углеводороды подразделяют на две группы:
ациклические или алифатические,т.е. "жирные" (от греческого слова "алейфар" – "жир", т.к. впервые структуры с длинными углеродными цепями были обнаружены в составе жиров);
циклические.
Открытая (незамкнутая) цепь алифатических углеводородов может быть неразветвленной или разветвленной. Углеводороды с неразветвленной углеродной цепью называют нормальными (н-) углеводородами.
Среди циклических углеводородов выделяют:
алициклические (т.е. алифатические циклические);
ароматические (арены).
В этом случае классификационным признаком служит строение цикла.
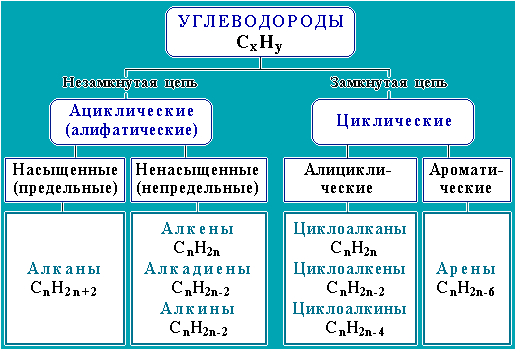
К ароматическим углеводородам относят соединения, содержащие один или несколько циклов С6Н6 (структура бензола).
2. По степени насыщенности различают:
насыщенные (предельные) углеводороды (алканы и циклоалканы), в которых имеются только простые связи С-С и отсутствуют кратные связи;
ненасыщенные (непредельные), содержащие наряду с одинарными связями С-С двойные и/или тройные связи (алкены, алкадиены, алкины, циклоалкены, циклоалкины).
Следует заметить, что хотя по составу бензол С6Н6 формально соответствует ненасыщенным циклическим углеводородам (его молекулу часто изображают как шестичленный цикл с тремя двойными связями), по свойствам это соединение
резко отличается от ненасыщенных веществ из-за делокализации кратных связей (часть I, раздел 4.10). Поэтому соединения ряда бензола относят к самостоятельной группе ароматических углеводородов (аренов). 2.АЛКАНЫ (предельные углеводороды, парафины)
Алканы – алифатические (ациклические) предельные углеводороды, в которых атомы углерода связаны между собой простыми (одинарными) связями в неразветвленные или разветвленные цепи.
Алканы – название предельных углеводородов по международной номенклатуре. Парафины– исторически сложившееся название, отражающее свойства этих соединений (от лат. parrum affinis – имеющий мало сродства, малоактивный). Предельными, или насыщенными, эти углеводороды называют в связи с полным насыщением углеродной цепи атомами водорода.
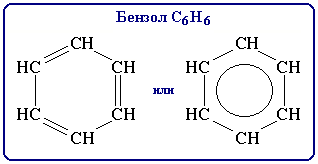
Простейшие представители алканов:
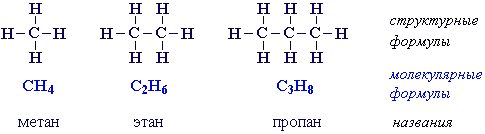
Модели молекул:
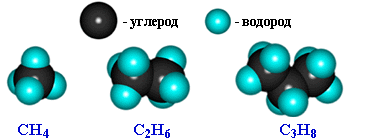
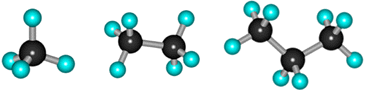
При сравнении этих соединений видно, что они отличаются друг от друга на группу -СН2- (метилен). Добавляя к пропану еще одну группу -СН2-, получим бутан С4Н10, затем алканы С5Н12, С6Н14 и т.д.
Теперь можно вывести общую формулу алканов. Число атомов углерода в ряду алканов примем за n, тогда число атомов водорода составит величину 2n+2. Следовательно, состав алканов соответствует общей формуле CnH2n+2. Поэтому часто используется такое определение:
Алканы - углеводороды, состав которых выражается общей формулой CnH2n+2, где n – число атомов углерода.
