
- •Поверхностные явления
- •Жидкость Газ
- •Определение параметрв пав
- •Смачивание флотация
- •Критерии гидрофильности
- •Дисперсные системы
- •Классификация коллоидных систем по агрегатному состоянию дисперсной фазы и дисперсионной среды
- •Классификация по наличию взаимодействия между частицами дисперсной фазы
- •Строение коллоидных частиц
- •Электрохимический или дзета-потенциал
- •Химическая конденсация:
- •Коллоидная защита
- •Седиментационный анализ
- •Эмульсии
- •Электрокинетические явления
- •Электролиз
- •Обратные явления
- •Оптические свойства коллоидных систем
- •Термофорез. Термопреципитация.
- •Размеры вмс
- •Коллиат св-во вмс
- •Мембранное равновесие Доннана
- •Калий-Натриевый насос
Коллоидная защита
У леофобных золей при добавлениинекоторых веществ наблюдается повышение устойчивости. Такие вещества называются защищёнными, а их стабилизирующее действие на системы – коллоидной защитой. Защитными свойствами обладают высокомолекулярные соединения, такие как белки (желатин и альбумин), полисахариды (крахмал), некоторые поверхностно активные вещества (пример ПАВ – олеат натрия(*)) и некоторые порошки. Механизм коллоидной защиты заключается в адсорбции леофильных частиц молекул …(*) на поверхности твёрдой фазы. И превращения её в леофильную, на которой образуется сольватная оболочка, препятствующая слипанию.
|
Механизм коллоидной защиты заключается в адсорбции леофильных частиц молекул …(*) на поверхности твёрдой фазы. И превращения её в леофильную, на которой образуется сольватная оболочка, припятствующая слипанию. защитное действие измеряется минимальным кол-м вещества, которое надо добавить к 10мл исследуемого золя. |
Молекулярно-кинетические свойства дисперсных систем
К ним относится броуновское движение, диффузия, осмотическое давление, (*) седиментация, вязкость. В отличие от истинных растворов, в дисперсных дисперсных системах диффузия протекает медленно, осмотическое давление низкое, для них характерна седиментация. Для некоторых видов она.. (*)
1) Броуновское движение
Как показал Эйнштейн, среднее значение квадрата смещения за промежуток времени τ определяется следующим соотношением:
|
η-(эта) вязкость среды [Па с] r- радиусчастицы измеряя смещение частиц за определенное время можно измерить их размер |
2) Диффузия
– самопроизвольное выравнивание частиц
по всему объему раствора под действием
броуновского движения. Идёт по градиенту
концентрации. Количественно описывается
законами Гика: -div=D∙S∙ τ,
где D-коэфицент
диффузии
τ,
где D-коэфицент
диффузии
D=
|
Скорость диффузии возрастает с увеличением температуры и уменьшается с увеличением размера частиц и вязкости среды |
3) Осмотическое давление
Осмос – явление
проникновения частиц при разности
насыщенности. Зависит от концентрации
осмотически-активных частиц. Величина
осмотического давления пропорциональна
числу частиц растворенного вещества:
 .
.
В случае коллоидных
растворов используют частичную
концентрацию, – число коллоидных частиц
в единице объёма: ν ;
ṅ=
;
ṅ= ;
основываясь на данной зависимости можно
определят молекулярную массу растворенного
вещества, но область осмотических
определений ограничивается веществами
с молекулярной массой от 10 до 500 тыс.
;
основываясь на данной зависимости можно
определят молекулярную массу растворенного
вещества, но область осмотических
определений ограничивается веществами
с молекулярной массой от 10 до 500 тыс.
4) Седиментация – оседание коллоидных частиц под действием сил тяжести или в поле центробежных сил (что ускоряет процесс). Движение частицы в вязкой среде тормозит сила трения. При уравнении силы тяжести и силы трения оседание происходит с постоянной скоростью.
 =mg=Vg
=mg=Vg =
=
 (
( -
- )g
= 6πηrU
[ где U=
)g
= 6πηrU
[ где U=
 =6n
=6n ,
где U –скорость
оседания)( закон оседания Стокса)
,
где U –скорость
оседания)( закон оседания Стокса)
Влияние силы тяжести
для частиц коллоидной степени дисперсности
проявляется в установлении состояния
равновесия, которая называется
седиментационная характеризующая
постепенным уменьшением концентрации
частиц от дна сосуда к верхним слоям
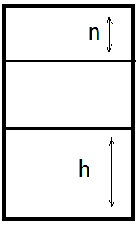
раствора. Для любых однородных частиц
данного размера относительное изменение
их числа в еденице объема в двух слоях
жидкости, отстоящих на расстоянии “h”
определяется уравнением:
 =
=
|
n –верхний слой
M=
= |


 =
=
 =2Dτ
– уравнение Эйнштейна-Смаровского
=2Dτ
– уравнение Эйнштейна-Смаровского =>
=>
 -
нижний, M
–молекулярная масса
-
нижний, M
–молекулярная масса
 =
= π
π
 ’этому
распределению подчиняется распрееление
частиц в атмосфере - параметрическое
уравнение (Лапласа)
’этому
распределению подчиняется распрееление
частиц в атмосфере - параметрическое
уравнение (Лапласа)