
- •Материя, пространство, время, абсолютность и относительность движения, системы отсчёта.
- •Кинематика поступательного движения, материальная точка.
- •Различные варианты механического движения тангенциальное и нормальное ускорения.
- •Кинематика вращательного движения абсолютно твёрдого тела.
- •Первый закон Ньютона, инерциальные и неинерциальные системы отсчёта, инертность, силы инерции.
- •Второй закон Ньютона (две формулировки). Сила, импульс тела, импульс силы.
- •Третий закон Ньютона, границы применимости законов классической механики.
- •Работа и мощность при поступательном движении тела.
- •Механическая энергия, кинетическая и потенциальная.
- •Закон сохранения импульса замкнутой системы, закон сохранения энергии замкнутой системы при упругом и неупругом ударах.
- •11. Силы в механике (упругости, трения, тяготения).
- •Второй закон Ньютона для вращательного движения (две формулы), момент силы, момент инерции.
- •Работа, мощность и кинетическая энергия при вращательном движении.
- •Законы сохранения момента импульса и кинетической энергии замкнутой системы тел.
- •Атомно-молекулярная теория строения вещества, принципы мкт. Уравнение состояния термодинамической системы, параметр состояния (p, V, t), физический смысл t.
- •Уравнение состояния идеального газа, основное уравнение мкт газа.
- •Внутренняя энергия идеального газа и методы её изменения (теплообмен и работа).
- •Первое начало термодинамики (первое начало для четырёх процессов: изотермический, изохорный, изобарный и адиобатный).
- •Термодинамический цикл, цикл Карно, тех. Циклы.
- •Второе начало термодинамики для теплового двигателя идеальной тепловой машины, идеальный холодильник, кпд тепловой машины.
- •Реальные газы, уравнение Ван-Дер-Ваальса, физический смысл поправок а и б, внутренняя энергия реального газа.
- •Энтропия, второй закон термодинамики (общая формулировка). Статистическое толкование второго начала, связь энтропии и вероятности состояния системы, «тепловая смерть вселенной».
Второе начало термодинамики для теплового двигателя идеальной тепловой машины, идеальный холодильник, кпд тепловой машины.
Второй закон термодинамики для теплового двигателя: теплота, сообщённая телу, не вся переходит в работу, часть тепла переходит к более холодному телу.
Переход тепла от холодного тела к горячему невозможен.
КПД тепловой машины:
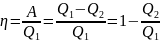
Идеальная тепловая машина — машина, в которой произведённая работа и разница между количеством подведённого и отведённого тепла равны. Работа идеальной машины описывается циклом Карно.
Реальные газы, уравнение Ван-Дер-Ваальса, физический смысл поправок а и б, внутренняя энергия реального газа.
Реальный газ – газ, свойства которых зависят от взаимодействия молекул.
В отличие от идеального газа, в уравнении состояния реального газа учитываются силы взаимодействия между молекулами и реальный V молекул, в частности при нормальных условиях.
Реальный газ занимает 0,0001% от реального объёма.
Если взять 1 моль реального газа m = μ, то уравнение реального газа имеет вид
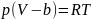
Где b – первая поправка в уравнение Ван-Дер-Ваальса
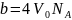
Силы взаимодействия молекул меняют давление молекул на стенки сосуда
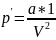
Где a – 2-я поправка в уравнение Ван-Дер-Ваальса, характеризующая силы межмолекулярного притяжения.
В результате уравнение реального газа для m = μ имеет вид:
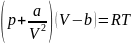
для произвольной массы газа:
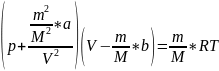
Внутренняя энергия реального газа:

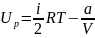
Энтропия, второй закон термодинамики (общая формулировка). Статистическое толкование второго начала, связь энтропии и вероятности состояния системы, «тепловая смерть вселенной».
В термодинамике существует два основных понятия:
Энергия W (агрегатное состояние термодинамической системы)
Энтропия S определяет направленность и быстроту термодинамического процесса.
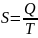
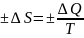
Рассмотрим изолированную систему из двух тел:
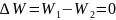
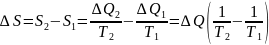
Отсюда следует, что в замкнутой системе общая энергия не изменится, а энтропия увеличится.
2-е начало термодинамики для любых процессов:
В замкнутой термодинамической системе энтропия всегда возрастает.
Границы изменения Энтропии:
Э. любого тела стремится к нулю Кельвина, если температура тела стремится к нулю.
Объяснить второе тело можно только с позиций теории вероятности.
Любая совокупность частиц стремится к равновесию. Э. же характеризует разупорядоченность системы:
чем больше S, тем больше вероятных состояний частиц системы.
Связь Э. и вероятности:
S = k*ln w
w – вероятн.
k = R/NA
Вывод: вероятность сост. В изолированной системе всегда возрастает (2-е нач).
Замечание: этот закон несправедлив при очень малом и очень большом числе молекул.
Тепловая смерть — термин, описывающий конечное состояние любой замкнутой термодинамической системы, и Вселенной в частности. При этом никакого направленного обмена энергией наблюдаться не будет, так как все виды энергии перейдут в тепловую. Термодинамика рассматривает систему, находящуюся в состоянии тепловой смерти, как систему, в которой термодинамическая энтропия максимальна.
