
Лаба 2
.docxФедеральное агентство железнодорожного транспорта
Федеральное государственное бюджетное образовательное учреждение
высшего образования «ПЕТЕРБУРГСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
ПУТЕЙ СООБЩЕНИЯ имени императора Александра I»
Кафедра «Инженерная химия и естествознание»
Дисциплина: «Современные защитные материалы»
Отчёт
По лабораторной работе №2
«оксидные плёнки»
Вариант №1
Выполнил студент
факультета ТЭС
группы ПТМ-613
Сызранов И.Ю.
Проверила
Масленникова Л.Л.
Санкт-Петербург
2018
Цель работы: изучение защитных свойств оксидных плёнок.
Основные теоретические положения:
Опыт 1
Влияние оксидной плёнки на коррозионную стойкость алюминия.
Ход работы:
В 3 пробирки налить по 3-4 мл 2Н раствора серной кислоты и в каждую опустить по кусочку алюминия. Затем в одну из пробирок добавить несколько капель насыщенного раствора сульфата меди (II), в другую – хлорида меди (II), третью оставить в качестве контрольной.
Наблюдать происходящие изменения и сделать вывод о влиянии сульфат – ионов и ионов хлора на скорость коррозии алюминия в серной кислоте.
Al + H2SO4 -> Al2(SO4)3 + H2↑
Al + CuCl2 -> Cu + AlCl3
Вывод:
Опытным путём установлено, что присутствие ионов SO4 не даёт реакции, с ионами Cl разрушилась плёнка и пошла реакция с выделением меди.
Опыт 2
Определение защитных свойств оксидной плёнки.
Ход работы:
K2Cr2O7 + HCl + H2O
Рыжий -> Зелёный при разрушении оксидной плёнки
При разрушении плёнки
Al + K2Cr2O7
Cr (VI) -> Cr (III)
Al = 3e -> Al3+
Cr6+ + -> C3+ (Cr2O3)
Вывод:
Алюминий взаимодействует с K2Cr2O7 (пассивирование) , образуется Al(OH)3, который может преобразовываться в оксидную плёнку
HCl разрушает оксидную плёнку
Опыт 3
Пассивирование железа раствором дихромата калия.
Ход работы:
Очистим пластину наждачкой от плёнки (Fe2O3), чтобы далее добавить
Fe + CuSO4 -> FeSO4 + Cu
Fe + K2Cr2O7 -> Fe2O3 + Cr2O3 + KOH
Fe2O3 – оксидная плёнка
Вывод:
Образуется оксидная плёнка на поверхности Fe при взаимодействии с K2Cr2O7 9%
И не идёт реакция с CuSO4
Задача
Плотность Cd = 8,64 г/см3, плотность CdO = 8,15 г/см3
А
=
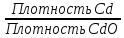 = 0,94 – плёнка не образуется, так как А
не входит в интервал 1,2 < A
< 1,6
= 0,94 – плёнка не образуется, так как А
не входит в интервал 1,2 < A
< 1,6
