
- •ПРЕДИСЛОВИЕ
- •ВВЕДЕНИЕ
- •РАЗДЕЛ I. ФИЗИКО-ХИМИЧЕСКИЕ ОСНОВЫ ГОРЕНИЯ
- •ГЛАВА 1. ГОРЕНИЕ – ОСНОВНОЙ ПРОЦЕСС НА ПОЖАРЕ
- •1.1. Определение горения
- •1.2. Характеристика участников процесса горения
- •1.4. Опасные факторы пожара
- •ГЛАВА 2. МАТЕРИАЛЬНЫЙ БАЛАНС ПРОЦЕССОВ ГОРЕНИЯ
- •2.1. Расчет объема воздуха, необходимого для горения
- •2.1.1. Горючее – индивидуальное химическое соединение
- •2.1.2. Горючее – смесь газов и паров
- •2.2.1. Горючее – индивидуальное химическое соединение
- •2.2.2. Горючее – смесь газов и паров
- •2.2.3. Горючее – сложное вещество с известным элементным составом
- •2.3. Продукты сгорания. Дым и его характеристики
- •ГЛАВА 3. ТЕПЛОВОЙ БАЛАНС ПРОЦЕССОВ ГОРЕНИЯ
- •3.1. Уравнение теплового баланса процесса горения
- •3.3. Расчет температуры горения
- •РАЗДЕЛ II. ТЕОРИИ ГОРЕНИЯ
- •4.1. Тепловая теория горения
- •4.1.1. Механизм химических реакций при горении
- •4.1.2. Факторы, влияющие на скорость реакций горения
- •4.2. Цепная теория горения
- •4.3. Диффузионная теория горения
- •ГЛАВА 5. ПЛАМЯ И ЕГО РАСПРОСТРАНЕНИЕ В ПРОСТРАНСТВЕ
- •5.1. Виды пламени
- •5.2. Структура пламени
- •5.3. Процессы, протекающие в пламени
- •5.4. Скорость распространения пламени
- •5.5. Характер свечения пламени
- •IV.I. ВОЗНИКНОВЕНИЕ ГОРЕНИЯ
- •ГЛАВА 6. САМОВОСПЛАМЕНЕНИЕ
- •ГЛАВА 7. САМОВОЗГОРАНИЕ
- •7.1. Механизм процесса самовозгорания веществ
- •7.2. Самовозгорание жиров и масел
- •7.3. Самовозгорание химических веществ
- •ГЛАВА 8. ВЫНУЖДЕННОЕ ВОСПЛАМЕНЕНИЕ (ЗАЖИГАНИЕ)
- •8.2. Закономерности перехода самовоспламенения к зажиганию
- •8.3. Зажигание нагретым телом
- •8.4. Элементы тепловой теории зажигания
- •8.6. Элементы тепловой теории зажигания электрической искрой
- •8.8. Зажигание твердых и жидких горючих веществ
- •8.9. Зажигание лучистым тепловым потоком
- •8.10. Основные виды и характеристики источников зажигания
- •IV.II. РАЗВИТИЕ ПРОЦЕССОВ ГОРЕНИЯ
- •ГЛАВА 9. ГОРЕНИЕ ГАЗОПАРОВОЗДУШНЫХ СМЕСЕЙ
- •9.1. Концентрационные пределы распространения пламени
- •9.2. Факторы, влияющие на КПР
- •9.2.1. Зависимость КПР от химической природы горючего вещества
- •9.2.2. Влияние начальной температуры смеси на КПР
- •9.2.3. Влияние давления горючей смеси на КПР
- •9.2.4. Влияние флегматизаторов и ингибиторов на КПР
- •ГЛАВА 10. ГОРЕНИЕ ЖИДКОСТЕЙ
- •10.1. Условия для возникновения горения жидкостей
- •9.2. Температурные пределы распространения пламени
- •10.3. Скорость испарения жидкости
- •10.4. Температура вспышки. Температура воспламенения жидкости
- •10.5. Механизм теплового распространения горения жидкостей
- •10.7. Распределение температуры в горящей жидкости
- •10.8. Вскипание и выброс при горении резервуара с ГЖ
- •ГЛАВА 11. ГОРЕНИЕ ТВЕРДЫХ ВЕЩЕСТВ И МАТЕРИАЛОВ
- •11.2. Основные закономерности процессов горения органических твердых горючих материалов
- •11.4. Гетерогенное горение
- •11.5. Горение металлов
- •11.6. Особенности горения пылевидных веществ
- •РАЗДЕЛ V. ВЗРЫВЫ.
- •ГЛАВА 12. ВЗРЫВЫ. УДАРНЫЕ ВОЛНЫ И ДЕТОНАЦИЯ
- •12.1. Основные определения. Типы взрывов
- •12.4. Основные свойства и параметры ударной волны
- •12.6. Взрывчатые вещества
- •12.6.1. Краткие сведения об основных взрывчатых веществах
- •Приложение 1
- •Приложение 2
- •Приложение 3
- •Приложение 4
- •Приложение 5

173
9.2. Факторы, влияющие на КПР
Концентрационные пределы распространения пламени зависят от химических, теплофизических свойств, а также параметров состояния горючего вещества и окислителя. Основными из них являются:
1.Химическая природа горючего и окислителя
2.Начальная температура смеси
3.Начальное давление смеси
4.Наличие флегматизаторов и ингибиторов
9.2.1. Зависимость КПР от химической природы горючего вещества
КПР существенно зависит от длины углеродной цепи и от класса органического вещества, т.е. наличия различных функциональных групп. Так, в гомологическом ряду с увеличением числа углеродных атомов в цепи снижаются оба КПР пламени, причем область воспламенения существенно сужается. Например, для гомологического ряда метана данная зависимость показана на рис.9.1.
С%. об.
15
 СН4
СН4
 С2Н6
С2Н6
С3Н8
10
С4Н10
 С5Н12 С6Н14 С7Н16
С5Н12 С6Н14 С7Н16
5 |
φн |
|
φн
1 |
2 |
3 |
4 |
5 |
6 |
nC |
|
|
|
|
|
|
174
Рис.9.1. Изменение КПР в гомологическом ряду метана
Влияние на КПР пламени различных функциональных групп (кратных связей, карбонильных, карбоксильных, гидроксильных, простых и сложноэфирных групп) наглядно иллюстрируется данными таблицы 9.2.
С появлением в молекуле вещества ненасыщенных связей и увеличением их кратности область воспламенения сильно расширяется. Заметно повышается химическая активность молекул и при появлении в них атомов кислорода. Хотя в этом случае НКПР несколько повышается, но область воспламенения в целом расширяется.
Таблица 9.2.
Концентрационные пределы распространения пламени некоторых веществ
Наименование вещества |
Структурная формула |
ϕн |
ϕв |
|
Этан |
СН3 - СН3 |
3,22 |
12,45 |
|
Этилен |
СН2 = СН2 |
2,75 |
28,60 |
|
Ацетилен |
СН ≡ СН |
2,50 |
80,0 |
|
Пропан |
СН3 - СН2 - СН3 |
2,10 |
9,50 |
|
н-Пропиловый спирт |
СН3 |
- СН2 – СН2 - ОН |
2,10 |
13,55 |
Ацетон |
СН3 – СО - СН3 |
2,26 |
13,00 |
|
Метилэтиловый эфир |
СН3 |
– О - СН2 - СН3 |
2,00 |
10,10 |
Метилацетат |
СН3 |
– О – СО - СН3 |
3,15 |
15,60 |
9.2.2. Влияние начальной температуры смеси на КПР
При увеличении начальной температуры горючей смеси область воспламенения расширяется, в основном за счет увеличения ВКПР. Напр и- мер, зависимость для метана выглядит следующим образом (рис.9.2).
Формулы для расчета концентрационных пределов распространения пламени справедливы при температурах среды близкой к 200С. Для более
175
высоких температур необходимо производить расчет с учетом изменения температуры.
Приближенно это можно сделать с помощью следующих формул:
ϕн(t) = ϕн ( 1− |
Т −Т0 |
) |
(9.6) |
||
1550 −Т0 |
|||||
|
|
|
|||
ϕв(t) = ϕв ( 1+ |
Т −Т0 |
|
), где |
(9.7) |
|
1100 −Т0 |
|||||
|
|
|
|||
ϕн, ϕв – концентрационные пределы распространения пламени, рассчитанные или определенные экспериментально при 200С;
ϕн(t) ,ϕн(t) – концентрационные пределы распространения пламени при температуре Т; 1550 К, 1100 К – температура горения соответственно на НКПР и ВКПР.
Расчет КПР при |
Пример 9.4. Рассчитать КПР газа пропана С3Н8 при |
повышенных |
3000С. |
температурах |
|
|
|
1.В примере 8.2. были рассчитаны значения НКПР и ВКПР для пропана при 200С:
ϕн = 2,07 %; ϕв = 12,03%.
2.С учетом заданной температуры КПР составят:
ϕн(t) = 2,07 ( 1 |
− |
|
|
573 |
−293 |
) = 1,61 % |
||
1550 |
−293 |
|||||||
|
|
|
||||||
ϕв(t) = 12,03 ( 1+ |
|
573 −293 |
) = 16,20 % |
|||||
1100 −293 |
||||||||
|
|
|
|
|
||||
9.2.3. Влияние давления горючей смеси на КПР
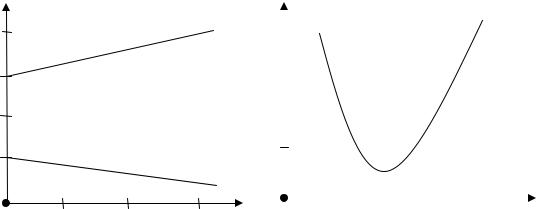
При давлениях выше атмосферного НКПР практически не меняется. Изменение ВКПР зависит от вида горючего. Так, у водорода он остается постоянным вплоть до 127 105 Па (127 атм), а у метана возрастает в три с лишним раза. При разрежении область воспламенения сужается и при определенном давлении, для каждого горючего своем, сливаются. При еще более
176
низких давлениях смесь становится негорючей (рис.9.3).
|
φ,% |
|
|
φ,в |
|
Р, Па |
|
|
|
|
||
|
|
|
|
|
|
|||||||
20 |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
Область |
||||
|
|
|
|
|
|
|
|
|
|
воспламенения |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
15 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
10 |
|
|
|
|
|
|
|
|
|
|
|
|
5 |
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
φ,н |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Т,К |
|
|
φ,% об |
|||||
300 |
400 |
500 |
600 |
|
|
|||||||
Рис.9.2. Зависимость КПР мета- |
|
|
Рис.9.3. Влияние давления на |
|||||||||
|
|
|
но-воздушной смеси от |
|
|
|
область воспламенения |
|||||
|
|
|
начальной температуры |
|
|
|
метана |
|||||
9.2.4. Влияние флегматизаторов и ингибиторов на КПР
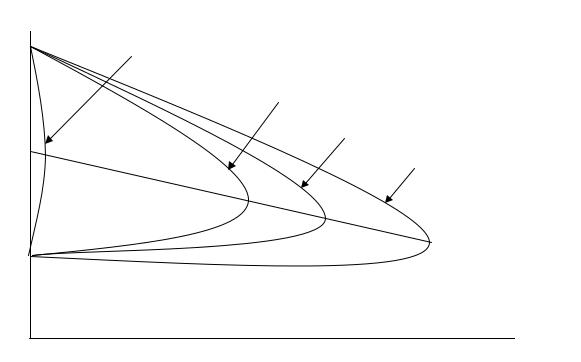
При введении инертных газов в газопаровоздушную смесь область воспламенения сужается, причем в основном за счет уменьшения ВКПР. Нижний предел возрастает незначительно. Графически зависимость КПР = f(ϕф) имеет вид треугольника и часто носит название "полуострова флегматизации". На рис.9.4 показан "полуостров флегматизации" метана различными газами. Точка Ф, находящаяся на мысе "полуострова", в которой КПР сливаются, называется минимальной флегматизирующей концентрацией. Это важнейшая характеристика инертных (нейтральных) газов, применяемых для предотвращения и тушения пожаров.
Минимальная флегматизирующая концентрация флегматизатора - это наименьшая концентрация флегматизатора, добавляемая в смесь горючего с окислителем, при которой смесь становится неспособной к распространению пламени при любом соотношении горючего и окислителя.
177
Применяется этот показатель при расчетах взрывоопасных составов газо-, паро- и пылевоздушных смесей в технологических и других процессах.
Флегматизирующая способность зависит от ряда теплофизических свойств флегматизаторов: теплоемкости, теплопроводности.
Ингибиторы горения, например, хладоны, по своей огнетушащей способности в десятки раз превосходят инертные газы. "Полуостров флегматизации" у хладонов почти незаметен на графике, поскольку их минимальная флегматизирующая концентрация не превышает 2,5 % об.
φ,% |
|
|
|
|
|
|
15 |
хладоны |
|
|
|
|
|
|
|
|
СО2 |
|
|
|
|
|
|
|
N2 |
|
|
10 |
|
|
|
|
Ar |
|
5 |
|
|
|
|
Ф |
|
|
|
|
|
|
|
|
|
10 |
20 |
30 |
40 |
50 |
φф,% |
|
|
|||||
Рис.9.4. Изменение КПР метана в зависимости от количества и |
|
|||||
|
|
вида инертных газов |
|
|
||
В практических расчетах для организации эффективной противопожарной защиты часто требуется знать геометрические размеры взрывоопасной зоны.
178
Метод расчета размеров зон, ограниченных НКПР газов и паров, при аварийном поступлении горючих газов и паров ненагретых легковоспламеняющихся жидкостей в помещение
Расстояния ХНКПР, YНКПР и ZНКПР для ГГ и ЛВЖ, ограничивающие область концентраций, превышающих НКПР, рассчитывают по формулам
ХНКПР = K1 |
|
|
|
|
δ C0 |
0,5 |
, |
(9.8) |
|||
|
ln |
|
|
||||||||
|
|
|
|||||||||
l K2 |
|
|
|
|
|||||||
|
|
|
|
CНКПР |
|
|
|||||
YНКПР = K1 |
|
|
|
|
|
δ C0 |
0,5 |
|
|||
|
2 |
ln |
|
|
, |
(9.9) |
|||||
|
|
|
|||||||||
b K |
|
|
|
|
|
||||||
|
|
|
|
|
|
CНКПР |
|
|
|||
ZНКПР = K3 |
|
|
|
|
|
δ C0 |
|
0,5 |
|
||
|
|
ln |
|
|
, |
(9.10) |
|||||
|
|
|
|||||||||
h K2 |
|
|
|
|
|
||||||
|
|
|
|
|
|
CНКПР |
|
|
|||
где К1 – коэффициент, принимаемый равным
1,1314 для горючих газов и
1,1958 для легковоспламеняющихся жидкостей; К2 – коэффициент, равный
1 для ГГ и Т/3600 для ЛВЖ;
Т – продолжительность поступления паров ЛВЖ, с; К3 – коэффициент, принимаемый равным
0,0253 для ГГ при отсутствии подвижности воздушной среды,
0,02828 для ГГ при подвижности воздушной среды,
0,04714 для ЛВЖ при отсутствии подвижности воздушной среды,
0,3536 для ЛВЖ при подвижности воздушной среды; l – длина помещения , м;
b – ширина помещения, м;
h– высота помещения, м;
δ– допустимые отклонения концентраций при задаваемом уровне значимости. При уровне значимости Q = 0,05 значения δ будут равны
1,27 для ЛВЖ при работающей вентиляции,
1,25 для ЛВЖ при неработающей вентиляции,
1,37 для ГГ при работающей вентиляции,
1,38 для ГГ при неработающей вентиляции; С0 – предэкспоненциальный множитель, % (объемн.), равный:
С0 |
= 3,77 103 |
|
m |
|
для ГГ при отсутствии подвижности воздушной среды, |
||||||
ρ |
г |
V |
|||||||||
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
св |
|
|
||
С0 |
= 3 |
102 |
|
|
m |
|
|
|
для ГГ при подвижности воздушной среды, |
||
ρ |
г |
V |
|
U |
|
||||||
|
|
|
|
|
|
||||||
|
|
|
|
|
св |
|
|
|
|||
U – подвижность воздушной среды, м/с;
|
|
|
|
|
|
|
|
|
179 |
|
|
|
m 100 |
0,41 |
для ЛВЖ при отсутствии подвижности воздушной среды, |
||||
С0 |
|
|
|
||||||
C |
|
ρ |
|
V |
|||||
= CH |
|
|
|
||||||
|
|
|
H |
|
п |
св |
|
||
|
|
|
m 100 |
0,46 |
для ЛВЖ при подвижности воздушной среды; |
||||
С0 |
|
|
|
|
|||||
|
C |
|
ρ |
|
V |
||||
= CH |
|
|
|
||||||
|
|
|
H |
|
п |
св |
|
||
СН – концентрация насыщенных паров при расчетной температуре, кПа. СН может быть рассчитана по формуле:
СН = 100 pH , где p0
РН – давление насыщенных паров при расчетной температуре, кПа; Р0 – атмосферной давление, равное 101, 3 кПа; ρп – плотность паров, кг/м3.
Плотность паров ρп рассчитывается по формуле: ρп = М/Vм, кг/м3.
При отрицательных значениях логарифмов расстояния ХНКПР, YНКПР и ZНКПР принимают равным 0.
Во всех случаях значения расстояний ХНКПР, YНКПР и ZНКПР должны быть не менее 0,3 м для ГГ и ЛВЖ.
Расчет размеров зон,
ограниченных НКПР газов и паров
Данные для расчета:
Пример 9.5. Определить размеры зоны, ограниченной
НКПР паров, образующейся при аварийной разгерметизации аппарата с ацетоном при работающей и неработающей вентиляции.
В центре помещения размером 40×40×3 м установлен аппарат с ацетоном. Масса ацетона в аппарате 25 кг. Расчетная температура в помещении 300С, давление нормальное. НКПР ацетона составляет 2,7 % (об). В результате разгерметизации в помещение поступило 25 кг паров ацетона за время испарения 208 с. При работающей общеобменной вен-
тиляции подвижность воздушной среды в помещении υ = 0,1 м/с.
Решение:
1.Расчет молярного объема паров при заданных условиях.
VМ = 1 27322,4 3031 = 24,9 м3/кмоль.
2.Расчет плотности паров при заданных условиях.
М(СН3СОСН3) = 58 кг/кмоль
ρп = М/Vм = 58/24,9 = 2,33 кг/м3.
3.Расчет свободного объема помещения.
Vсв = 40 40 3 0,8 = 3840 м3.
4.Расчет давления насыщенного пара ацетона при 300С по уравнению Антуана.

180
Уравнение Антуана: lg р = 6,37551 – 1281,721/(237,088 + t)
|
(6,37551− |
1281,721 |
) |
|
РН = 10 |
237,088+30 |
|||
|
= 37,73 кПа. |
5.Расчет концентрации насыщенных паров СН.
СН = 100 37,73/101,3 = 37,36 %.
6.Расчет предэкспоненциального множителя С0 при работающей вентиляции.
С0 |
|
25 100 |
0,46 |
||
= 37,36 |
|
|
= 3,93 % |
||
3736 2,33 3840 |
|||||
|
|
|
|
||
7. Расчет предэкспоненциального множителя С0 при неработающей вентиляции.
С0 |
|
25 100 |
0,41 |
||
= 37,36 |
|
|
= 5,02 % |
||
3736 2,33 3840 |
|||||
|
|
|
|
||
8. Расстояния ХНКПР, YНКПР |
и ZНКПР при работающей вентиляции составят |
|||||||||||||||||
ХНКПР = 1,1958 |
|
|
|
208 |
|
|
|
|
|
|
1,27 3,93 |
0,5 |
||||||
40 |
|
|
|
|
|
|
ln |
|
|
|
|
|
= 9,01 м |
|||||
3600 |
|
|
|
2,7 |
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
YНКПР = 1,1958 |
|
|
|
|
208 |
|
|
|
|
|
|
1,27 3,93 |
0,5 |
|||||
40 |
|
|
|
|
|
|
|
|
ln |
|
|
|
|
|
= 9,01 м |
|||
|
3600 |
|
|
2,7 |
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
ZНКПР = 0,3536 |
3 |
|
|
208 |
|
ln |
1,27 |
3,93 |
0,5 |
= 0,2 м. |
||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||
3600 |
|
|
|
2,7 |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
9. Расстояния ХНКПР, YНКПР |
и ZНКПР при неработающей вентиляции составят |
|||||||||||||||||
ХНКПР = 1,1958 |
|
|
|
208 |
|
|
|
|
|
|
1,25 5,02 |
0,5 |
||||||
40 |
|
|
|
|
|
|
ln |
|
|
|
|
|
= 10,56 м |
|||||
3600 |
|
|
|
2,7 |
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
YНКПР = 1,1958 |
|
|
|
|
208 |
|
|
|
|
|
|
1,25 5,02 |
0,5 |
|||||
40 |
|
|
|
|
|
|
|
|
ln |
|
|
|
|
|
= 10,56 м |
|||
|
3600 |
|
|
2,7 |
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
208 |
|
|
|
|
|
|
1,25 5,02 0,5 |
|||||||
ZНКПР = 0,04714 3 |
|
|
|
|
|
ln |
|
|
|
|
= 0,03 м. |
|||||||
3600 |
|
|
2,7 |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
За начало отсчета принимают внешние габаритные размеры аппарата.
Расчет безопасных |
Пример 9.5. Газоанализатор показал наличие 0,3 % па- |
концентрации газов и |
ров амилацетата СН3СООС5Н11. Можно ли проводить |
паров с использованием |
сварочные работы? |
|
|
коэффициентов |
|
безопасности |
|
|
|
Значения НКПР И ВКПР следует применять при расчетах безопасных концентраций газов и паров с использованием коэффициентов безопасности:
ϕг.без. ≤ ϕн , где (9.11)
Кб
ϕг.без. – безопасная концентрация горючих газов, паров или пылей, % объемных;

181
ϕн – НКПР, % объемных;
Кб – коэффициент безопасности.
1.При расчете взрывобезопасных концентраций газов, паров и пылей внутри технического оборудования, трубопроводов, вентиляционных систем.
Кб = 2.
2.При расчете предельно-допустимых взрывобезопасных концентраций газов,
парво, пылей в воздухе рабочей зоны с потенциальными источниками зажигания
Кб = 20.
Решение:
1. Составляем уравнение реакции горения амилацетата.
СН3СООС5Н11 + 9,5( О2 + 3,76 N2 ) =7СО2 + 7Н2О + 9,5· 3,76 N2
|
β = 9,5 |
100 |
|
|
2. |
ϕн = НКПР = |
= 1,14 % |
||
8,684 9,5 + 4,679 |
3. Рассчитаем безопасную концентрацию:
ϕг.без. = 120,14 = 0,05 %
0,3 > 0,05, следовательно, проводить сварочные работы нельзя.
Задания для самоконтроля
1.Как связаны нормальная и видимая скорости распространения пламени?
2.Укажите значение α в области безопасных концентраций.
3. Как влияет отвод тепла на скорость распространения пламени?
4. Как называется область концентраций горючего вещества выше ВКПР? Почему она так называется?
5. Зависит ли Uн от скорости химической реакции? Поясните.
6. Изобразите графически изменение температуры в кинетическом пламени. 7. Влияют ли инертные примеси на Uн? Поясните.
8. КПР вещества составляет 2-20 %. Какова пожаробезопасная область для этого вещества при проведении сварочных работ?
9. Как влияет на КПР начальная температура смеси?
10. В какой области концентраций горючего находится стехиометрическая концентрация?
11. В каком случае возникает стационарное пламя?
12. Сущность закона косинусов.
13. Что означает и чему равно критическое значение Uh?
14. КПР этилена 3-32 %, а КПР пропана 2-9,5 %. Сравните пожарную опасность этих веществ.
15. Как зависит КПР от концентрации флегматизаторов и ингибиторов? 16. Сколько зон можно выделить во фронте пламени?
17. Что называется нормальной скоростью распространения пламени?
18. Как связаны массовая и нормальная скорости распространения пламени? 19. Являются ли КПР конкретного вещества постоянной величиной? Почему? 20. Что называется фронтом пламени?
21. Как зависит Uн от состава горючей смеси?
