
- •1)Азотистый баланс
- •1. Синтез 5'-фосфорибозиламина
- •Реакции синтеза амф и гмф
- •4. Образование нуклеозидтрифосфатов атф и гтф.
- •1) Главные компоненты желудочного сока
- •Реакция взаимопревращения глицина и серина
- •2) Распад пуриновых оснований
- •3) Регуляция синтеза белка
- •4) Обнаружение молочной кислоты в желудочном
- •1. Метаболизм феиилаланина
- •2. Особенности обмена тирозина в разных тканях
- •Механизм реакции синтеза дезоксирибонуклеотида
- •3. Реакция фосфорилирования
- •4) Определение свободной соляной кислоты
- •Окисление аланина
- •3) Синтез амидов из карбоновых кислот
- •1. Особенности обмена метионина
- •2. Обмен цистеина
- •4) Мочевая кислота сыворотки крови
- •Реакция синтеза глутаминовой кислоты
- •Реакция синтеза глутамина
- •Реакция синтеза аспарагина
- •Переваривание белков в желудочно-кишечном тракте
Реакция синтеза глутаминовой кислоты
-
синтез глутамина – взаимодействие глутамата с аммиаком. Является главным способом уборки аммиака, наиболее активно происходит в нервной и мышечной тканях, в почках, сетчатке глаза, печени. Реакция протекает в митохондриях.
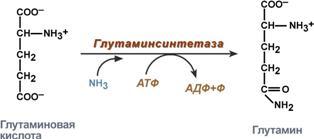
Реакция синтеза глутамина
Образование большого количества глутамина обеспечивает высокие концентрации его в крови (0,5-0,7 ммоль/л).
Так как глутамин проникает через клеточные мембраны путем облегченной диффузии, то он легко попадает не только в гепатоциты, но и в другие клетки, где есть потребность в аминогруппах. Азот, переносимый глутамином, используется клетками для синтеза пуринового и пиримидинового колец, гуанозинмонофосфата (ГМФ), аспарагина, глюкозамино-6-фосфата (предшественник всех остальных аминосахаров).
-
синтез аспарагина – взаимодействие аспартата с аммиаком. Является второстепенным способом уборки аммиака, энергетически невыгоден, т.к. при этом тратятся 2 макроэргические связи,
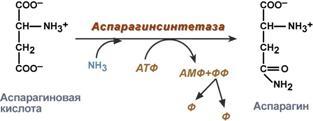
Реакция синтеза аспарагина
-
синтез карбамоилфосфата в митохондриях печени – реакция является первой в процессе синтеза мочевины, средства для удаления аммиака из организма.
2)
П р е в р а щ е н и е а м и н о к и с л о т п о к а р б о к с и л ь н о й г р у п п е
Такое превращение связано с удалением карбоксильной группы от аминокисло-
ты и образованием биогенных аминов.
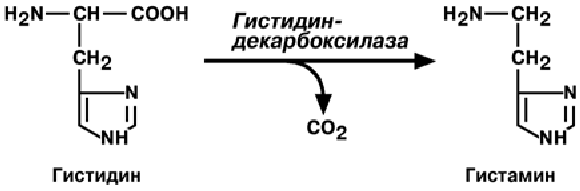
Г И С Т А М И Н
Реакция образования гистамина наиболее активно идет в тучных клетках, базо-
филах и эозинофилах. В них гистамин синтезируется и накапливается в секреторных
гранулах.
В кровь гистамин выделяется при повреждении ткани, при ударе, электрическом
раздражении. В клинической практике секреция гистамина обычно связана с аллер-
гиями – при повторном попадании антигена в ранее сенсибилизированный организм
развивается аллергическая реакция.
Физиологические эффекты
1. Расширение артериол и капилляров. Как следствие – покраснение кожи, сни-
жение артериального давления;
2. Повышение проницаемости стенки капилляров. Как следствие, выход жидкости
в межклеточное пространство – отечность, снижение артериального давления;
3. Если п.п.1 и 2 наблюдаются в головном мозге – повышение внутричерепного
давления;
4. Увеличивает тонус гладких мышц бронхов. Как следствие – спазм и удушье;
5. Слабо повышает тонус мышц желудочно-кишечного тракта.
6. Стимулирует секрецию слюны и желудочного сока.
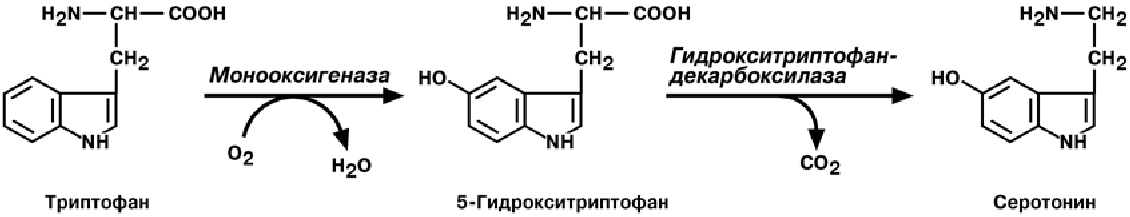
С Е Р О Т О Н И Н
Серотонин активно синтезируется в тучных клетках кожи, в селезенке, ЦНС, лег-
ких, печени.
Физиологические эффекты
1. Стимулирует сокращение гладких мышц желудочно-кишечного тракта. Как
следствие, повышение перистальтики ЖКТ;
2. Выражено стимулирует сокращение гладких мышц сосудов, кроме сосудов
миокарда и скелетных мышц. Как следствие, повышение артериального давления;
3. Слабо увеличивает тонус гладких мышц бронхов;
4. В центральной нервной системе является тормозным медиатором;
5. В периферических нервных окончаниях обуславливает возникновение боли и
зуда (например, при укусе насекомых).
Г А М М А - А М И Н О М А С Л Я Н А Я К И С Л О Т А
Синтез γ-аминомасляной кислоты происходит в центральной нервной системе, в
подкорковых образованиях головного мозга (гипоталамус, черная субстанция, блед-
ный шар).
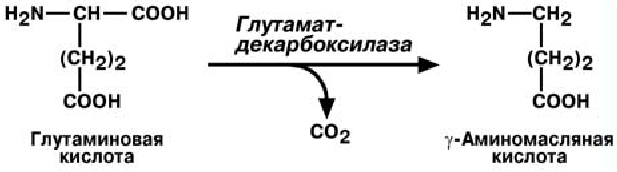
Физиологические эффекты
В центральной нервной системе является тормозным медиатором;
О Б Е З В Р Е Ж И В А Н И Е Б И О Г Е Н Н Ы Х А М И Н О В
Реакции инактивация биогенных аминов протекают с образованием свободного
аммиака и ФАДН2. Катализирует реакцию моноаминоксидаза, она обнаружена во
многих тканях, но наиболее активна в печени, желудке, почках, кишечнике, нервной
ткани.
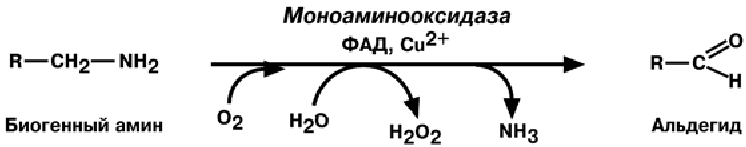
3)
Синтез пуриновых оснований происходит во всех клетках организма, глвнам об-разом в печени. Исключение составляют эритроциты, полиморфноядерные лейкоци-ты, лимфоциты.
На синтез пуринового кольца затрачивается 6 молекул АТФ
Рибозо-5-фосфат является тем якорем, на основе которого синтезируется
пуриновый цикл. Первая реакция синтеза пуринов заключается в активации уг-лерода в первом положении рибозо-5-фосфата, это достигается синтезом 5-фосфоибзил-1-пирофосфата. Вторая реакция – это еренс NH2-группы глутами-на на активированный атом С1 рибозо-5-фосфата с образованием 5-фосфо-рибозиламина
4) Принцип:креатин в щел.ср. дает с пикрин.кислотой пикрат кератина оранж-крас цвета. Интенсивность овраски пропорциональна концентр.креатина в моче
Ход работы: в 2 пробирки: 1-вносят мочу, разведен в 50 раз, во2-эталон.р-р кератина. В каждую пробирку по 0,5 пикриновой к-ты, по 0,5 NaOH. Перемешивают и чз 30 мин колориметрируют.
Нормальные величины:
Д:27-62 мкмоль/л
Ж:44-88 мкмоль/л, М: 44-100 мкмоль/л
Билет №16
1)
При ухудшении всасывания аминокислот, при избытке белковой пищи, при на-
рушении деятельности пищеварительных желез, недопереваренные остатки белков
достигают толстого кишечника, где подвергаются воздействию кишечной микрофло-
ры. Этот процесс получил название гниение белков в кишечнике. Он также акти-
вируется при снижении перистальтики кишечника (запоры). При этом образуются
продукты разложения аминокислот, представляющие собой как токсины (кадаве-
рин, путресцин, крезол, фенол, скатол, индол, пиперидин, пирролидин), так и ней-
ромедиаторы (серотонин, гистамин, октопамин. тирамин). При распаде серусодер-
жащих аминокислот образуются сероводород и метилмеркаптан (СН3SН).
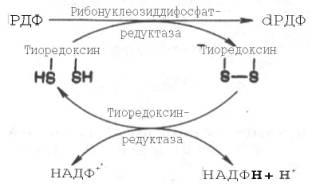
2) Тиоредоксин легко окисляется, превращаясь в дисульфидную S-S-форму. Для его восстановления в системе имеется специфический ФАД-содержащий фермент тиоредоксинредуктаза (мол. масса 68000), требующая наличия восстановленного НАДФН. Обозначив условно рибонуклеозиддифосфат РДФ, образование дезоксирибонуклео-тидов можно представить следующим образом:
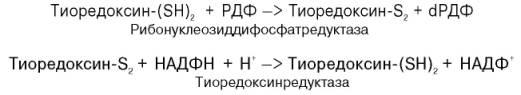
Обе стадии могут быть представлены в виде схемы:
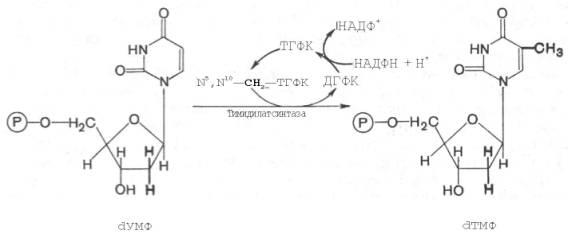
Для синтеза тимидиловых нуклеотидов, помимо дезоксирибозы, требуется также метилированное производное урацила – тимин. Оказалось, что в клетках имеется особый фермент тимидилатсинтаза, катализирующая метилирование не свободного урацила, а dУМФ; реакция протекает по уравнению:
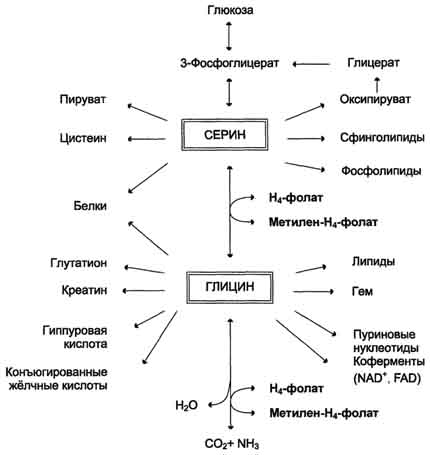
3) Глицин - также заменимая аминокислота, основным источником которой служит серии. Реакцию синтеза глицина из серина катализирует фермент серин-оксиметилтрансфераза, кофермен-том которой является Н4-фолат (см. схему А).
Реакция превращения серина в глицин легко обратима. Основной путь катаболизма глицина у человека и других позвоночных также связан с использованием Н4-фолата (см. схему Б).
Эта реакция обратима и катализируется глицинсинтазой - ферментным комплексом, похожим на пируватдегидрогеназный комплекс, и локализованным в митохондриях клеток печени. По последним данным глицинрасщепляющая ферментная система несколько отличается от глицинсинтазы и содержит 4 белка: Р-белок, включающий кофермент ПФ, Н-белок, содержащий липоевую кислоту, Т-белок с коферментом Н4-фолат, L-белок, являющийся дигидролипоилдегидрогеназой с коферментом NAD+.
4)
Билет №17
1)
С И Н Т Е З М О Ч Е В И Н Ы
В печеночные клетки аммиак попадает в виде глутамина, глутаминовой кислоты,
аланина, в свободном виде. Кроме этого, при метаболизме он образуется в большом
количестве и в самих гепатоцитах. В печени весь аммиак используется для синтеза
мочевины. Увеличение синтеза мочевины наблюдается при распаде тканевых бел-
ков (голодание, избыточные физические нагрузки, сахарный диабет) или избыточном
белковом питании.
Реакции синтеза мочевины являются циклическим процессом и получили назва-
ние орнитиновый цикл.
Синтез мочевины начинается в митохондриях (первая и вторая реакции), ос-
тавшиеся три реакции идут в цитозоле. Для переноса цитруллина и орнитина через
митохондриальную мембрану существуют специальные переносчики.
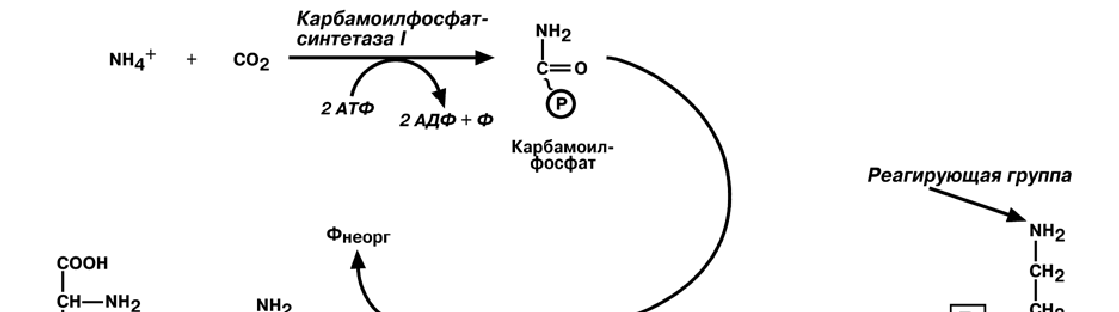
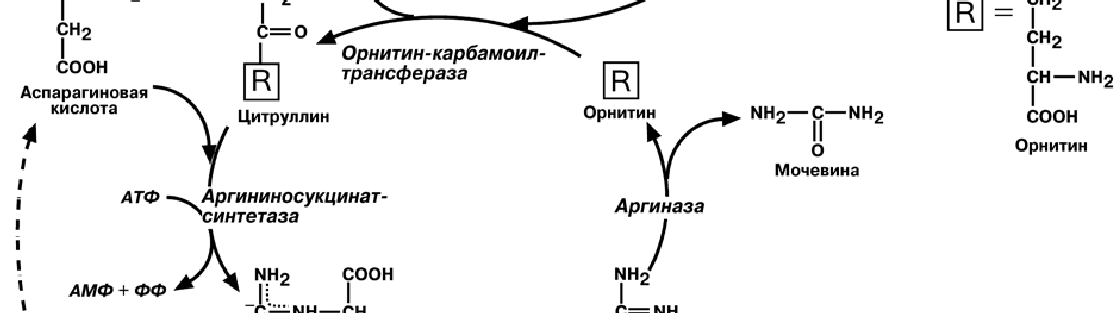
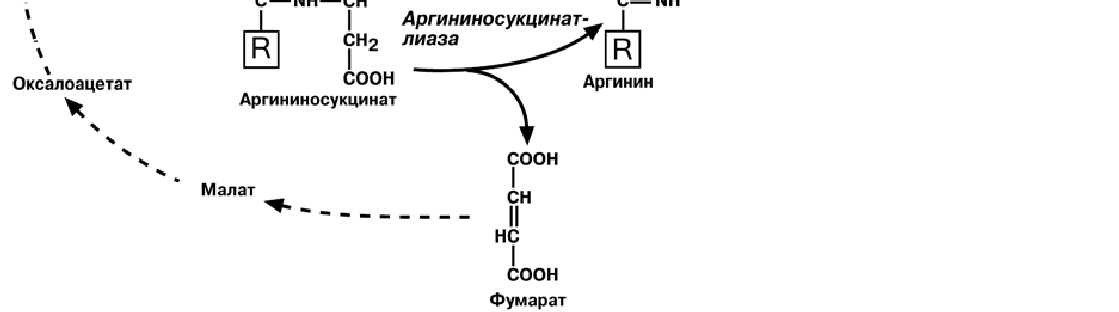
В образовании одной молекулы мочевины участвует 1 молекула NH3, 1 молекула
CO2, аминогруппа 1 молекулы аспарагиновой кислоты, затрачивается 4 макроэрги-
ческих связи трех молекул АТФ.__
2)
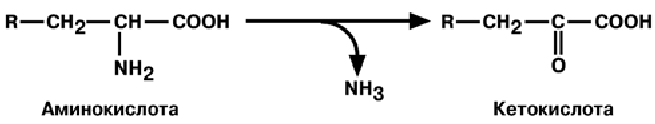
тИ П Ы Д Е З А М И Н И Р О В А Н И Я
• внутримолекулярное – с образованием ненасыщенной жирной кислоты;
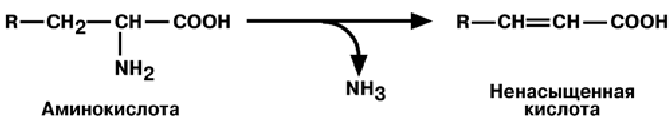
• восстановительное – с образованием насыщенной жирной кислоты;
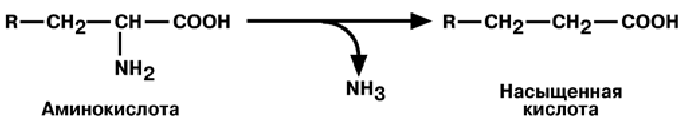
• гидролитическое – с образованием карбоновой гидроксикислоты;

• окислительное – с образованием кетокислот.
3)
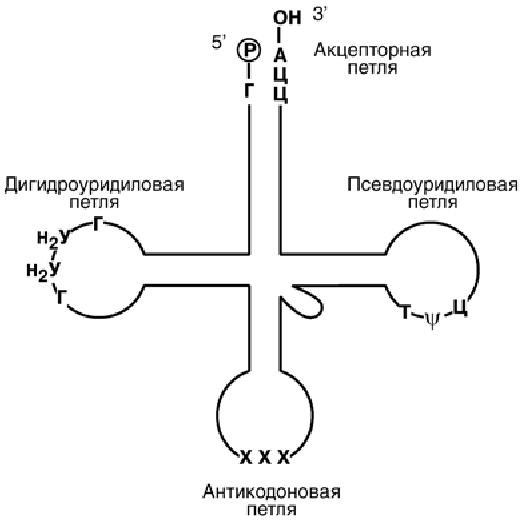
Транспортные РНК (тРНК) бактерий и эукариот включают 73-93 нуклеотида. Они переносят аминокислоты из цитозоля к рибосомам.Вторичная структура тРНК напоминает клеверный лист, а третичная – латинскую букву L.В «клеверном листе» выделяют четыре участка (или ветви, петли), каждый из которых имеет собственную функцию: антикодоновый,псевдоуридиловый, дигидроуридиловый, акцепторный. На 5’-конце тРНК находится гуаниловый нуклеотид, на 3’-конце – триплет Ц-Ц-А.
4)
Определение свободной соляной кислоты
в желудочном соке
Отклонения в составе пищеварительных соков или появление в
них компонентов, не содержащихся в физиологических условиях,
дают важную информацию о патологии пищеварения. В
клинической практике используют методы анализа желудочного
сока для диагностики и лечения заболеваний.
При анализе желудочного сока определяют его общее
количество, цвет, запах, наличие слизи, общую кислотность,
количество свободной и связанной соляной кислоты, присутствие
молочной кислоты, крови и желчных пигментов.
А. ПРИ ПОМОЩИ ИНДИКАТОРА «КОНГО КРАСНЫЙ»
Принцип
В присутствии свободной соляной кислоты в желудочном соке
индикатор «конго красный» меняет окраску на синюю, оставаясь в
нейтральной и щелочной среде красным (зона перехода рН 3,0-5,2).
Реактивы индикаторная бумага «конго красный»
Материал исследования
Нормальный и патологический желудочный сок.
Проведение анализа
На две разные полоски индикаторной бумаги наносят
стеклянной палочкой по 1 капле нормального и патологического
желудочного сока.
Б. ПРИ ПОМОЩИ ИНДИКАТОРА ДИМЕТИЛАМИНОАЗОБЕНЗОЛА
Принцип
Индикатор, п-диметиламиноазобензол, в присутствии
свободной соляной кислоты, имеет красную окраску, в щелочной
среде – желтую (зона перехода рН 2,3-4,2).
Реактивы
Индикатор п-диметиламиноазобензол.
Материал исследования
Нормальный и патологический желудочный сок.
Проведение анализа
В две пробирки вносят по 10 капель исследуемого желудочного
сока, добавляют по 2 капли п-диметиламиноазобензола.__
Билет №18
1)
