
- •Боровская модель атома
- •Полуклассическая теория Бора
- •Модели атомов
- •Решение уравнения Шрёдингера
- •Визуализация орбиталей атома водорода
- •Принцип Паули
- •[Править] Строение атомов и принцип Паули
- •Распределение электронов по орбиталям в водородоподобных и многоэлектронных атомах
- •Структура периодической системы
- •Ядерно-физические характеристики
- •Моменты ядра
- •Магнитный момент
- •Электрический квадрупольный момент
- •Энергия связи
- •Ядерные силы
- •Уровни ядра
- •Ядерные реакции
- •Закон радиоактивного распада
- •Виды лучей радиоактивного распада
- •Альфа-распад
- •Бета-распад
- •Гамма-распад (изомерный переход)
- •Цепные реакции
- •Типы реакций
- •Термоядерная энергетика и гелий-3
- •Стандартная модель
- •Фермионы
- •Античастицы
- •Номенклатура мезонов
- •Мезоны без аромата
- •Мезоны с ароматом
Боровская модель атома
Материал из Википедии — свободной энциклопедии
![]()
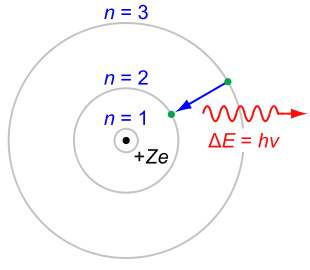
Боровская модель водородоподобного атома (Z — заряд ядра), где отрицательно заряженный электрон заключен в атомной оболочке, окружающей малое, положительно заряженное атомное ядро. Переход электрона с орбиты на орбиту сопровождается излучением или поглощением кванта электромагнитной энергии (hν).
Бо́ровская моде́ль
а́тома (Моде́ль Бо́ра) —
полуклассическая модель атома,
предложенная Нильсом
Бором
в 1913 г. За основу он взял планетарную
модель атома, выдвинутую Резерфордом.
Однако, с точки зрения классической
электродинамики, электрон в модели
Резерфорда, двигаясь вокруг ядра, должен
был бы излучать
непрерывно, и очень быстро, потеряв
энергию, упасть на ядро. Чтобы преодолеть
эту проблему Бор ввел допущение, суть
которого заключается в том, что электроны
в атоме могут двигаться только по
определенным (стационарным) орбитам,
находясь на которых они не излучают, а
излучение или поглощение происходит
только в момент перехода с одной орбиты
на другую. Причем стационарными являются
лишь те орбиты, при движении по которым
момент количества движения электрона
равен целому числу постоянных
Планка[1]:
![]() .
.
Используя это допущение и законы классической механики, а именно равенство силы притяжения электрона со стороны ядра и центробежной силы, действующей на вращающийся электрон, он получил следующие значения для радиуса стационарной орбиты Rn и энергии En находящегося на этой орбите электрона:

Здесь me — масса электрона, Z — количество протонов в ядре, ε0 — диэлектрическая постоянная, e — заряд электрона.
Именно такое выражение для энергии можно получить, применяя уравнение Шрёдингера, решая задачу о движении электрона в центральном кулоновском поле.
Радиус первой орбиты в атоме водорода R0=5,2917720859(36)×10−11 м[2], ныне называется боровским радиусом, либо атомной единицей длины и широко используется в современной физике. Энергия первой орбиты E0 = − 13.6 эВ представляет собой энергию ионизации атома водорода.
Полуклассическая теория Бора
Основана на двух постулатах Бора:
-
Атом может находиться только в особенных стационарных, или квантовых, состояниях, каждому из которых отвечает определенная энергия. В стационарном состоянии атом не излучает электромагнитных волн.
-
Излучение и поглощение энергии атомом происходит при скачкообразном переходе из одного стационарного состояния в другое, при этом имеют место два соотношения:
-
ε = En2 − En1, где
 —
излучённая (поглощённая) энергия,
—
излучённая (поглощённая) энергия,
 —
номера квантовых состояний. В
спектроскопии
—
номера квантовых состояний. В
спектроскопии
 и
и
 называются
термами.
называются
термами. -
Правило квантования момента импульса:


Далее исходя из соображений классической физики о круговом движении электрона вокруг неподвижного ядра по стационарной орбите под действием кулоновской силы притяжения, Бором были получены выражения для радиусов стационарных орбит и энергии электрона на этих орбитах:
![]()
![]() м —
боровский
радиус.
м —
боровский
радиус.
![]()
![]() —
энергетическая
постоянная
Ридберга
(численно равна 13,6 эВ).
—
энергетическая
постоянная
Ридберга
(численно равна 13,6 эВ).
Модели атомов
-
Кусочки материи. Демокрит полагал, что свойства того или иного вещества определяются формой, массой, и пр. характеристиками образующих его атомов. Так, скажем, у огня атомы остры, поэтому огонь способен обжигать, у твёрдых тел они шероховаты, поэтому накрепко сцепляются друг с другом, у воды — гладки, поэтому она способна течь. Даже душа человека, согласно Демокриту, состоит из атомов[2].
-
Модель атома Томсона (модель «Пудинг с изюмом», англ. Plum pudding model). Дж. Дж. Томсон предложил рассматривать атом как некоторое положительно заряженное тело с заключёнными внутри него электронами. Была окончательно опровергнута Резерфордом после проведённого им знаменитого опыта по рассеиванию альфа-частиц.
-
Ранняя планетарная модель атома Нагаоки. В 1904 году японский физик Хантаро Нагаока предложил модель атома, построенную по аналогии с планетой Сатурн. В этой модели вокруг маленького положительного ядра по орбитам вращались электроны, объединённые в кольца. Модель оказалась ошибочной.
-
Планетарная модель атома Бора-Резерфорда. В 1911 году[3] Эрнест Резерфорд, проделав ряд экспериментов, пришёл к выводу, что атом представляет собой подобие планетной системы, в которой электроны движутся по орбитам вокруг расположенного в центре атома тяжёлого положительно заряженного ядра («модель атома Резерфорда»). Однако такое описание атома вошло в противоречие с классической электродинамикой. Дело в том, что, согласно классической электродинамике, электрон при движении с центростремительным ускорением должен излучать электромагнитные волны, а, следовательно, терять энергию. Расчёты показывали, что время, за которое электрон в таком атоме упадёт на ядро, совершенно ничтожно. Для объяснения стабильности атомов Нильсу Бору пришлось ввести постулаты, которые сводились к тому, что электрон в атоме, находясь в некоторых специальных энергетических состояниях, не излучает энергию («модель атома Бора-Резерфорда»). Постулаты Бора показали, что для описания атома классическая механика неприменима. Дальнейшее изучение излучения атома привело к созданию квантовой механики, которая позволила объяснить подавляющее большинство наблюдаемых фактов.
Атом водорода является атомом химического элемента водорода. Он состоит из положительно заряженного протона, который является ядром водородного атома, и единственного отрицательно заряженного электрона. В общем случае, атом водорода описывается двухчастичной матрицей плотности или двухчастичной волновой функцией. Часто в квантовой механике рассматривается электрон в электростатическом поле атомного ядра. В этом случае, электрон описывается редуцированной одночастичной матрицей плотности или волновой функцией. Из-за своей простоты как проблема двух тел атом водорода имеет специальное значение в квантовой механике и релятивистской квантовой механике поскольку соответствующие уравнения допускают точное или приближенное аналитическое решения.
В 1913 Нильс Бор получил спектральные частоты водородного атома в его модели атома водорода, имеющей множество предположений и упрощений. Эти предположения не были полностью правильны, но действительно приводили к правильным значениям энергии. Результаты расчёта Бора для частот и основных значений энергии были подтверждены в 1925/26 полным квантовым-механическим анализом, который использовал уравнение Шрёдингера. Решение уравнения Шрёдингера для электрона в электростатическом поле атомного ядра может быть найдено в аналитической форме. Из него получают уровни энергии электрона и, таким образом, его частоты. Решение уравнения Шрёдингера даёт больше информации и о форме атомных орбиталей (их анизотропии) атома водорода.
Уравнение Шрёдингера также применяется к более сложным атомам и молекулам, однако, в большинстве таких случаев, решение не является аналитическим, и необходимы компьютерные вычисления, или должны быть сделаны какие-нибудь упрощающие предположения.
