
05 семестр / К экзамену-зачёту / Ответы на экзамен 2 / Билет №29_доп
.doc
Элементарная ячейка СаТЮз примитивная, кубическая. Федоровская группа РтЗт. Начало координат обычно выбирают в центре тяжести атомов титана, которые в этом случае занимают все вершины элементарного куба, в центре которого расположен атом кальция. Атомы кислорода распределяются по серединам всех ребер, создавая вокруг атома кальция координационный многогранник в форме кубооктаэд-ра (к. ч. 12).

Структурный тип перовскита CaTiO3
ПЕРОВСКИТ, минерал CaTiO3; иногда содержит изоморфные примеси. Как правило, Са замещается на Се, Ti-на Nb и Та, что приводит к образованию кнопита СеТЮ3 (содержит до 8% оксидов РЗЭ), дизаналита (Са, Na) (Nb, Ti)O3 (до 26% Nb20s) и лопарита (Се, Na, Ca) (Nb, Ti) О, (до 32% оксидов РЗЭ). П. кристаллизуется в ромбич. сингонии; Рстп, а — = 5,3370, Ъ = 7,6438, с = 5,4439, : = 4. Атомы Са (координац. число 12) находятся внутри кубооктаэдрич. полостей каркаса, образованного октаэдрами, к-рые связаны друг с другом вершинами; атомы Ti находятся внутри октаэдров. П. образует псевдокубич. или октаэдрич. кристаллы с плохой спайностью. Твердость П. по минералогии, шкале 5,5-6,0, плотн. 4000-4300 кг/м3. Парамагнитен. Разлагается кипячением с H2S04 и сплавлением с KHSO4. Крупные кристаллы бесцветные или от темно-коричневого до черного цвета. П.
может накапливаться в россыпях. Встречается в основных и ультраосновных породах (кимберлиты, пироксениты и др.), в щелочных породах, пегматитах. Кнопит и дизаналит-характерные минералы карбонатитов. П.-источник Ti, Mb, РЗЭ и ряда др. элементов.
Иногда П. называют хим. соединения (NaNbO3, ВаТЮ3>LiNbO3 и др.), к-рые в кристаллич. состоянии имеют аналогичную структуру. Предполагают, что значит, часть ниж. мантии Земли состоит из т. наз. силикат-перовскита (Mg, Fe) SiO3, к-рый имеет такую же структуру. П. назван в честь Л. А. Перовского.
Р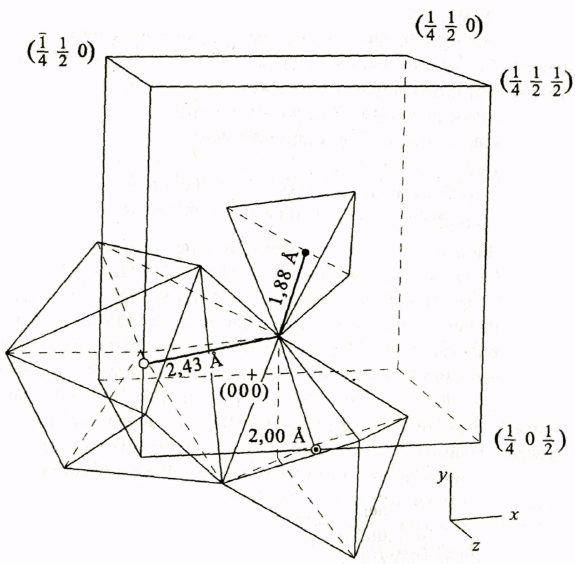 ис.
3.32. Фрагмент кристаллической структуры
феррита-граната иттрия:
ис.
3.32. Фрагмент кристаллической структуры
феррита-граната иттрия:
 •
ионы
Fe3+-
в тетраэдрах; Θ—
ионы Fe3+
в октаэдрах; о - ионы Y
3+
в додекаэдрax.
•
ионы
Fe3+-
в тетраэдрах; Θ—
ионы Fe3+
в октаэдрах; о - ионы Y
3+
в додекаэдрax.
Ионы кислорода находятся в вершинах тетраэдров, октаэдров и додекаэдров рис 3.14 Fe
