
- •1. Химическая коррозия металлов, ее распространенность, опасность, зависимость от различных факторов.
- •2. Защита от химической коррозии.
- •3. Электрохимическая коррозия Ме, ее распространенность, опасность, основные особенности.
- •4.Корризия с водородной и кислородной деполяризацией, их распространенность в строительстве.
- •16. Легирование как метод защиты от электрохимич. Коррозии
- •12. Коррозия бетона и железобетона в жидких средах.
- •17. Обработка коррозионной среды и ингтбиторы коррозии.
- •18.Защитные покрытия в строительстве.
- •19.Электрохимическая защита от коррозии (протекторная и катодная).
1. Химическая коррозия металлов, ее распространенность, опасность, зависимость от различных факторов.
Хим.коррозия-самопроизвольный процесс разрушения Ме под действием сухих газов и неэлектролитов, при которых окисление Ме и восстановление окислителя протекает в виде геторогенной реакции.
Коррозия под действием сухого воздуха- самый распространенный тип.В воздухе основной окислитель, вызывающий коррозию-кислород. 2Ме+О2=2Ме(1). В результате на на поверхности Ме появляются продукты коррозии:оксиды, соли или их смеси. Термодинамическая оценка самопроизвольного протекания этой реакции показывает, что все Ме при обычных тем-рах должны обязательно подвергаться этой реакции.
В хим. коррозии можно выделить 2 этапа:
1.первоначальное окисление- образование оксидной пленки(1-ый слой).Появляются очень быстро.
2.Этап роста оксидной пленки.На этапе очень важно какая пленка продуктов коррозии получится(сплошная,несплошная).
- пленка несплошная
а)для щелочных и щелочно-земельных Ме(Na,Ca,K,Ba) Vok/VMe<1(что очень опасно в практике).
б)W,Mo,V при t>6000С Vok/VMe<2,5-3,5(в данном случае образуется очень объемная пленка, которая со временем “отскакивает”, т.к. не может удержаться на поверхности Ме.
- Большинство Ме дают сплошную пленку(Fe,Al,Cu) 1<Vok/VMe<2.5-3.5-условие сплошности. Скорость коррозии при сплошной пленке зависит от вида пленки(упорядоченная-неупорядоченная,плотная-неплотная).
Упорядоченность пленки зависит от 3 факторов:
температура -невысокая тем-ра t<3000С основная реакция (1) идет с не очень высокой скоростью и оксид получ. упорядоченным,плотным(логариф.закон роста оксидной пленки h=klgτ):при образовании кристалл. решетки оксидов Ме атомы Ме и О2 успевают вставать в узлы решетки и оксид получается упорядоченным.
- t>3000С.При высоких тем-рах скорость реакции (1) очень сильно возрастает и атомы Ме и О2 не успевают встать в узлы решетки. Оксид неупорядочен, с большим кол-вом деффектов(параболический закон роста h2=kτ).При такой высокой тем-ре получается очень толстая пленка-окалина.Тем-ру,при которой образуется окалина-тем-ра окалинообразования(разная для разных Ме).Тем-ра окалнообр-я-характеристика жаростойкости Ме(способность Ме сопротивляться коррозионному воздействию при высоких тем-рах).
Способность Ме сохранятьсвои мех. хар-ки при высоких тем-рах назыв. жаропрочность.
Переход от логариф. к парабол. закону идет постепенно в определенном интервале тем-р.В нем набл. степенной закон hn=kiτ, где n=3,4,5….
-тем-ры близкие к тем-рам плавления. Паралинейный закон роста пленки: скорость коррозии велика и не меняется во времени h=kiτ ( пленка м. плавиться раньше, чем сам Ме и она м. отскакивать.И тогда коррозия станов. более опасна).Для некоторых Ме м. наблюдаться линейный закон роста оксидной пленки (плавиться).
Чем выше тем-ра, тем опаснее хим. коррозия: сварка Ме; термообработка Ме; оборудование, работающее с нагревом.
природа Ме Природа Ме проявляется через сплошную оксидную пленку. Все Ме:- жаростойкие и нежаростойкие.1. Ме, сохраняющие логариф закон роста оксидной пленки до тем-р, близких к тем-рам плавления(Cr,Al,цирконий). 2.Fe,Cu.
влияние состава окруж. среды.
Появление первичных
слоев оксида(быстро), затем пленка(рост
пленки). Он зависит от: прир. Ме,
![]() ,состава
ОС.
,состава
ОС.
Пленка оксидов
может получаться сплошной и не сплошной.
Не сплошная: Na,
K,
Ca,
Ba![]() <1.
Сплошная: W,Mo,V
при
<1.
Сплошная: W,Mo,V
при
![]() >6000
>6000
![]() >2,5-3,5
>2,5-3,5
Пленка тормозит
кор. Сплошную пленку разделяют:
упорядоченная, неупорядоченная. Зависит
от: прир. Ме,
![]() ,состава
ОС.
,состава
ОС.
-


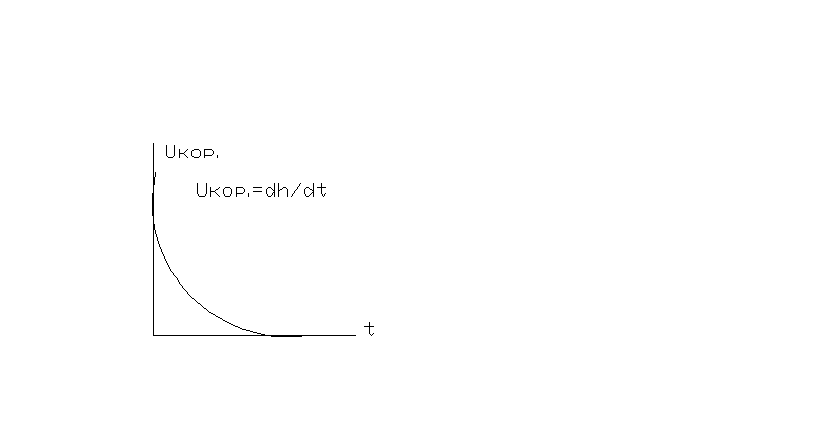 <3000С.
реакция (1) идет с неограниченным ростом
скорости и оксид получается упорядоченным.
<3000С.
реакция (1) идет с неограниченным ростом
скорости и оксид получается упорядоченным.
Хим. кор. при низкой
![]() не
опасна, Ме сам себя защищает за счет
упорядоченной пленки.
не
опасна, Ме сам себя защищает за счет
упорядоченной пленки.
-

 >3000С,
пленка не упорядоченная, не плотная.
>3000С,
пленка не упорядоченная, не плотная.
Uкор.
остается высокой. При такой высокой
![]() получается
очень толстая пленка. Неупорядоченная
– окалина Ме необходимо защищать.
получается
очень толстая пленка. Неупорядоченная
– окалина Ме необходимо защищать.
-

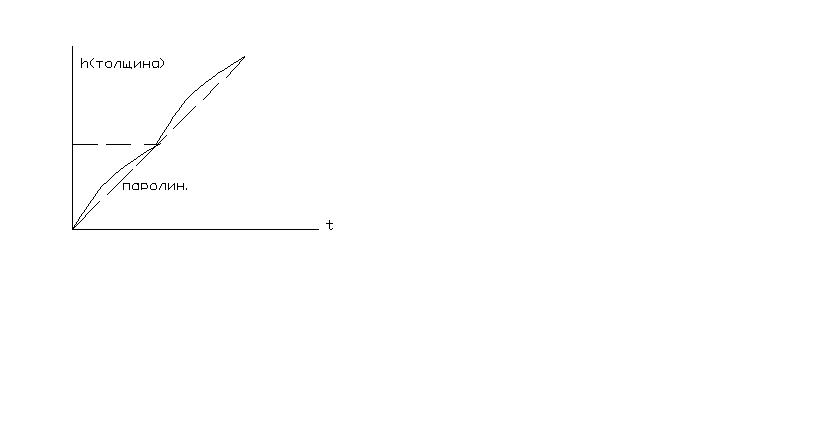
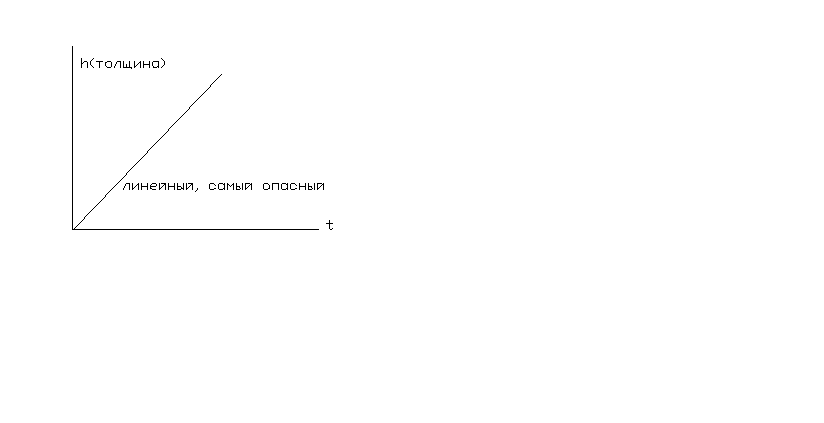 близкая к
близкая к
 плавления.
Пленка может плавиться раньше, чем сам
Ме, может отскакивать, разгоняться
плавления.
Пленка может плавиться раньше, чем сам
Ме, может отскакивать, разгоняться кор.
еще более опасна (паролинейный и линейный
з-ны).
кор.
еще более опасна (паролинейный и линейный
з-ны).
Чем выше![]() ,
тем опаснее хим. кор. Свойства прир. Ме:
жаростойкие – Ме, сохр. логарифмический
з-н роста оксидной пленки (дает упорную
пленку) до
,
тем опаснее хим. кор. Свойства прир. Ме:
жаростойкие – Ме, сохр. логарифмический
з-н роста оксидной пленки (дает упорную
пленку) до![]() ,
близких к
,
близких к
![]() плавления.
Не жаростойкие (большинство).
плавления.
Не жаростойкие (большинство).
Влияние состава ОС (на прим. Fe)
![]()
![]()
![]() калеобразования
стали и чугуна – 3000С
Три осн. направления хим. кор.: воздействие
на Ме жаростойкое легирование; изоляция
Ме от ОС используют жарост. покрытия;
используют защ. атм.
калеобразования
стали и чугуна – 3000С
Три осн. направления хим. кор.: воздействие
на Ме жаростойкое легирование; изоляция
Ме от ОС используют жарост. покрытия;
используют защ. атм.
