
- •Фундаментальные теории и законы химии
- •Основные классы неорганических соединений
- •Название кислоты, структурная формула которой
- •Строение атома
- •Природный хлор содержит два изотопа. Чему равно количество нейтронов ядра одного из изотопов, если известно, что массовое число его 37:
- •Периодический закон и система Менделеева
- •Химическая связь
- •Какое из предложенных обозначений химической связи является валентной схемой:
- •Химическая термодинамика
- •Химическая кинетика. Равновесие
- •Дисперсные системы
- •Растворы
- •Окислительно-восстановительные реакции
- •Электрохимия
- •Полимеры
Строение атома
-
Кто является автором первой модели строения атома, согласно которой атом можно представить в виде положительно заряженной сферы с вкрапленными электронами:
-
Первая частица, входящая в состав атома – электрон, была открыта:
-
Кем предложена планетарная модель строения атома:
-
Ученый, впервые высказавший идею о двойственной природе электрона:
-
Автор волнового уравнения, описывающего вероятность нахождения электрона в некотором объеме пространства:
-
Кто из ученых, рассматривая строение атома, характеризовал электрон корпускулярно-волновым уравнением:
-
Из каких частиц состоит атомное ядро:
-
Наименьший отрицательный заряд, принятый в химии за единицу (-1), несут на себе:
-
Массу, равную массе атома водорода (принятой в химии за единицу), и заряд +1 имеют элементарные частицы:
-
Совокупность мест пространства, в которой наиболее вероятно нахождение электрона, называется:
-
Разновидность атомов одного элемента, отличающиеся величиной атомных масс, называется:
-
Природный хлор содержит два изотопа. Чему равно количество нейтронов ядра одного из изотопов, если известно, что массовое число его 37:
-
Форму атомной орбитали и энергетические подуровни в электронной оболочке атома определяет:
-
Какое квантовое число определяет энергию и размер электронных орбиталей:
-
Формулировка: «В атоме не может быть более двух электронов, обладающих одинаковым набором всех четырех квантовых чисел», выражает:
-
Природный хлор содержит два изотопа. Чему равно количество нейтронов ядра одного из изотопов, если известно, что массовое число его 37:
-
Какая частица состоит из 17 протонов, 20 нейтронов и 17 электронов:
-
Определите массовое число атома алюминия, учитывая, что атом алюминия включает 13 протонов, 14 нейтронов и 13 электронов:
-
Электрические провода для линий электропередач (ЛЭП) изготавливают из алюминия, используя его хорошую электропроводность. Данное свойство объясняется электронным строением атома. Укажите формулу валентного слоя атома алюминия:
-
Неон химически инертен, потому что:
-
Атом элемента имеет электронную конфигурацию внешнего уровня 3s23p5. Для него наиболее свойственно:
-
Электронную формулу атома 1s22s22p63s23p64s23d6 имеет химический элемент:
-
Электронную формулу атома 1s22s22p63s23p64s23d10 имеет химический элемент:
-
Приведите пример соединения, в состав которого входят: анион с конфигурацией 1s22s22p63s23p6 и катион с конфигурацией 1s22s22p6:
-
Приведите пример соединения, в состав которого входят: анион с конфигурацией 1s22s22p6 и катион с конфигурацией 1s22s22p63s23p6:
-
Химический элемент железо имеет электронную формулу:
-
Атом какого элемента в невозбужденном состоянии имеет три неспаренных электрона на 4р-подуровне:
-
На одной р-орбитали не может находиться:
-
Электронная формула внешнего энергетического уровня атома элемента, имеющего формулы газообразного водородного соединения RН3 и высшего оксида R2О5:
-
Электронная формула атома 1s22s22p3. Формулы водородного соединения и высшего оксида этого элемента:
-
Электронная формула атома наиболее активного металла:
-
Символ и формула высшего оксида элемента, электронная формула внешнего и предвнешнего энергетических уровней атома которого 3s23p64s13d5:
-
Выберите два элемента, свойства которых будут повторяться, если конфигурации их внешних энергетических уровней:
-
Выберите химический элемент, который отличается от остальных по химическим свойствам (активности):
-
Атом элемента имеет электронную конфигурацию внешнего энергетического уровня 3s1. Для него наиболее характерно:
-
Сколько протонов и нейтронов в молекуле воды:
-
Сколько протонов и нейтронов в ионе аммония:
-
Ион калия с зарядом +1 содержит электронов, протонов, нейтронов в количестве:
-
Элемент с порядковым номером 13, имеет три внешних электрона в конфигурации:
-
Элемент с порядковым номером 15, имеет пять внешних электронов в конфигурации:
-
Укажите значения всех квантовых чисел для электрона, который находится на 4s-орбитали:
-
На каком энергетическом уровне и на какой орбитали может находиться электрон, для которого n = 3, l = 1:
-
На каком энергетическом уровне, и на какой орбитали может находиться электрон, для которого n = 4, l = 2:
-
Символы химических элементов
 Cl
и
Cl
и
 Cl
отражают разновидность атомов, которая
носит название:
Cl
отражают разновидность атомов, которая
носит название: -
Укажите значения всех квантовых чисел для электрона, который находится на 2р-орбитали:
-
Укажите значения всех квантовых чисел для электрона, который находится на 3d-орбитали:
-
Число валентных электронов у возбужденного атома углерода (С), способных образовать ковалентную химическую связь обменным механизмом:
-
Число валентных электронов у возбужденного атома бора (В), способных образовать ковалентную химическую связь обменным механизмом:
-
Какие изменения происходят с атомным ядром при a-радиоактивном распаде:
-
Схема радиоактивного распада:
 Э
→
Э
→
 Не
+
Не
+
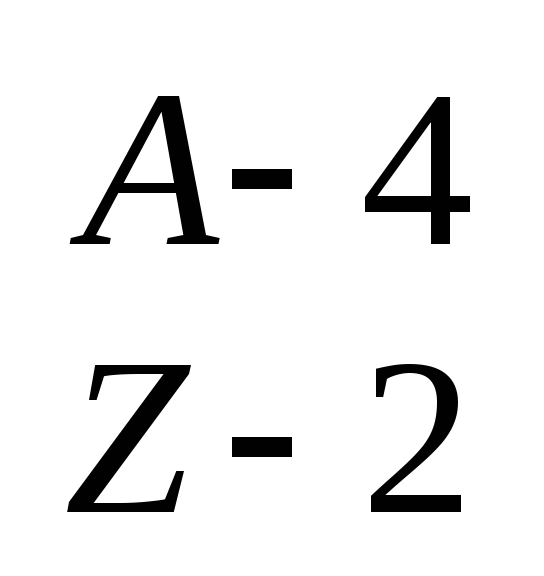 Э′
отражает:
Э′
отражает: -
Изотоп 40К превращается в изотоп 40Са. Какой тип радиоактивного распада при этом реализуется:
-
Изотопы какого элемента образуются при испускании изотопом
 I
I
 частицы:
частицы: -
Тритий – это изотоп:
