Лекция №11. Семестр 1.
-
Уравнение Менделеева - Клапейрона.
-
Барометрическая формула.
-
Распределение Больцмана.
-
Основное уравнение М.К.Т. (уравнение Клаузиуса).
-
Средне-квадратичная скорость молекул газа.
-
Средняя кинетическая энергия поступательного движения молекул газа.
-
Закон распределения молекул идеального газа по скоростям и энергиям теплового движения.
1. Уравнение Менделеева - Клапейрона.
Между параметрами
определяющими состояние газа существует
определенная связь, называемая уравнением
состояния.
Его общий вид:
![]() ,
где каждый из параметров является
функцией 2-х других.
,
где каждый из параметров является
функцией 2-х других.
Объединив закон Бойля-Мариотта и Гей-Люссака, Клапейрон вывел уравнение состояния идеального газа
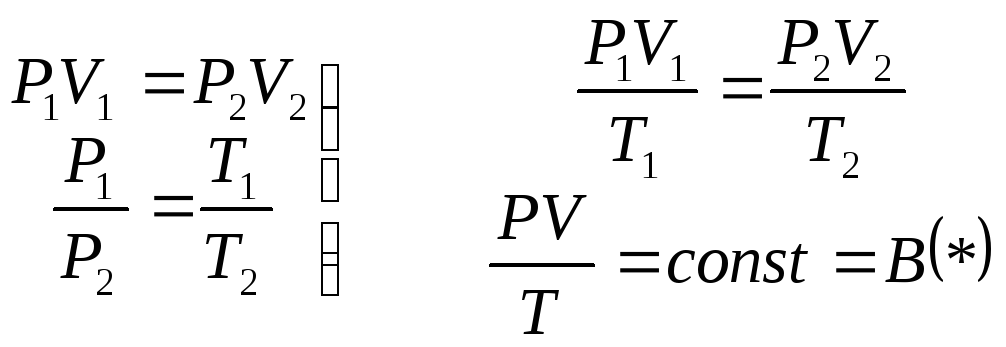 (11.1)
(11.1)
Для данной массы
газа величина
![]() постоянная, различная для различных
газов.
постоянная, различная для различных
газов.
Менделеев объединил
уравнение Клапейрона с законом Авогадро
отнеся уравнение (*) к 1-му молю и использовав
соответственно молярный объемV.
Тогда постоянная
![]() будет одинакова для всех газов и
обозначается
будет одинакова для всех газов и
обозначается
![]() – молекулярная газовая постоянная.
– молекулярная газовая постоянная.
![]() (112.2)
(112.2)
![]() и
и
![]() – давление, молярный объем и абсолютная
температура газа. Физический
смысл
– давление, молярный объем и абсолютная
температура газа. Физический
смысл
![]() – универсальная
газовая постоянная,
численно равная работе совершенной 1
молем идеального газа при изобарном
повышении температуры на 1С.
– универсальная
газовая постоянная,
численно равная работе совершенной 1
молем идеального газа при изобарном
повышении температуры на 1С.
![]()
Определяется из уравнения (11.2) при нормальных условиях:
![]()
![]()
![]() и
и
![]()
Для произвольной
массы газа
![]() с молярной массой
с молярной массой
![]() и объемом
и объемом
![]() уравнение Менделеева - Клапейрона имеет
вид:
уравнение Менделеева - Клапейрона имеет
вид: ![]() ,
(11.3)
,
(11.3)
так как
![]() ;
;
![]() , (11.4)
, (11.4)
С учетом того что
![]() – концентрация,
– концентрация,
![]()
![]() ,
тогда
,
тогда
![]() ;
;
![]() –
представляет собой универсальную
газовую постоянную, отнесенную к 1
молекуле.
–
представляет собой универсальную
газовую постоянную, отнесенную к 1
молекуле.
Тогда ![]() (11.5)
(11.5)
Давление идеального
газа при данной
![]() прямо
пропорционально концентрации его
молекул. Из 12.5
прямо
пропорционально концентрации его
молекул. Из 12.5
![]() ,
то есть, при одинаковых
,
то есть, при одинаковых
![]() и
и
![]() все газы содержат в единице объема
одинаковое число молекул.
все газы содержат в единице объема
одинаковое число молекул.
Число молекул
содержащихся в
![]() газа при нормальных условиях называется
числом
Лошмидта.
газа при нормальных условиях называется
числом
Лошмидта. ![]() .
.
Уравнение Менделеева-Клайперона является обобщением экспериментальных газовых законов и включает их в качестве частных случаев.
2. Барометрическая формула.
Из-за хаотичного теплового движения молекулы газа занимают весь предоставленный объем, равномерно заполняя его, в случае, если на молекулы газа не действуют внешние силы. Атмосферный воздух земли не ограничен стенками, но не разлетается – этому препятствует сила земного притяжения.
С другой стороны
при отсутствии теплового движения (![]() )
каждая отдельная молекула газа должна
была бы падать вниз – они скопились бы
у поверхности земли, где их потенциальная
энергия минимальна.
)
каждая отдельная молекула газа должна
была бы падать вниз – они скопились бы
у поверхности земли, где их потенциальная
энергия минимальна.
Благодаря борьбе этих двух противоположных тенденций установлено подвижное равновесие, при котором – концентрация молекул воздуха у поверхности земли максимальна и постепенно уменьшается с высотой.
Так как
![]() ,
следовательно, по мере подъема над
уровнем земли и уменьшением концентрации
будет так же уменьшаться и атмосферное
давление.
,
следовательно, по мере подъема над
уровнем земли и уменьшением концентрации
будет так же уменьшаться и атмосферное
давление.
Зависимость
давления от высоты р(h)
– называется Барометрической
формулой:
![]() (11.6)
(11.6)
Отсчет высоты идет
от уровня моря, где
![]() считается нормальным, поэтому можно
записать
считается нормальным, поэтому можно
записать ![]() (11.7)
(11.7)
По этой формуле можно определить атмосферное давление в зависимости от высоты, или, измерив, давление, найти высоту.
![]() – молярная масса;
– молярная масса;
![]() – ускорение
свободного падения;
– ускорение
свободного падения;
![]() – универсальная
газовая постоянная;
– универсальная
газовая постоянная;
![]() – абсолютная
температура;
– абсолютная
температура;
![]() – нормальное
давление.
– нормальное
давление.
Из (12.5) следует, что давление с высотой убывает тем быстрее, чем тяжелее газ.
График зависимости:
|
|
Определим высоту, на которой давле |
|
ние газа падает вдвое h1/2)=1/20.Подставим это в (12.7) и получим
|
|
|
то есть при подъеме на высоту 6 км |
|
|
над
уровнем моря,
|
|
|
половины от первоначального значе- |
|
|
ния. При подъеме на 12 км давление |
|
|
упадет
до
|
Измеряя барометром давления в горах можно согласно формуле (12.7) определить высоту места над уровнем моря. На этом принципе основаны устройства авиационных высотомеров - альтиметров.