
Федеральное агентство по образованию
Государственное образовательное учреждение
высшего профессионального образования
Уфимский государственный авиационный технический университет
Виды дисперсных систем Методические указания
к лабораторной работе по курсу “Физическая и коллоидная химия”
для студентов специальностей 280101 “Безопасность жизнедеятельности в
техносфере”, 280103 “Защита в чрезвычайных ситуациях”,
направления 280200 “Защита окружающей среды”
Уфа 2010
Работа 1. Получение и свойства эмульсий
Цель работы. Изучение методов получения эмульсий и исследование их устойчивости.
Краткие теоретические положения.
Эмульсия
– микрогетерогенная система, состоящая
из двух взаимно нерастворимых жидкостей,
распределенных одна в другой в виде
капелек. Жидкость,
взвешенная в виде капелек, называется
дисперсной фазой. Жидкость, в которой
распределена дисперсная фаза, называется
дисперсионной средой. Условно эмульсии
обозначают в виде дроби
![]() ,
где в числителе указано агрегатное
состояние фазы (жидкость 1),
а
в знаменателе – агрегатное состояние
среды (жидкость 2).
,
где в числителе указано агрегатное
состояние фазы (жидкость 1),
а
в знаменателе – агрегатное состояние
среды (жидкость 2).
Эмульсии широко распространены в природе (молоко, млечный сок растений и т.д.), их легко изготовить также искусственным путем (смазки, маргарин, косметические кремы и т.д.).
Эмульсии обычно классифицируют по двум признакам:
1) по концентрации дисперсной фазы:
– разбавленные (объем дисперсной фазы не выше 0,1%);
– концентрированные (объем дисперсной фазы 0,1% – 74%);
– высококонцентрированные (объем дисперсной фазы более 74%).
2) по полярности дисперсной фазы и дисперсионной среды:
– Эмульсии I рода (прямые). Эмульсии неполярной или слабо полярной жидкости распределены в полярной. Например, эмульсия масла в воде – М/В.
– Эмульсии II рода (обратные). Эмульсии полярной жидкости в неполярной, например, вода в масле – В/М.
Эмульсии, подобно другим дисперсным системам, могут быть получены двумя путями: конденсацией паров одной жидкости в другой или диспергированием. Наибольшее распространение получил второй способ, при котором диспергирование жидкости производится размешиванием, встряхиванием или растиранием. Хороший способ получения высокодисперсных эмульсий – диспергирование с помощью ультразвука.
Специфическим свойством эмульсий является обращение фаз эмульсии – изменение типа эмульсии, т.е. дисперсная фаза становится дисперсионной средой, а дисперсионная среда – дисперсной фазой (переход М/В → В/М или обратно).
Большинство эмульсий являются термодинамически неустойчивыми. Для их стабилизации используются специальные вещества – эмульгаторы. В качестве эмульгаторов применяют неорганические электролиты, коллоидные ПАВ, ВМС, высокодисперсные порошки.
Многие эмульгаторы являются поверхностно-активными веществами, т.е. понижают поверхностное натяжение на границе обеих жидкостей. Для получения концентрированных эмульсий необходимо введение эмульгатора в довольно больших количествах. Эмульгатор образует механически прочную защитную оболочку, препятствующую слиянию капель. В некоторых случаях защитные оболочки образуются частицами высокодисперсных твердых порошков.
Для характеристики эмульгатора весьма существенно его отношение к обеим жидкостям, образующим эмульсию. Вещества, растворимые в воде и нерастворимые в другой фазе, являются хорошими эмульгаторами для эмульсий типа м/в. Примером такого эмульгатора может служить олеат натрия или другие мыла щелочных металлов.
Эмульгаторами для систем типа В/М являются мыла металлов Са, Zn, A1 и др., которые плохо растворимы в воде и хорошо растворимы в углеводородах и маслах.
Различие между эмульгаторами обоих типов можно объяснить тем, что обе поверхности адсорбированной пленки эмульгатора по-разному смачиваются водой и маслом. Стремление сократиться у данной поверхности будет тем больше, чем больше поверхностное натяжение. Так как охватывающая поверхность больше, чем охватываемая, то, очевидно, что при прочих равных условиях в шарики соберется та жидкость, которая хуже растворяет и слабее взаимодействует с эмульгатором (рисунок 1).
а б
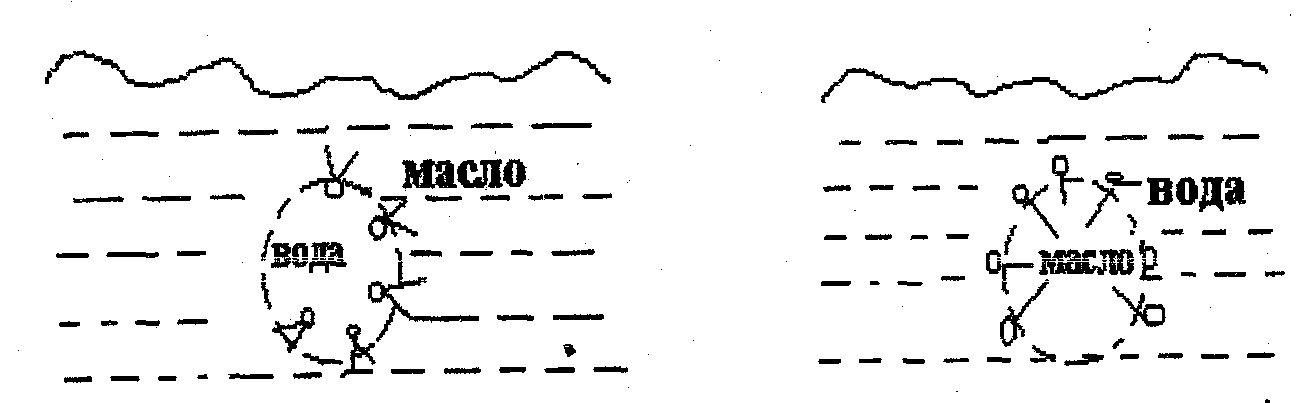
Рисунок 1 - Схема расположения молекул эмульгатора на поверхности капелек эмульсий
а – эмульсия типа В/М, эмульгатор олеат кальция;
б – эмульсия типа М/В, эмульгатор олеат натрия
В эмульсиях типа вода в масле полярные части молекул мыла щелочного металла погружены в капли эмульгированной воды, а углеводородная часть – в дисперсионную среду – масло (рис. 1, а). В эмульсиях масло в воде молекулы мыла располагаются так, что их полярные части обращены в дисперсионную среду, которой является вода (рис. 1, б).
Выяснение типа эмульсии можно провести следующими способами:
-
Эмульсии М/В легко смешиваются с водой, но не с маслом, а эмульсии В/М смешиваются с маслом, но не смешиваются с водой.
-
Эмульсии М/В хорошо окрашиваются водорастворимыми красителями, а эмульсии обратного типа – красителями, растворимыми в масле.
-
При нанесении капли эмульсии на парафиновую поверхность капля растекается, если дисперсионной средой является масло, и не растекается, если таковой служит вода.
На практике иногда необходимо выделить из эмульсии ее составные части, т.е. разрушить эмульсию (деэмульгация), для чего применяют следующие методы:
– седиментация – всплывание или оседание капель дисперсной фазы (например, отделение сливок от молока);
– коалесценция (полное разрушение эмульсий, когда в чистом виде выделяются отдельные компоненты);
– химические методы (применяются химические вещества – деэмульгаторы);
– термические методы (нагрев, замораживание);
– электрические методы.
Приборы и реактивы.
-
Пипетки емкостью 1 см3.
-
Пробирки градуированные.
-
Водный раствор проксанола (2%-ный).
-
Бензин.
-
Масло растительное.
-
Бура Na2B4О7∙10 Н2О.
-
Дистиллированная вода.
Порядок выполнения работы.
1. Наливают в четыре пробирки дистиллированную воду, примерно половину их объема.
2. В первую пробирку добавляют примерно 0,5 см3 бензина, закрывают ее пробкой; несколько раз энергично встряхивают и ставят в штатив.
3. Во вторую пробирку добавляют примерно 0,5 см3 растительного масла, закрывают пробкой, встряхивают и ставят в штатив.
4. В третью пробирку добавляют 5–10 капель 2%-ного раствора проксанола, затем ~ 0,5 см3 бензина, встряхивают и ставят в штатив.
5. В четвертую пробирку добавляют ~ 0,2 г буры Na2B4О7∙10 Н2О, встряхивают до полного растворения соли, затем добавляют 0,5 см3 растительного масла, энергично встряхивают и ставят в штатив.
6. Отмечают скорость образования и расслоения эмульсии в каждой пробирке.
7. Анализируют результаты, формулируют выводы.
