
- •Опд.Ф.02.06 теплотехника
- •Методическое пособие
- •Для решения задач по разделу «Техническая термодинамика»
- •Специальности:
- •Предисловие
- •Условные обозначения
- •1 Основы технической термодинамики
- •Задачи к разделу 1.
- •2 Смеси идеальных газов
- •2.1 Массовый состав смеси
- •2.2 Объемный состав смеси
- •3 Теплоемкость газов
- •4 Термодинамические процессы газов
- •5 Водяной пар. Диаграмма h,s водяного пара. Исследование паровых процессов по диаграмме h,s
- •Теоретический паросиловой цикл (цикл Ренкина).
- •Влажный воздух
- •Библиографический список
5 Водяной пар. Диаграмма h,s водяного пара. Исследование паровых процессов по диаграмме h,s
Вода и. водяной пар широко применяются в энергетике, в отоплении, вентиляции, горячем водоснабжении.
Водяной пар - реальный газ. Он может быть влажным, сухим насыщенным и перегретым. Уравнения состояния реальных тазов сложны, поэтому в теплотехнических расчетах предпочитают использовать таблицы и диаграммы. Особое значение для технических расчетов процессов с водяным паром имеет h,s -диаграмма водяного пара.
В диаграмме h,S нанесена (рис. 5.1, ) верхняя пограничная кривая (степень сухости пара X=1) соответствующая сухому насыщенному пару. Выше этой кривой располагается область перегретого пара.

а) б)
Рисунок 5.1 Диаграмма h,S водяного пара
Ниже влажного насыщенного пара. В область влажного насыщенного пара нанесены кривые сухости ( X=0,95; Х=0,90; X=0.85 и т.д.)
В координатных, осях h,S (рис.5.1..) нанесены кривые простейших процессов р=сonst (изобары); v= сonst (изохоры); t =сonst (и термы); любая вертикальная линия (рис.5.2.) изображает адиабатный процесс (S=const ).
В области влажного насыщенного пара изотермы (t =сonst )совпадают с кривыми изобары (р=сonst), так как парообразование происходит при постоянном давлении и при постоянной температуре. На верхней пограничной кривой направление изотермы меняется и в пограничной кривой направление изотермы меняется и области перегретого пара изотермы отклоняются вправо и не совпадают с изобарами.
Практически
применяется часть диаграммы h,S
, когда X![]() 0,5
, которая
заключена в рамку. Эта часть диаграммы
приведена в приложении и на рис.5.2.
0,5
, которая
заключена в рамку. Эта часть диаграммы
приведена в приложении и на рис.5.2.
Состояние перегретого пара на диаграмме h,S определяется двумя параметрами (р1 и t1 или р1 и v1 ), а влажного насыщенного пара - одним параметром и степенью сухости пара Х. По 2 заданным параметрам р1 и t1 в области перегретого пара находим точку I (рис. 5.2.), соответствующую заданному состоянию водяного пара. Для этого состояния из диаграммы можно найти все другие параметры (h1,s1,v1).
З![]() начение
внутренней анергии подсчитывается по
формуле
начение
внутренней анергии подсчитывается по
формуле
5.1
Зная вид термодинамического процесса, двигаются по нему до пересечения с заданным конечным параметром и находят на диаграмме конечное состояние пара..Определив параметры коночного состояния, можно рассчитывать показатели процесса (работу, теплоту, изменение параметров)
 Изменение
внутренней энергии
Изменение
внутренней энергии
![]() и работу в любом процессе подсчитывают
по формулам
и работу в любом процессе подсчитывают
по формулам
Рассмотрим основные задачи, решаемые по h,S диаграмме.
Изохорный процесс (v= const)
Количество теплоты, участвующая в процессе определяется по формуле 5.2,. для определения изменения внутренней энергии.
Работа изохорного процесса равна нулю.
Изобарный процесс (р=сonst), количество теплоты, участвующая в процессе определяется по формуле:
![]()
Изменение внутренней энергии по формуле 5.2
![]() Работу
изобарного процесса можно сравнить
Работу
изобарного процесса можно сравнить
5.5
или по формуле 5.3
Изотермный процесс (t =сonst ).
Теплоту и работу процесса находят по формуле:
![]() 5.6
5.6
Адиабатный
процесс
![]() .
На рис. 5.2. представлен адиабатный
процесс, протекающий без теплообмена
с внешней среда В адиабатном процессе
энтропия не изменяется и очень часто
этот процесс называется изоэнтропным.
.
На рис. 5.2. представлен адиабатный
процесс, протекающий без теплообмена
с внешней среда В адиабатном процессе
энтропия не изменяется и очень часто
этот процесс называется изоэнтропным.
Работа
процесса происходит за счет изменения
внутренней
![]() .
.
П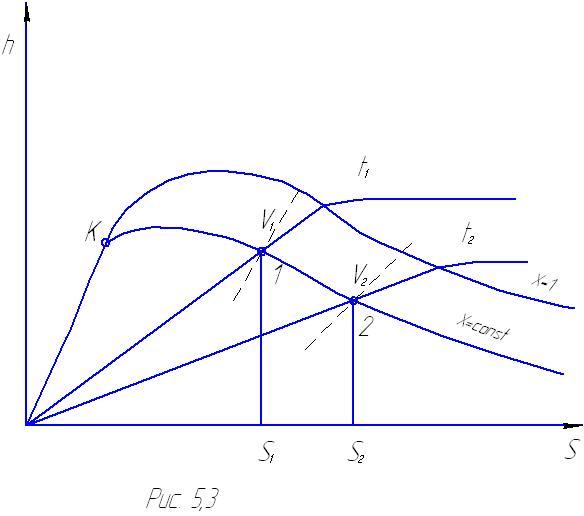 роцесс
при постоянной степени сухости (Х=сonst)
решается также по диаграмме h,S
(рисунок5.2)
роцесс
при постоянной степени сухости (Х=сonst)
решается также по диаграмме h,S
(рисунок5.2)
Приблизительное количество определяется по формуле
![]() 5.7
5.7
Изменение внутренней энергии в процессе находят обычным способом по формуле 5.2
Работа процесса определяется по формуле 5.3.
Рисунок 5.2 Диаграмма h,S водяного пара
