
- •Комплексные соединения
- •Определение комплексных соединений
- •Основные понятия
- •Номенклатура комплексных соединений
- •Одноядерные комплексы
- •Классификация комплексных соединений
- •Катионные комплексы
- •Анионные комплексы
- •Нейтральные комплексы
- •Катионно-анионные комплексы
- •Циклические комплексы (хелаты)
- •Изомерия комплексных соединений
- •Ионизационная изомерия
- •Солевая изомерия
- •Координационная изомерия
- •Геометрическая изомерия (цис-, транс-изомерия)
- •Хлороамминдиэтилен диаминкобальта(III).
- •Природа химической связи в комплексных соединениях Метод валентных связей
- •Теория кристаллического поля
- •Теория поля лигандов
- •Свойства комплексных соединений Окраска комплексных соединений
- •Магнитные свойства комплексных соединений
- •Равновесия в растворах комплексных соединений
- •Устойчивость комплексных соединений
- •Кинетика и механизм реакций обмена лигандов
- •Кислотно - основные свойства комплексных соединений
- •Окислительно-восстановительные свойства комплексных соединений
- •Длины волн спектра и соответствующие им окраски

Гем - комплекс протопорфирина с железом является важнейшим хелатным комплексом железа(II)

Витамин В12(цианкобаламин).
Комплексные соединения
(лекции)
Определение комплексных соединений
Основатель координационной теории строения комплексных соединений А.Вернер делил все химические соединения на соединения первого порядка, построенные согласно классической теории валентности (простые или атомные соединения типа HCl, H2O, NH3, CH4, CoCl3) и соединения высшего порядка (или молекулярные). Соединения высшего порядка, согласно А. Вернеру, представляют собой продукты сочетания соединений первого порядка, например:
NH3 + HCl = [NH4]Cl.
KF + BF3 = K[BF4].
AgCl + 2NH3 = [Ag(NH3)2] Cl.
CrCl3 + 6H2O = [Cr( H2O)6] Cl3.
Fe(CN)3 + 3KCN = K3[Fe(CN)6].
Молекулярные соединения (соединения высшего порядка) называются комплексными или координационными соединениями.
Различить комплексные и простые соединения иногда очень трудно. В зависимости от условий одно и то же соединение можно рассматривать и как простое, и как комплексное. Так, галогениды щелочных и щелочно-земельных металлов, которые в газообразном состоянии существуют в виде отдельных молекул, в твёрдом состоянии ассоциированы. В растворе эти соединения диссоциируют на простые ионы. Хлорид натрия в кристаллическом состоянии следует рассматривать как высокомолекулярное комплексное соединение (NaCl)n. Вода
в парообразном состоянии отвечает формуле H2O, а в жидком состоянии - формуле (H2O)n. И с точки зрения химической связи различие между простыми и комплексными частицами обычно отсутствует.
Из-за огромного разнообразия комплексных соединений и их характерных свойств чёткого определения «комплексное соединение» не существует. Но поскольку в лабораторной практике химики чаще всего имеют дело с соединениями в твёрдом или растворённом состояниях, то
комплексными или координационными соединениями принято называть соединения, в узлах кристаллической решётки которых находятся комплексы, способные к самостоятельному существованию в растворе.
Основные понятия
Согласно координационной теории в молекуле любого комплексного соединения различают центральный атом или ион- комплексообразователь, вокруг которого в непосредственной близости координировано некоторое число противоположно заряженных ионов или электронейтральных молекул, называемых лигандами. Центральный атом- комплексообразователь и лиганды образуют внутреннюю координационную сферу. Ионы, не разместившиеся во внутренней сфере, составляют внешнюю координационную сферу. При написании формул комплексных соединений центральный атом вместе с лигандами заключают в квадратные скобки. Внутренняя сфера комплекса в значительной степени сохраняет стабильность при растворении, а ионы, находящиеся во внешней сфере, легко отщепляются. Внешняя сфера комплексного соединения может состоять из катионов, если комплексный ион является анионом, или анионов, если комплексный ион является катионом, и может совсем отсутствовать, если заряд комплекса равен нулю. Заряд комплексного иона равен алгебраической сумме зарядов комплексообразователя и лигандов. При расчёте заряды молекул принимаются равными нулю.

Общее число электродонорных центров лигандов (атомов или π-связей), координированных центральным атомом, называется координационным числом. В качестве центрального атома-комплексообразователя могут выступать практически любые химические элементы, но наиболее прочные комплексы образуют d-элементы.
K4[Fe(CN)6] = 4K+ + [Fe(CN)6]4-
Выше были рассмотрены одноядерные комплексы. Во внутренней сфере такого комплекса находится один центральный атом-комплексообразователь и некоторое число лигандов, при наличии же во внутренней сфере нескольких центральных атомов это будет многоядерный комплекс. Например, [PdCl6]2- - одноядерный комплекс, а [Os3(CO)12] – трёхядерный.
Лиганды могут координироваться центральным атомом за счёт образования σ-,(σ,π)- или только многоцентровых π-связей. Соответственно их называют σ-,(σ,π)- и π-лигандами. Если лиганды соединяются с центральным атомом одним атомом-донором, это монодентатные лиганды. К ним относятся анионы Cl,Br, S2,CN, SCN, нейтральные молекулы H2O,NH3 и многие другие. Лиганды, которые могут соединяться с центральным атомом-комплексообразователем в зависимости от условий различными донорными атомами, называются амбидентатными. Например, у лиганда –SCN- донорным атомом может быть либо S,либо N.
Для комплексных соединений с монодентатными лигандами координационное число центрального атома равно числу лигандов. Например, в комплексном соединении K2[PtCl6] центральным атомом-комплексообразователем является платина в степени окисления +4, во внутреннюю сферу входят 6 анионов хлора. Координационное число центрального атома равно 6. Комплексный ион представляет собой анион, заряд которого равен +4 - 6= -2.Во внешней сфере находятся 2 иона калия. В комплексном соединении [Pt(NH3)4Cl2]Cl2 центральным атомом - комплексообразователем также является платина в степени окисления +4, во внутреннюю сферу входят 4 молекулы аммиака,2 аниона хлора. Координационное число центрального атома также равно 6. Комплексный ион представляет собой катион, заряд которого равен +4 +0 –2 = +2. Во внешней сфере находятся 2 иона хлора.
В комплексном ионе лиганды могут быть связаны с центральным атомом посредством не только одного, но и нескольких атомов. Число донорных центров лиганда, образующих координационные связи с центральным атомом (т.е. число σ-связей, формируемых одним σ- или (σ,π)-лигандом с центральным атомом), называется дентатностью (от лат. dentalus – имеющий зубы). Для π-лигандов понятие дентатность не применяется.
Этилендиамин (сокращённое обозначение en), двухзарядные ионы C2O42-, S2O32-,CO32-,SO42- и им подобные относятся к бидентатным лигандам. Примеры комплексных соединений Со3+ с этими лигандами:
Na3[Co(C2O4)3], [Co(en)3](NO3)3, Ca3[Co(S2O3)3]2.
Лиганды могут быть также тридентатными, тетрадендатными, … полидентатными. Для комплекса с полидентатными лигандами координационное число равно числу таких лигандов, умноженному на дентатность.
Лиганды, координирующиеся через два или более донорных атомов к одному центральному атому, образуя один или несколько гетероциклов, называются хелатными. Замыкание хелатного цикла такими лигандами называется хелатированием (хелатообразованием), например, катион бисэтилендиаминмедь(II)
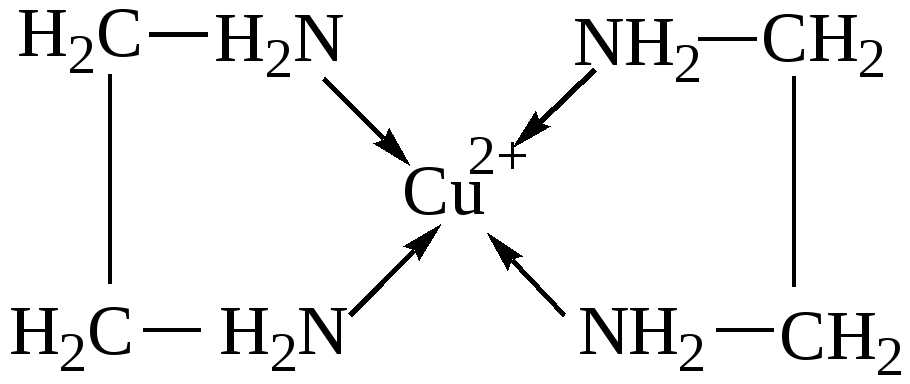
Существуют многоядерные комплексы, в которых центральные атомы непосредственно связаны меду собой. Такие комплексы называются кластерами, например: [(CO)5Mn-Mn(CO)5].
