
- •Методологія наукових досліджень методичні рекомендації до виконання розрахункової роботи
- •Завдання розрахункової роботи
- •А Розрахунок кінетичних параметрів хімічної реакції в потоці газу
- •Б Розрахунок кінетичних параметрів топохімічної реакції
- •В Розрахунок регресійної моделі за результатами дробового експерименту
- •Висновки
- •Список використаної літератури
- •Список рекомендованої літератури
- •Захист розрахункової роботи
- •Додаток а Зразок титульного листа
- •Додаток б
Міністерство освіти і науки, молоді та спорту України
Національний технічний університет України
«Київський політехнічний інститут»
ЕЛЕКТРОННЕ НАВЧАЛЬНЕ ВИДАННЯ
Методологія наукових досліджень методичні рекомендації до виконання розрахункової роботи
для студентів хіміко-технологічного факультету.
Напрям підготовки: 6.051301 – Хімічна технологія.
Професійна спрямованість «Хімічні технології неорганічних речовин»
Київ НТУУ «КПІ»
2011
Зміст
Вступ 3
Завдання розрахункової роботи 4
А Розрахунок кінетичних параметрів хімічної реакції в потоці газу 4
Б Розрахунок кінетичних параметрів топохімічної реакції 7
В Розрахунок регресійної моделі за результатами дробового експерименту 8
Висновки 11
Список використаної літератури 11
Захист розрахункової роботи 12
Додаток А 14
Додаток Б 15
Вступ
Виконання розрахункової роботи (РР) сприятиме засвоєнню і поглибленому вивченню кредитного модуля «Методологія наукових досліджень". Дані методичні рекомендації визначають порядок виконання, обсяг і зміст РР та порядок її захисту.
Мета роботи: виконання кінетичних розрахунків хімічної реакції в потоці і топохімічної реакції, обробка результатів дробового факторного експерименту.
Структура пояснювальної записки (обсяг до 10 с.): титульний аркуш; завдання; основна частина з трьох розділів; висновки, список використаної літератури.
Завдання розрахункової роботи
Вид завдання і номер варіанта N визначає викладач.
А Розрахунок кінетичних параметрів хімічної реакції в потоці газу
Для кінетичного
рівняння
![]() ,
що описує перебіг реакції А
+ В
продукти, визначити сумарний порядок
реакції
,
що описує перебіг реакції А
+ В
продукти, визначити сумарний порядок
реакції
![]() ,
порядки реакції за компонентами (nA,
nB) та константу швидкості
k за даними, що одержані
на проточній установці ідеального
витиснення. Варіанти вихідних даних
наведені у таблицях.
,
порядки реакції за компонентами (nA,
nB) та константу швидкості
k за даними, що одержані
на проточній установці ідеального
витиснення. Варіанти вихідних даних
наведені у таблицях.
Таблиця
А1 – Залежність ступеня перетворення
х від часу
![]() (с)
(с)
|
№ |
Концентраційні параметри |
Ступінь перетворення х (частка) |
||||||
|
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
|||
|
|
|
Час, с |
||||||
|
1 |
0,2 |
1,5 |
0,5128/N |
0,8333/N |
1,2121/N |
1,6667/N |
2,2222/N |
2,9167/N |
|
2 |
0,5 |
1,5 |
0,2051/N |
0,3333/N |
0,4848/N |
0,6667/N |
0,8889/N |
1,1667/N |
|
3 |
0,2 |
2,5 |
0,1739/N |
0,2727/N |
0,381/N |
0,5/N |
0,6316/N |
0,7778/N |
Таблиця
А2 – Залежність ступеня перетворення
х від часу
![]() (с)
(с)
|
№ |
Концентраційні параметри |
Ступінь перетворення х (частка) |
|||||||||||
|
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
||||||||
|
|
|
Час, с |
|||||||||||
|
1 |
0,2 |
1,5 |
0,8004/N |
1,3353/N |
2,0067/N |
2,8768/N |
4,0546/N |
5,7536/N |
|||||
|
2 |
0,5 |
1,5 |
0,3201/N |
0,5341/N |
0,8026/N |
1,1507/N |
1,622/N |
2,3014/N |
|||||
|
3 |
0,2 |
2,5 |
0,4658/N |
0,7628/N |
1,1215/N |
1,5666/N |
2,1395/N |
2,9182/N |
|||||
Таблиця
А3 – Залежність ступеня
перетворення х від часу
![]() (с)
(с)
|
№ |
Концентраційні параметри |
Ступінь перетворення х (частка) |
||||||
|
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
|||
|
|
|
Час, с |
||||||
|
1 |
0,2 |
5 |
0,2255/N |
0,3625/N |
0,5224/N |
0,7136/N |
0,9501/N |
1,2587/N |
|
2 |
0,5 |
5 |
0,1426/N |
0,2293/N |
0,3304/N |
0,4513/N |
0,6009/N |
0,796/N |
|
3 |
0,2 |
10 |
0,1586/N |
0,2542/N |
0,3652/N |
0,4971/N |
0,6595/N |
0,8699/N |
Таблиця
А4 – Залежність ступеня
перетворення х від часу
![]() (с)
(с)
|
№ |
Концентраційні параметри |
Ступінь перетворення х (частка) |
||||||
|
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
|||
|
|
|
Час, с |
||||||
|
1 |
0,2 |
1,5 |
2,88/N |
5,02/N |
7,95/N |
12,10/N |
18,32/N |
28,37/N |
|
2 |
0,5 |
1,5 |
0,46/N |
0,80/N |
1,27/N |
1,94/N |
2,93/N |
4,54/N |
|
3 |
0,2 |
2,5 |
0,97/N |
1,63/N |
2,47/N |
3,56/N |
5,03/N |
7,13/N |
Таблиця
А5 – Залежність ступеня
перетворення х від часу
![]() (с)
(с)
|
№ |
Концентраційні параметри |
Ступінь перетворення х (частка) |
||||||
|
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
|||
|
|
|
Час, с |
||||||
|
1 |
0,2 |
1,5 |
0,338/N |
0,543/N |
0,787/N |
1,073/N |
1,427/N |
1,874/N |
|
2 |
0,5 |
1,5 |
0,214/N |
0,344/N |
0,498/N |
0,679/N |
0,902/N |
1,185/N |
|
3 |
0,2 |
2,5 |
0,197/N |
0,311/N |
0,441/N |
0,588/N |
0,758/N |
0,964/N |
Таблиця
А6 – Залежність ступеня
перетворення х від часу
![]() (с)
(с)
|
№ |
Концентраційні параметри |
Ступінь перетворення х (частка) |
||||||
|
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
|||
|
|
|
Час, с |
||||||
|
1 |
0,2 |
1,5 |
0,1259/N |
0,0989/N |
0,0722/N |
0,0491/N |
0,0336/N |
0,0093/N |
|
2 |
0,5 |
1,5 |
0,3128/N |
0,2464/N |
0,1816/N |
0,1233/N |
0,0829/N |
0,0259/N |
|
3 |
0,2 |
2,5 |
0,1259/N |
0,0989/N |
0,0722/N |
0,0491/N |
0,0336/N |
0,0093/N |
Таблиця
А7 – Залежність ступеня
перетворення х від часу
![]() (с)
(с)
|
№ |
Концентраційні параметри |
Ступінь перетворення х (частка) |
||||||
|
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
|||
|
|
|
Час, с |
||||||
|
1 |
0,2 |
3 |
2,162/N |
3,786/N |
6,035/N |
9,307/N |
14,418/N |
23,302/N |
|
2 |
0,5 |
4 |
0,257/N |
0,448/N |
0,709/N |
1,085/N |
1,665/N |
2,662/N |
|
3 |
0,2 |
5 |
1,278/N |
2,218/N |
3,499/N |
5,332/N |
8,143/N |
12,938/N |
Таблиця
А8 – Залежність ступеня
перетворення х від часу
![]() (с)
(с)
|
№ |
Концентраційні параметри |
Ступінь перетворення х (частка) |
||||||
|
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
|||
|
|
|
Час, с |
||||||
|
1 |
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
Послідовність виконання розрахунків:
-
заповнити відповідну таблицю (згідно завдання) з точністю до третього знаку після коми;
-
побудувати графіки
 .
.
Розрахунок швидкості реакції в окремих точках
-
використати програму кафедри ТНР та ЗХТ “Расчет скоростиVBA.xls” для розрахунку швидкостей для 3-х кривих і апроксимувати залежність
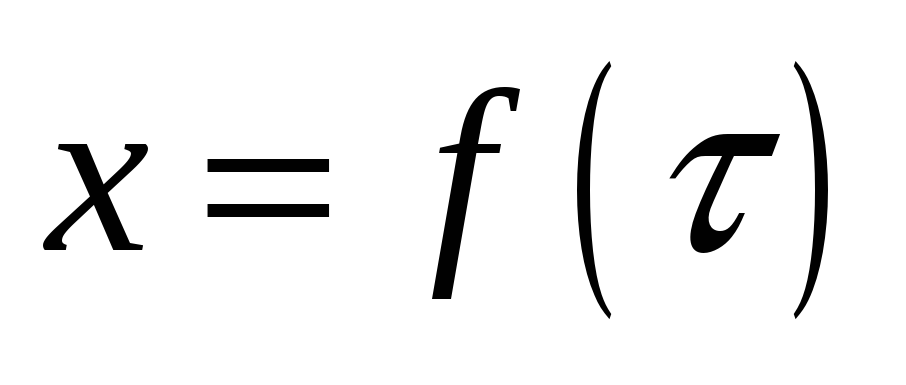 поліномом третього степеня;
розрахувати значення швидкостей для
точок з Х=0,2; 0,3; 0,4; 0,5; 0,6 (остання
точка не враховується як ненадійна).
поліномом третього степеня;
розрахувати значення швидкостей для
точок з Х=0,2; 0,3; 0,4; 0,5; 0,6 (остання
точка не враховується як ненадійна).
Розрахунок кінетичних параметрів
-
використати кафедральну програму ТНР та ЗХТ “Расчет кинетичпараметровVBA.xls” для розрахунку кінетичних параметрів. Дружній інтерфейс програми сприяє швидкому вводу вихідних даних і отриманню результатів розрахунку.
-
інтегрувати отримане кінетичне рівняння при знайдених і округлених значеннях порядків, розв’язати його відносно
 при заданих значеннях
при заданих значеннях
 ,
х та
,
х та
 (одна точка для кожній з 3 кривих).
Порівняти результат з розрахунком на
ПК.
(одна точка для кожній з 3 кривих).
Порівняти результат з розрахунком на
ПК.
