
2.Водные ресурсы
Водные ресурсы
Вода выполняет важную роль в быту и народном хозяйстве. В ряде производств вода играет роль и сырья, и реагента. Например, в производстве водорода, кислот, щелочей в реакциях гидратации и гидролиза, т.е. в химической промышленности. В металлургической, пищевой и легкой промышленности вода используется как растворитель твердых, жидких и газообразных веществ. В некоторых производствах вода образуется вследствие химических реакций, т.е. можно сказать, что вода в ряде производств выполняет технологическую функцию. В значительно больших объемах используется как теплоноситель (у воды большая теплоемкость, доступность, безопасность). Водой (паром) нагревают и охлаждают. В огромных количествах воду используют как теплоноситель в ТЭЦ, АЭС, котельных.
Большим потребителем воды является химическая промышленность. Поэтому, как правило, химические и нефтеперабатывающие предприятия строят рядом с водными источниками. Например, для производства 1 тонны алюминия необходимо 1500 тонн воды, 1 тонны вискозного шелка – 1200 м3 свежей и 1500 м3 оборотной воды, завод хлорорганического синтеза потребляет воды как город с населением 800 тыс. человек.
Средне-суточное потребление воды на 1 городского жителя 300 – 500 литров.
Однако самым большим потребителем является сельское хозяйство. На производство суточной нормы продуктов на одного человека необходимо 6 м3 воды.
Вода занимает 70% поверхности земного шара - ее общий объем 1345 млн.км3. 97% всего количества воды - это мировой океан.
Пресная вода, которая составляет всего 2% от общего объема, распределена на земном шаре неравномерно. Поэтому в разных странах нехватка пресной воды ощутима (1/3 населения испытывает недостаток пресной воды).
Запасы пресной воды потенциально велики. Однако в любом районе мира они могут истощиться из-за нерационального водопользования или загрязнения. На промышленные и хозяйственные нужды используется, в основном, пресная вода - это около 150 км3, что составляет менее 0,5% всего речного стока Земли. Но для того, чтобы иметь это количество воды для промышленных и хозяйственных нужд, из источников необходимо отбирать в 4 раза больше, т.е. 600 км3 в год.
Подавляющее большинство промышленных предприятий загрязняют водоемы. Конечно, в настоящее время многие предприятия используют возвратные воды, но огромное их количество сбрасывается в реки и другие водоемы (сброс составляет порядка 450 км3). Однако для обеззараживания даже после основательной биологической очистки эти воды необходимо разбавлять свежей чистой водой. Нормы разбавления велики и составляют, например, для стоков производства синтетических волокон 1:185, а для стоков производства полиэтилена и полистирола 1:29.
Для обезвреживания стоков во всем мире ежегодно нужно затрачивать примерно 5500 км3 чистой воды. Это в 3 раза больше расхода на все другие нужды человечества, что составляет 30% устойчивого стока всех рек мира.
Таким образом, очевидно, что проблема пресной воды тесно связана не только с проблемой экономии, но и с проблемой очистки сточных вод.
Характеристика воды и основные примеси, содержащиеся в воде
Природные воды на основании происхождения можно разделить на следующий категории:
Атмосферные воды, выпадающие в виде дождя и снега. Они содержат небольшое количество примесей, преимущественно в виде растворенных газов: кислорода, оксида углерода, оксида азота, сероводорода, органических веществ, пыли. Атмосферная вода практически не содержит растворенных солей. Вода, содержащая менее 1 грамма солей на 1 литр, называется пресной. В данном случае атмосферные воды - это пресные воды.
Поверхностные воды – речные, озерные, морские, содержат, кроме примесей имеющихся в атмосферной воде, самые разнообразные вещества. При чем, от небольших количеств до насыщения. Это гидрокарбонаты кальция, магния, натрия, калия, а также сульфаты и хлориды. В морской воде присутствуют почти все элементы таблицы Менделеева, включая драгоценные и радиоактивные элементы. В мировом океане растворено примерно 5*1016 т солей (если этой солью покрыть поверхность земного шара то толщина слоя составит около 45м). Уже сейчас химическая промышленность добывает из морской воды 200 млн. тонн поваренной соли. Добывают также магний калий и бром.
При содержании солей более 1 грамма на 1 литр вода называется соленой. Таким образом, мы имеем соленую воду в морях, океанах и некоторых озерах.
Во всех поверхностных водах содержатся органические вещества, в том числе и болезнетворные бактерии.
В Белгородской области почти все реки относятся к третьему классу чистоты – умеренно загрязненные. Основными потребителями поверхностных вод в Белгородской области являются рыбхозы - 80 млн.м3, промышленность - 25 млн.м3 , сельское хозяйство - 1,5 млн.м3 .
Подземные воды – воды артезианских скважин, колодцев, ключей, гейзеров так же как и поверхностные воды, содержат разнообразные минеральные соли, состав которых зависит от характера горных пород, через которые просачиваются атмосферные и поверхностные воды. Но, в отличие от поверхностных вод, благодаря высокой фильтрующей способности почв и горных пород, в подземных водах нет органических примесей и бактериальной загрязненности.
Питьевое водоснабжение России в основном обеспечивается за счет подземных вод.
В Белгородской области в качестве источников водоснабжения используются в основном подземные воды, базирующиеся, как правило, на турон-маастрихтском и альб-сеноманском водоносных горизонтах. Незначительная часть сельских населенных пунктов использует воду четвертичного и палеогенового водоносных горизонтов (шахтные колодцы).
По данным Комитета природных ресурсов по Белгородской области, общие прогнозные эксплуатационные ресурсы подземных вод составляют около 6 млн. м3/сут.
В настоящее время на территории области для хозяйственно-питьевого, производственно-технического и сельскохозяйственного водоснабжения разведано 55 месторождений пресных подземных вод с общими эксплуатационными запасами 1373,7 тыс. м3/сут. Из разведанных 55 месторождений сейчас эксплуатируются только 27.
Общее среднее потребление воды хозяйственно-питьевого назначения на одного жителя области составляет 267 л/сут, среднее потребление воды на одного городского жителя - 305 л/сут, а сельского - около 210 л/сут.
Наша область располагает небольшими ресурсами поверхностных вод. В основном преобладают малые реки и ручьи, и только 14 рек имеют протяженность от 50 до 200 км.
В последние годы интенсивно ведутся разработки по разведке, добыче и разливу минеральных вод (Майская, Святой Источник, и т.д.). Воды, содержащие радон, используются в лечебных целях (Борисовский, Чернянский районы).
Все примеси содержащиеся в воде можно разделить по признаку физико-химического состояния их в воде, в частности, их дисперсности. В таблице 2.1. приводится схема классификации примесей воды.
Таблица 2.1. Классификация примесей воды
Фазовая
характерис-тика
Гетерогенные системы
Гомогенные системы
Группа I
Группа II
Группа III
Группа IY
Физико-химическая характеристика
Взвеси (суспензии, эмульсии)
Золи и высокомолеку-лярные соединения
Молекулярно-растворимые вещества
Вещества, диссоцииру-ющие на ионы
Размеры частиц, см
10-1
10-3
10-7
10-8
В первую группу входят нерастворимые в воде примеси с размерами частиц больше 10-4 см, образующие так называемые взвеси. Это глинистые вещества, карбонаты, гипс, ил, мелкий песок, гидроксиды металлов, некоторые органические вещества, планктон. Среди них могут быть бактерии, споровые микроорганизмы, вирусы. На поверхности взвешенных частиц могут находиться радиоактивные и ядовитые вещества. Системы первой группы неустойчивы.
Вторую группу примесей составляют вещества, находящиеся в коллоидно-дисперсном состоянии (гидрофильные и гидрофобные коллоиды).
Это минеральные и органоминеральные частицы почв и грунтов, гумусовые вещества (придающие воде окраску), вирусы, бактерии, высокомолекулярные органические вещества с размерами частиц 10-5 — 10-6 см.
В третью группу примесей воды входят растворимые газы и органические вещества биологического и технологического происхождения. Эти вещества могут придавать воде различную краску, привкусы и запахи. Некоторые примеси сильно токсичны.
К четвертой группе примесей относятся вещества, образующие при диссоциации в воде ионы.
В зависимости от наличия тех или иных примесей в воде применяются различные методы очистки.
Качество воды
Качество воды оценивают по следующим показателям: прозрачность, цвет, запах, жесткость, окисляемость, реакция воды, общее солесодержание.
Прозрачность воды измеряется толщиной слоя воды, через который можно различать визуально или с помощью фотоэлемента изображение перекрестья или определенного шрифта. Прозрачность зависит от наличия в воде грубодисперсных взвесей и коллоидных частиц. Эти примеси засоряют трубопроводы, образуют пробки, коллоидные частицы засоряют диафрагмы пропускающих устройств, вызывают вспенивание воды и переброс воды в котлах и аппаратах.
Жесткость воды различают временную (обусловлена наличием гидрокарбонатов натрия, магния, кальция, которые при кипячении переходят в нерастворимые карбонаты, выпадающие в виде плотного осадка – накипи). Постоянная жесткость обусловлена наличием в воде хлоридов и сульфатов магния и кальция, которые не удаляются из воды при кипячении. Жесткость выражается в миллиграммэквивалентах ионов кальция или магния на 1 литр воды. Жесткость равна 1 мгэкв, если в 1 литре содержится 20,04 мг ионов кальция или 12,16 мг ионов магния.
Жесткость - очень важная характеристика воды. При нагревании жесткой воды образуется накипь. По химическому составу накипь представляет смесь различных веществ: гипса, карбонатов, силикатов кальция, фосфора, алюминия и т.д. Она имеет низкую теплопроводность. Следовательно, чем выше слой накипи, тем ниже производительность и экономичность паровых котлов и теплообменников (в котлах при наличии накипи в 1 мм расход топлива повышается на 5 %). Кроме того, при этом имеет место окисление стали, пережег котла, аварии и даже взрыв. Жесткая вода непригодна для электролиза, текстильной промышленности, пищевой и т.д.
Окисляемость воды обусловлена присутствием в ней органических веществ, легкоокисляющихся соединений железа и сероводорода, способных окисляться различными окислителями. Так как состав этих примесей неопределенен, окисляемость воды выражается в количестве перманганата калия или эквивалентном ему количестве кислорода, затраченного на окисление 1 литра воды, то есть мг/л.
Степень кислотности воды определяется величиной индекса рН . Если рН = 6,5 – 7,5 вода нейтральна; если рН < 6,5 – вода считается кислой; если рН > 7,5 - щелочной.
По своим характеристикам природные воды близки к нейтральным. Однако, за некоторыми исключениями, природную воду нельзя использовать без предварительной подготовки. Особенно это важно для питьевой воды.
Питьевая и техническая вода
В зависимости от назначения и использования вода делится на питьевую и техническую; их качество определяется ГОСТом.
Питьевая вода - к ней предъявляются особые требования – кроме цвета, запаха, вкуса важным является бактериальная загрязненность. В 1 миллилитре воды должно быть не более 100 бактерий, а, например, кишечных палочек не более 3, соли не должны превышать 1000 мг/л.
Очень часто для питьевых целей используют не только подземные воды, но и поверхностные, поэтому как те, так и другие подвергаются различным степеням очистки на водоочистных станциях или сооружениях. На рис.2.2. приведена схема очистки поверхностных вод, используемых в качестве питьевой воды. Если водозабор осуществляется непосредственно из водоема (1), то вода поступает в грубый отстойник (2) самотеком через предохранительную сетку, которая предотвращает попадание в отстойник крупных предметов, рыбы и т.д.
Рис. 2.2. Схема очистных сооружений для поверхностных вод:
1- водоем; 2- грубый отстойник; 3 – коагулятор; 4 – отстойник; 5 – открытые фильтры; 6- система для обеззараживания; 7 – водораспределительная система.
В отстойнике вода отстаивается. Однако легкая взвесь осаждается медленно, а коллоидные частицы (глина, кремниевые кислоты, гуминовые кислоты) методом осаждения не отделяются, поэтому вода насосом подается в смеситель коагулятор (3), в который одновременно поступает раствор электролита Al2SO4, FeSO4 или другие коагулянты.
Коагуляция - это процесс разделения гетерогенных систем.
В упрощенном виде это выглядит так: электролит в очень разбавленном состоянии гидролизуется с образованием положительно заряженных частиц. Они, в свою очередь, адсорбируются на поверхности отрицательно заряженных коллоидных частиц и нейтрализуют их заряды. Это приводит к слипанию частиц, они становятся более крупными и способными к осаждению. Образовавшиеся в процессе коагуляции хлопья твердых частиц слипаются с легкой взвесью, адсорбируют на поверхности органические красящие вещества и тем самым осветляют воду (расход коагулянта 120 г/м3 весной, летом - 70, а зимой - 20). Для интенсификации процесса коагуляции применяются дополнительные реагенты - флокулянты – кремниевая кислота, карбоксиметилцеллюлоза и т.д. Из смесителя вода поступает в отстойник (4), где завершается коагуляция: крупные частицы выпадают в осадок. Отстойник - это большие, непрерывно действующие бетонированные резервуары с системой перегородок, увеличивающих время пребывания воды в отстойнике. Затем вода подается в открытые фильтры (5), здесь она фильтруется под давлением (высота столба воды - 2 м, скорость прохождения воды - 1 м/час, фильтрующий материал - кварцевый песок слоем до 1 м, диаметр частиц до 1 мм, внизу гравий). Основная часть загрязнений оседает на поверхности песка, создавая фильтрующую пленку. Станции имеют несколько фильтров, т.к. их периодически чистят.
Осветленная вода поступает далее для обеззараживания в аппарат (6), где проводится хлорирование. Чтобы удалить запах хлора, добавляют аммиак или сульфат натрия. Норма остатка хлора 0,2 – 0, 4 мг/л. В последнее время для обеззараживания используется озонирование и другие методы.
После обеззараживания вода поступает в водораспределительную систему (7) и далее к потребителю.
Промышленная вода может быть питательной (используется для технологических целей) и оборотной (после использования ее охлаждают и опять возвращают в производственный цикл).
Количество примесей в промышленной воде не должно превышать определенные нормы, которые устанавливаются в зависимости от назначения воды. Например, вода для паровых котлов не должна содержать оксид углерода, должно быть мало кислорода; для производства полупроводников и люминофоров вообще должна быть высокая степень очистки воды. Для промышленной воды не имеет значения бактериальная загрязненность (кроме пищевой и фармацевтической промышленности, некоторых химических технологий).
Таким образом, очевидно, что промышленные воды также должны подвергаться соответствующей обработке.
К основным методам очистки промышленных вод следует отнести: коагуляцию, отстаивание, фильтрацию (это как для питьевой воды), а также умягчение, обессоливание, дистилляцию, деаэрацию. Схема промышленной водоподготовки приведена на рис. 2.3.
Осветление воды достигается отстаиванием ее с последующим фильтрованием через зернистый материал различной дисперсности. Для коагуляции коллоидных примесей и абсорбции окрашенных веществ, содержащихся в воде, добавляют электролиты - сульфаты алюминия и железа.
Обессоливание – это удаление из воды катионов, образующих пену и накипь Ca2+ , Mg2+ . Для этого воду пропускают через специальные фильтры с Н-катионитом и ОН-анионитом. Возможно также использование дистилляции или вымораживания.
Для умягчения воды используются физические, химические и физико-химические способы. К физическим - относятся кипячение, дистилляция, вымораживание. Химические способы - это использование специальных реагентов, которые связывают ионы магния и кальция в нерастворимые или легкоудаляемые соединения (гашеная известь, сода, едкий натр и т.д.).
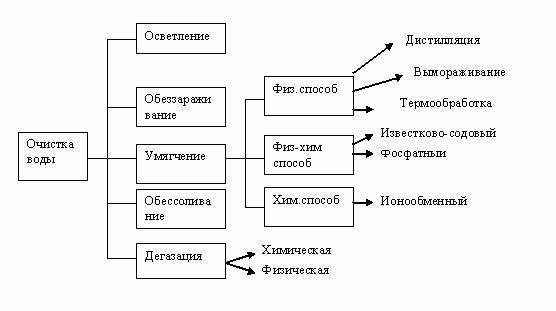
Рис. 2. 3. Схема промышленной водоподготовки.
В настоящее время основным является физико-химический метод, основанный на способности некоторых не растворяемых синтетических материалов обменивать свои ионы на ионы, присутствующие в воде (катиониты, аниониты). Обмен осуществляется в ионообменниках (скоростных фильтрах).
Умягчение воды резко снижает скорость образования накипи, но не предупреждает ее и поэтому в воду добавляют антинакипины: фосфат натрия гексаметафосфат Na2PO4, (NaPO3)6. Они образуют нерастворимые в воде примеси и после соответствующей обработки с использованием дубильных веществ (например, крахмал) превращают накипь в рыхлый осадок, который легко удаляется. Для предупреждения образования накипи используется также магнитный метод очистки воды.
Деаэрация (дегазация). Удаление из воды растворенных газов может осуществляться физическими методами: кипением, при этом удаляется кислород и оксид углерода; нагревом в вакууме. Химический метод заключается в добавлении к воде химических реагентов, связывающих кислород и оксид углерода (сульфат натрия, гидразин (N2H4 ), или в использовании чугунно-стружечный фильтров, в которых при соединении кислорода с железом образуется оксид железа, который удаляется промывкой фильтра.
Следует отметить, что водоочистка сказывается на себестоимости продукции. Например, фильтрование воды увеличивает ее стоимость в 2,5 раза, частичное умягчение в 8 раз, а обессоливание и умягчение в 10 – 12 раз.
Сточные воды. Методы очистки
Количество сточных вод растет и перед человечеством стоит проблема истощения пресных вод.
Главными источниками загрязнения рек Белгородской области являются сточные воды населенных пунктов, предприятий промышленности, животноводческих комплексов, сельскохозяйственных полей. Необходимо иметь в виду, что большинство сточных вод после их очистки не соответствует по ряду показателей природоохранным нормативам. Антропогенному загрязнению в той или иной мере подвержены все реки Белгородской области. Самые распространенные загрязнители вод - нефтепродукты, аммонийный азот, фенолы и органические вещества. По некоторым из них наблюдаются превышения предельно допустимых концентраций (ПДК). В области преобладает 3-й класс качества воды (умеренно-загрязненная).
Поэтому необходим новый подход к проблеме пресной воды. Во-первых, следует минимально использовать свежую воду, особенно на химических предприятиях, а во вторых, внедрять бессточные и замкнутые системы. Задача сокращения расходов воды в настоящее время решается в 3 направлениях:
Ø применение оборотного водоснабжения;
Ø замена водяного охлаждения воздушным;
Ø очистка сточных вод и их повторное использование.
Сточные воды содержат органические и неорганические примеси и болезнетворные бактерии.
Химическое загрязнение представляет собой изменение естественных химических свойств воды за счет увеличения содержания в ней вредных примесей как неорганической (минеральные соли, кислоты, щелочи, глинистые частицы), так и органической природы (нефть, нефтепродукты, органические остатки, поверхностно-активные вещества, пестициды).
Причем следует иметь в виду, что каждое производство имеет свой набор веществ, от которых необходимо очистить сточные воды. Поэтому очистка сточных вод очень сложный процесс, который зачастую идет в несколько стадий, или применяются разнообразные методы очистки.
Существующие методы очистки вод можно разделить на следующие:
1.физические (включая механические) методы очистки воды.
2. химические методы очистки воды.
3. физико-химические методы очистки воды.
4.биологические методы очистки воды.
К физическим методам относятся методы, основанные на воздействии на водную систему при различных технологических процессах: магнитных, электрических полей, ультразвука, радиационного облучения и т.д. Особо выделяется среди физических методов - механический.
Механические методы очистки воды удаляют до 60% нерастворимых примесей из бытовых вод и 95% из технических. Это методы отстаивания, центрофугирования, механического удаления нефтепродуктов, которые всплывают на поверхность воды.
При механической очистке сточных вод применяют песколовки, резервуары-отстойники, нефтеловушки, пруды-отстойники различных конструкций.
Песколовки предназначены для выделения механических примесей с размером частиц более 250 мкм. Необходимость предварительного выделения механических примесей (песка, окалины и др.) обуславливается тем, что при отсутствии песколовок эти примеси выделяются в других очистных сооружениях, усложняя эксплуатацию последних.
Принцип действия песколовки основан на изменении скорости движения твердых тяжелых частиц в потоке жидкости.
Статические отстойники используют нефтетранспортные предприятия (нефтебазы, нефтеперекачивающие станции). Для этой цели обычно используют стандартные стальные или железобетонные резервуары, которые могут работать в режиме резервуара-накопителя, резервуара-отстойника или буферного резервуара в зависимости от технологической схемы очистки сточных вод. В этих резервуарах отделяют до 90-95% легко отделимых компонентов. Для этого в схему очистных сооружений устанавливают два и более буферных резервуара, которые работают периодически: заполнение, отстой, выкачка. Отстаивание воды в вертикальных резервуарах может протекать в динамическом и непроточном режимах.
Отличительная особенность динамических отстойников заключается в отделении примеси, находящейся в воде, при движении жидкости.
В динамических отстойниках или отстойниках непрерывного действия жидкость движется в горизонтальном или вертикальном направлении, отсюда и отстойники подразделяются на вертикальные и горизонтальные.
Горизонтальный отстойник представляет собой прямоугольный резервуар (в плане) высотой 1,5-4 м, шириной 3-6 м и длиной до 50 м. Выпавший на дне осадок специальными скребками передвигают к приемнику, а затем гидроэлеватором, насосами или другими приспособлениями удаляют из отстойника. Всплывшие примеси выводят с помощью скребков и поперечных лотков, установленных на определенном уровне.
В зависимости от улавливаемого продукта горизонтальные отстойники делятся на песколовки, нефтеловушки, мазутоловки, бензоловки, жироловки и т.п.
Вертикальный отстойник представляет собой цилиндрический или квадратный (в плане) резервуар с коническим днищем для удобства сбора и откачки осаждающегося осадка. Движение воды в вертикальном отстойнике происходит снизу вверх (для осаждающихся частиц).
В процессе механической очистки используются различного типа фильтры. Фильтрование в настоящее время используется все чаще, так как повышаются требования к качеству очищенной воды. Фильтрование применяют после очистки сточных вод в отстойниках и биологической очистки. Процесс основан на прилипании грубодисперсных частиц, особенно нефти и нефтепродуктов, к поверхности фильтрующего материала. Фильтры могут быть тканевые, сетчатые, зернистые. Пленочные фильтры очищают воду на молекулярном уровне.
Для микрофильтров используется капроновая микросетка или микросетка из волокнистого стекла, латунная, никелевая, из нержавеющей стали, фосфористой бронзы, нейлона. Размеры ячеек от 20 до 70 микрон.
В последнее время широко используется процесс разделения с использованием молекулярных сит. Наиболее перспективным для тонкой очистки считается мембранный метод. Этот метод, характеризуется высокой четкостью разделения смесей веществ.
Мембраны обладают свойством полупроницаемости - они задерживают не только взвешенные в воде вещества, но и растворенные.
Мембранный метод используют для обработки воды и водных растворов, очистки сточных вод, очистки и концентрации растворов. Особенно эффективен этот метод для обессоливания воды (удерживается до 98% соли).
Принципиальное отличие мембранного метода от традиционных приемов фильтрования - разделение продуктов в потоке, т.е. разделение без осаждения на фильтроматериале осадка, постепенно закупоривающего рабочую пористую поверхность фильтра.
Основные требования, предъявляемые к полупроницаемым мембранам: высокая разделяющая способность (селективность); высокая удельная производительность (проницаемость); химическая стойкость к действию среды разделяемой системы; неизменность характеристик при эксплуатации; достаточная механическая прочность, отвечающая условиям монтажа, транспортировки и хранения мембран; низкая стоимость.
Для разделения или очистки некоторых нетермостойких продуктов применение мембранного метода является решающим, так как этот метод работает при температуре окружающей среды.
В то же время мембранный метод имеет недостаток - накопление разделяемых продуктов вблизи рабочей поверхности разделения. Для борьбы с этим явлением проводят турбулизацию слоя жидкости, прилегающего к поверхности мембраны, чтобы ускорить перенос растворенного вещества.
Для мембран используют разные материалы, а различие в технологии изготовления мембран позволяет получить отличные по структуре и конструкции мембраны, применяемые в процессах разделения различных видов.
В зависимости от разделяемых сред и требований, предъявляемых к качеству разделения, технологических условий эксплуатации, используются различные мембраны. Они могут быть плоскими (ленты до 1 м шириной), трубчатыми (диаметром от 0,5 до 25 мм), различными по структуре - пористые, непористые, анизотропные, изотропные, уплотняющие и т.д. Изготовляются мембраны из стекла, металлической фольги, полимеров – ацетата целлюлозы, полиамидов, поливинилов и т.д. Мембраны из ацетатцеллюлозы самые дешевые. Для увеличения механической прочности мембраны имеют тканевую основу. В средине 80-х годов появились высокопроизводительные композитные мембраны, что расширило их использование.
При использовании мембран вода не должна быть по кислотности выше рH~4, а температура не превышать35 градусов.
К физическим методам относится электролитический метод. При этом способе электрический ток пропускают через промышленные стоки, что приводит к выпадению большинства загрязняющих веществ в осадок. Этот способ очень эффективен и требует относительно небольших затрат на сооружение очистных станций.
Магнитный метод очистки воды. Предложен Вермаереном для предотвращения накипи. Суть метода состоит в том, что вода пропускалась через магнитные активаторы (С- образные магниты, в рабочий зазор которых помещается ионообменная колонна). Магнитное поле интенсифицирует ионообмен, т.е. корректирует солевой обмен и способствует уменьшению накипообразования.
Магнитная обработка водных систем, прежде всего, ускоряет процесс кристаллизации примесей и тем самым уменьшает количество накипи на стенках. При магнитной обработке скорее идет процесс осветления воды.
Биологическая очистка воды заключается в минерализации органических загрязнений сточных вод при помощи аэробных биохимических процессов. В результате биологической очистки вода становится прозрачной, не загнивающей, содержащей растворенный кислород и нитраты.
Биологическая очистка сточных вод в естественных условиях часто осуществляется на специально подготовленных участках земли - полях орошения или полях фильтрации. На полях орошения одновременно с очисткой вод производится выращивание сельскохозяйственных культур или трав. Поля фильтрации предназначены только для биологической очистки сточной жидкости. На отведенных под поля орошения и фильтрации участках земли планируется оросительная сеть из магистральных и распределительных каналов, по которым разливаются сточные воды. Очистка от загрязнений происходит в процессе фильтрации вод через почву. Слой почвы в 80 см обеспечивает достаточно надежную очистку.
Для биологической очистки сточных вод в естественных условиях используют биологические пруды. Они представляют собой неглубокие земляные резервуары от 0,5 до 1 м глубиной, в которых происходят те же процессы, что и при самоочищении водоемов. Биологические пруды работают при температуре не менее 60С и не выше 200С и кислотности воды в интервале рH от 6,5 до 8,2.Обычно пруды устраивают в виде 4 -5 секций на местности, имеющий уклон. Их располагают ступенями так, что вода из верхнего пруда самотеком направляется в расположенный ниже.
Биологическая очистка сточных вод в искусственных условиях производится в специальных сооружениях – биофильтрах или аэротенках.
Биофильтрами называются сооружения, в которых биологическая очистка сточных вод осуществляется при их фильтрации через слой крупнозернистого материала. Поверхность зерен покрыта биологической пленкой, заселенной аэробными микроорганизмами. Сущность биологической очистки сточных вод на биофильтрах не отличается от процесса очистки на полях орошения или полях фильтрации, однако биохимическое окисление происходит гораздо интенсивнее.
Аэротенки представляют собой железобетонные резервуары, через которые медленно протекают подвергающиеся аэратации сточные воды, смешанные с активным илом.
Активный ил имеет вид хлопьев бурого цвета. Он состоит, в основном, из бактериальных клеток. На поверхности хлопьев, между ними или внутри них обычно находятся разнообразные простейшие организмы.
Источником питания организмов активного ила служат загрязнения сточных вод. Содержащиеся в сточной жидкости вещества сорбируются поверхностью активного ила. Уже после контакта ила со сточной водой концентрация в ней органических веществ снижается более чем на половину. Растворенные органические вещества переносятся ферментами - пермеазами внутрь бактериальных клеток, где они подвергаются разрушению и перестройке.
Взвешенные вещества, поступающие в аэротенк, также сорбируются поверхностью активного ила. Частично наряду с бактериями они служат пищей простейшим, а частично под воздействием бактериальных ферментов превращаются в растворенные вещества и усваиваются микрофлорой.
Аэротенки обеспечивают высокую степень очистки сточных вод, могут применяться в любых климатических условиях и не требуют больших площадей. Очистные сооружения г.Белгорода используют для очистки сточных вод аэротенки.
Новой модификацией аэротенка является биотенк. Его особенность - установленные в внутри аэротенка пластины из пленки, которая так же участвует в процессе очистки.
В процессе биологической очистки не достигается полного удаления из сточных вод всех бактерий, в том числе болезнетворных. Поэтому после биологической очистки воды проводят дезинфекцию сточных вод перед выпуском их в водоем. Это осуществляют хлорированием, ультрафиолетовыми лучами, электролизом, озонированием или ультразвуком.
Для обработки и обезвреживания осадка, образующегося на очистных канализационных станциях, применяют особые методы и сооружения: гнилостные резервуары (септики), двухъярусные отстойники и метантанки.
Для обезвоживания сброженного осадка его направляют на иловые площадки, где он подвергается естественной сушке. После чего может быть утилизирован как органическое удобрение. Обезвоживание осадка можно производить и искусственным путем на вакуум-фильтрах, вакуум-прессах, центрифугах, а также термической сушкой.
Следует отметить, что не все сточные воды следует подвергать биологической очистке. Если в них отсутствуют органические вещества или их количество мало, то биологическая очистка не производится.
Химические и физико-химические методы очистки воды. Сущность химического метода заключается в том, что на очистных станциях в стоки вносят реагенты - коагулянты. Они вступают в реакцию с растворенными и нерастворенными загрязняющими веществами и способствуют выпадению их в осадок, откуда их удаляют механическим путем. Особенно хорошо химический метод зарекомендовал себя при очистке вод в период паводков.
Но это способ непригоден для очистки стоков, содержащих большое количество разнородных загрязнений. Так как практически каждое производство имеет свои сточные воды, то и очистка производится с использованием определенных коагулянтов. Например, для очистки вод гальванических цехов (основном цианиды) используется окисление хлором. Но практически всегда требуется после этого доочистка воды.
Химический метод состоит в добавлении к очищаемой воде коагулянтов – гидролизных солей с гидролизующими катионами, анодным растворением металлов, или простым изменением кислотности воды (уменьшение рН), если в обрабатываемой воде уже содержаться в достаточном количестве катионы, способные образовать при гидролизе малорастворимые соединения.
В настоящее время в качестве коагулянтов используют соли алюминия, железа или их смеси (сульфат алюминия, алюминат натрия, полихлорид алюминия, квасцы алюмокалиевые или аммиачные, кремниевая кислота).
Для ускорения процесса коагуляции и интенсификации работы очистных сооружений широко применяют флокулянты: полиакриламид (ПАА), активированная кремниевая кислота анионного типа, глина, зола, феррохромовые шлаки и др.
Обработка воды с использованием коагулянтов известна давно, использовать же активно этот метод стали сравнительно недавно. Это связано с тем, что, во-первых, критерием оценки санитарной надежности были биологические показатели. Во-вторых, для этого метода нужна большая доза коагулянтов, необходимость для каждого случая очистки своей дозировки и своего коагулянта, высокая стоимость коагулянтов, а также плохие условия отделения осадков коагулянта и т.д.
Но в настоящее время расчет дозировки проводится автоматически по качественным показателям стоков. Большой расход коагулянтов можно в настоящее время компенсировать использованием дешевых отходов промышленных производств и высокомолекулярных коагулянтов.
В случае нефте- и маслосодержащих сточных вод после нефтеловушек, применение коагулянтов снижает концентрацию нефтепрмесей в 2 - 3 раза. Лучшими коагулянтами считаются FeSO4, Ca(OH)2.
В том случае, когда в воде содержатся красящие и дубильные вещества, применение коагулянтов типа FeSO4, Al2 (SO4)3 очищает воду на 80 – 90%.
Преимуществом методов очистки с помощью коагулянтов по сравнению с биологическим, является сокращение длительности очистки; меньшая площадь очистных сооружений, почти полное удаление фосфатов и микроэлементов; незначительное изменение pH; независимость от токсических веществ; большие возможности автоматизации производства.
Но в тоже время существенным недостатком является - увеличение объема осадков (без коагулянтов осадок составляет 0,4 – 0,6 % от объема обрабатываемой жидкости, а при его наличии до 2,5%).
Следует отметить также, что химический метод менее эффективен при очистке бытовых и сточных вод, содержащих органические соединения.
Более прогрессивным является метод электрокоагуляция - метод очистки воды с использованием электролиза с растворимыми электродами.
При очистке воды с использованием коагулянтов часто используют ультразвук. Он разрушает крупные частицы, при этом также уничтожаются некоторые бактерии, зоопланктон, водоросли.
Интенсифицировать процесс очистки можно используя бета-, гамма- рентгеновское излучение, электрические и магнитные поля - это также улучшает качество воды, снижает расходы коагулянтов, а, следовательно, снижает себестоимость очищенной воды.
К химическим методам относится экстрагирование, извлечение загрязнений из воды с помощью другой жидкости. Для экстрагирования подбирают не смешивающуюся с водой жидкость, в которой вещество, загрязняющее воду, растворяется лучше, чем в воде.
В качестве экстрагентов применяются органические жидкости: бензол, минеральные масла, четыреххлористый углерод, сероуглерод и др. Самый процесс осуществляется в аппаратах, называемых экстракторами. Недостатками этого метода можно считать растворимость экстрагента в воде и неполноту разрушения эмульсии.
Очистка сточных вод методом адсорбции основана на том, что растворенные в них вещества адсорбируются на поверхности адсорбента. Адсорбция относится к физико-химическим методам очистки. В качестве сорбента применяют золу, торф, каолин, коксовую мелочь, активированный уголь и др.
В некоторых случаях можно практически целиком удалить из воды загрязняющее вещество. Если адсорбирующее вещество является малоценным и стоимость адсорбента невысока (опилки, торф, шлак и т. д.), то после очистки адсорбент выбрасывается вместе с адсорбированным веществом. Если загрязняющее вещество и адсорбент представляют собой определенную ценность, то адсорбент подвергается регенерации непосредственной отгонкой адсорбированного вещества или экстракцией его каким-либо растворителем. Часто регенерировать адсорбент полностью не удается, так как он вступает в химические реакции с адсорбируемым веществом.
Следует отметить, что правила спуска сточных вод в водоемы не допускают сброса кислых и щелочных стоков, так как они губят микрофлору водоемов. Необходимо производить нейтрализацию подобных сточных вод перед спуском в водоем. При расчете нейтрализационных установок учитывают только концентрацию свободных кислот и оснований.
При нейтрализации кислых вод применяют известь, известняк, мрамор, доломит и обожженный доломит; щелочные воды нейтрализуются технической серной кислотой. При нейтрализации сточных вод следует учитывать естественную нейтрализующую способность водоема. Искусственной нейтрализации должно подвергаться лишь то количество кислоты, которое не может быть нейтрализовано в нем.
Для нейтрализации сточных вод прибегают к мутационному фильтрованию через мел, мрамор, доломит или обожженный доломит, известный под названием «магномасса».
Из всех перечисленных материалов самым удобным является магномасса, а самой важной ее частью — окись магния, обладающая рядом преимуществ по сравнению с карбонатами и окисью кальция: а) окись магния нерастворима в воде и поэтому не переходит в раствор в отсутствие кислот; б) при нейтрализации ею сильных кислот не происходит образования двуокиси углерода и, следовательно, в нейтрализованной воде не возрастает карбонатная жесткость; в) скорость нейтрализации окисью магния больше, чем карбонатами.
Для нейтрализации следует также использовать взаимную нейтрализацию стоков. Когда в производстве имеются кислые и щелочные стоки, рационально нейтрализовать их смешиванием. Количество свободной щелочности и кислотности в стоках определяют анализом.
В тех случаях, когда требуется извлечь из сточных вод ценные вещества, применяется метод флотации, относящийся к физико-химическим методам.
Он основан на различной смачиваемости частиц смеси гидрофобных (не смачиваемых) и гидрофильных (смачиваемых) веществ. Практически применяется пенно-флотационный процесс, заключающийся в том, что через жидкость с флотируемым веществом снизу продувается воздух. Пузырьки воздуха адсорбируют на своей поверхности частицы извлекаемого (гидрофобного) вещества и выносят их на поверхность воды.
Для усиления флотационного эффекта к воде добавляют поверхностно-активные вещества (нефть, мазут, смолы, керосин, высокомолекулярные жирные кислоты, меркаптаны, ксантогенаты и др.), которые понижают поверхностное натяжение жидкости, ослабляя связь воды с твердым веществом.
Процесс флотации усиливается также введением в жидкость пенообразователей (тяжелый пиридин, креозол, фенолы, синтетические моющие вещества и т. д.), которые также понижают поверхностное натяжение жидкости и увеличивают дисперсность пузырьков и их устойчивость.
После очистки вода подвергается дополнительной обработке с использованием хлора, активированного угля, перманганата калия, аммиака, и т.д.
Обеззараживание воды является обязательным звеном в процессе приготовления питьевой и, иногда, промышленной воды. После очистки сточных вод, зачастую, прежде чем вторично использовать воду, требуется ее обеззараживание.
Отказ от обеззараживания приводит к развитию новых бактерий, паразитов, которые могут привести к заболеваниям и даже летальным исходам (например, в 1993 году в Миллуоки - (США) 50% населения пострадало, около 4000 человек госпитализировали и 50 умерло).
Для обеззараживания используется хлор, озон, иод, марганцевогислый калий, перекись водорода, гипохлорид натрия и кальция.
Один из методов обеззараживания - метод с применением химических окислителей. Это хлорамины или связанный хлор и молекулярный хлор, гипохлоридная кислота - свободный хлор. Бактерицидное действие свободного хлора в 20 – 25 раз сильнее. При хлорировании необходимо перемешивание, а затем не менее чем 30-минутный (при совместном хлорировании и аммонизации 60-минутный) контакт с водой, прежде чем вода поступит к потребителю.
Хлорирование проводят с помощью приборов - хлораторов. Так как бактерицидность хлора снижается с повышением рН, то обеззараживание проводится до того, пока в воду вводятся некоторые реагенты. Бактерии, находящиеся в воде, под действием хлора и его производных погибают. Хлор используется также и для обесцвечивания воды. Чтобы удалить запах хлора в воду добавляют аммиак.
Впервые обработка больших количеств воды хлором была применена в Германии в 1894 г. А. Траубе, который использовал в качестве реагента хлорную известь.
Хлорирование больших количеств воды в России было впервые осуществлено в 1910 г. как принудительная мера во время эпидемии холеры в Крондштате и брюшного тифа на Нижегородском водопроводе. Вначале воду хлорировали раствором хлорной извести. Первые опыты по применению газообразного хлора были осуществлены в 1917 г. на Петроградской водопроводной станции. Однако широкое использование газообразного хлора для дезинфекции воды началось в 1928-1930 гг., когда появились первые аппараты-хлораторы отечественной конструкции.
Хлорирование воды - постоянное мероприятие, осуществляемое на коммунальных водопроводах и станциях по обработке технических и сточных вод.
При наличии в воде фенола, хлор применять нельзя, в этом случае используют аммиак или сульфат аммония.
На очистных сооружениях используют также комбинированные методы обеззараживания: хлорирование с манганированием. Бактерицидный эффект хлора несколько усиливается при добавлении в обрабатываемую воду перманганата калия, этот реагент целесообразно применять при наличии неприятных запахов и привкусов, обусловленных наличием органических веществ, водорослей, актиномицетов и др.
Комбинированные хлор-серебряный и хлор-медный методы обеззараживания воды заключаются в одновременном добавлении в нее активного хлора и ионов серебра или меди. Бактерицидное действие ионов серебра и хлора в холодной воде находится в пределах суммарного эффекта доз хлора и серебра. Поскольку бактерицидность ионов серебра заметно возрастает с увеличением температуры, обеззараживающий эффект хлор-серебрянного метода увеличивается в теплой воде. Это способствует успешному применению данного метода для дезинфекции воды в плавательных бассейнах, где очень важно уменьшить дозу вводимого в воду хлора. Необходимые дозы серебра обычно подают в виде «серебряной воды».
Обеззараживание воды йодом. Данный метод применяют для обеззараживания воды в бассейнах. Для этой цели используют насыщенный раствор йода в воде, концентрация которого возрастает с повышением температуры.
Эффективным методом обеззараживания является озонирование. При озонировании не изменяются вкусовые качества воды, химические свойства, бактерицидное действие проходит быстрее и не надо, как в случае хлора, выдерживать воду.
Озон получают действием электрического заряда на воздух, обогащенный кислородом. При обработке воды озон разлагается с выделением атомного кислорода.
Озонирование воды имеет ряд преимуществ по сравнению с хлорированием: озон улучшает органолептические свойства воды и не загрязняет ее дополнительно химическими веществами; озонирование не требует дополнительных операций для удаления из очищенной воды избытка бактерицида, как дехлорирование при хлоре; это позволяет пользоваться повышенными дозами озона; озон вырабатывается на месте; для его получения требуется лишь электроэнергия, из химических реактивов пользуются только силикагелем в качестве адсорбента влаги (для подсушивания воздуха).
Широкому использованию метода озонирования мешает сложность получения озона, связанная с затратой больших количеств электроэнергии высокой частоты и использование высокого напряжения.
Для обеззараживания также применяют ультрафиолет, ультразвук, фторирование, причем иногда в воду специально добавляют фтор для предупреждения кариеса. После обеззараживания вода поступает в водонапорную башню, которая поддерживает постоянное давление в водопроводе.
Обработка воды озоном усложняется также его коррозионной активностью. Озон и его водные растворы разрушают сталь, чугун, медь, резину и эбонит. Поэтому все элементы озонаторных установок и трубопроводы, по которым транспортируются его водные растворы, должны изготовляться из нержавеющей стали или алюминия. В этих условиях продолжительность службы установок и трубопроводов из стали 15 — 20 лет, а алюминия 5 — 7 лет.
Запахи и привкусы, обусловленные наличием в воде микроорганизмов, можно устранить, используя активированный уголь как гранулированный, так и порошкообразный.
Существует также термический метод обеззараживания, который применяется при обеззараживании небольшого количества воды (больницы, санатории, пароходы, поезда). Гибель бактерий происходит за 5 – 10 мин в процессе кипячения. Метод дорогостоящий и не нашел широкого применения.
Кроме обеззараживания некоторые производства требуют стерилизации – уничтожения всех живых организмов в воде.
Прогресс техники, тщательный учет местных гидрологических условий при планировании производственных комплексов, позволит в перспективе обеспечить качественный круговорот пресных вод и, кроме того, пополнять ресурсы пресных вод, например за счет опреснения морских вод. Технически эта проблема решена, но очень дорогостоящая, так как требует большого расхода энергии.
Контрольные вопросы
1. Назовите основные характеристики воды, основные примеси, содержащиеся в воде.
2. Охарактеризуйте природные воды, их категории. Дайте определение качества воды. Укажите основные направления использования воды на производстве. Приведите примеры.
3. Назовите основные характеристики питьевой воды. Какие требования предъявляются к питьевой воде. Объясните схему очистки поверхностных вод при использовании ее в качестве питьевой воды.
4. Назовите основные характеристики промышленной или технической воды. Какие требования предъявляются к технической воде? Что такое водоподготовка?
5. Перечислите основные операции подготовки технологической воды. Охарактеризуйте их.
6. В чем заключается рациональное использование водных ресурсов в промышленности?
7. Охарактеризуйте основные методы очистки сточных вод.
8. Охарактеризуйте основные методы обеззараживания воды: хлорирование, озонирование, ультразвук, ультрафиолет, термическое обеззараживание.
