
- •Лекция 1 Введение
- •Физика Предмет физики
- •Лекция 2 Механика
- •Кинематика материальной точки
- •Динамика.
- •Динамика материальной точки.
- •Первый закон Ньютона. Инерциальные системы отсчёта (исо). Принцип относительности. Преобразования Галилея.
- •Импульс частицы (количество движения)
- •Второй закон Ньютона. Понятие силы. Масса – мера инертности. Определение силы.
- •Закон независимости действия сил (принцип суперпозиции сил). Равнодействующая сил.
- •Интегральное выражение основного закона динамики. Понятие импульса силы.
- •Третий закон Ньютона.
- •Динамика систем материальных точек. Обобщение II закона Ньютона для системы материальных точек. Импульс системы. Закон сохранения импульса системы.
- •Центр инерции системы частиц (тела). Закон аддитивности массы.
- •Интегральное выражение основного закона динамики системы частиц. Закон сохранения проекции импульса системы.
- •Классификация сил. Фундаментальные воздействия. Законы эмпирических сил.
- •Закон всемирного тяготения.
- •Однородное поле тяжести Земли.
- •Понятие веса тела.
- •Упругие деформации. Закон Гука.
- •Силы трения.
- •Сухое трение.
- •Трение покоя.
- •Трение скольжения.
- •Трение качения.
- •Вязкое трение.
- •Сила сопротивления.
- •Сила Архимеда.
- •Реактивная сила.
- •Механическая энергия и её виды. Закон сохранения механической энергии.
- •Консервативные и неконсервативные силы.
- •Закон сохранения механической энергии.
- •Потенциальная энергия упругих взаимодействий.
- •Потенциальная энергия тяготения.
- •Теорема о потенциальной энергии. Связь между консервативной силой и потенциальной энергией.
- •Потенциальные кривые.
- •Основной закон динамики вращательного движения. Закон сохранения момента импульса системы частиц (тела).
- •Динамика материальной точки
- •Динамика системы материальных точек
- •Динамика вращательного движения тела относительно неподвижной оси.
- •Элементы динамики твёрдого тела.
- •Закон сохранения момента импульса относительно оси.
- •Кинетическая энергия вращения твёрдого тела.
- •Плоское движение твёрдого тела.
- •Теорема Штейнера.
- •Работа момента силы относительно оси.
- •Заключение.
- •Основы молекулярной физики и термодинамики. Введение
- •Элементы молекулярно-кинетической теории. Основные представления и понятия.
- •Модель идеального газа. Уравнение состояния идеального газа.
- •Основное уравнение молекулярно-кинетической теории идеального газа.
- •Температура
- •Тепловая скорость молекул газа.
- •Вывод уравнения состояния идеального газа.
- •Барометрическая формула. Закон Больцмана.
- •Закон равномерного распределения энергии по степеням свободы молекул газа.
- •Внутренняя энергия идеального газа.
- •Распределение молекул по скоростям (закон Максвелла).
- •Распределение по кинетическим энергиям поступательного движения молекул газа.
- •Явление переноса
- •Явление теплопроводности. Закон Фурье.
- •Явление диффузии. Закон Фика
- •Вязкое трение. Закон ньютона.
- •Явление переноса в газах.
- •Средняя частота столкновений и средняя длина свободного пробега молекул газа.
- •Диффузия в газах.
- •Теплопроводность газов.
- •Вязкость газов.
- •Внутренняя энергия термодинамической системы. Работа и теплота как обобщённые формы обмена энергией в термодинамике.
- •Первое начало термодинамики.
- •Равновесные процессы.
- •Применение первого начала термодинамики к равновесным процессам с идеальным газом. Изотермический процесс.
- •Изохорный процесс.
- •Изобарный процесс.
- •Адиабатный процесс.
- •Политропный процесс.
- •Круговые процессы. Цикл Карно. Кпд тепловых машин.
- •Второе начало термодинамики.
- •Теорема Карно и Клаузиуса.
- •Энтропия.
- •Основное уравнение термодинамики обратимых процессов.
- •Примеры расчёта энтропии для обратимых процессов. Энтропия идеального газа.
- •Изменение энтропии при обратимом нагреве (охлаждении) жидких и твёрдых тел.
- •Изменение энтропии при фазовых превращениях.
- •Подведём итоги об энтропии и её свойствах.
- •Примеры роста энтропии в изолированных системах.
- •Расширение идеального газа в пустоту.
- •Формула Больцмана. Статистический смысл энтропии.
Основное уравнение термодинамики обратимых процессов.
![]() Так
как энтропия является функцией состояния,
то её можно использовать как параметр
состояния при анализе термодинамических
процессов. Выразим
Так
как энтропия является функцией состояния,
то её можно использовать как параметр
состояния при анализе термодинамических
процессов. Выразим
![]() и подставим в выражение первого начала
термодинамики:
и подставим в выражение первого начала
термодинамики:
![]() .
.
Это и есть основное уравнение термодинамики обратимых процессов.
Для адиабатного обратимого процесса:
![]()
 ,
,
![]() .
.
В обратимом адиабатном процессе энтропия сохраняется. Поэтому адиабатный обратимый процесс называют изоэнтропийным.
Цикл Карно наиболее просто и наглядно
выглядит в параметрах
![]() и
и
![]() (см.
диаграмму). Размерность диаграммы:
(см.
диаграмму). Размерность диаграммы:
![]() .
.
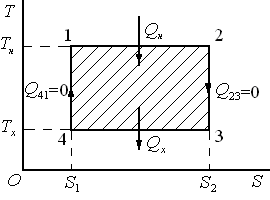
На диаграмме изображён цикл Карно в режиме теплового двигателя.
Для изотермических процессов расширения и сжатия находим:
![]() ,
,
![]() .
.
КПД теплового двигателя Карно равен:
![]() .
.
Работа за цикл равна заштрихованной площади на диаграмме:
![]() .
.
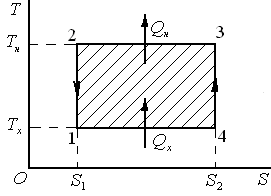
Если запустить тепловую машину Карно против часовой стрелки (см. диаграмму), то она будет работать в режиме холодильной установки или теплового насоса.
![]() ,
,
![]() ,
,
![]() ,
,
КПД холодильной машины и теплового насоса соответственно равны:
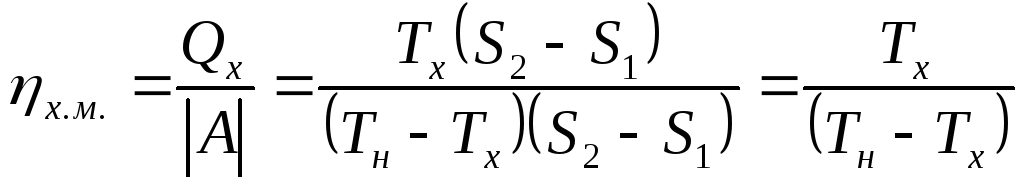 ,
,
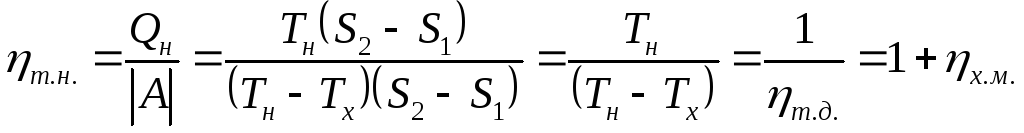
Примеры расчёта энтропии для обратимых процессов. Энтропия идеального газа.
Найдём изменение энтропии идеального газа:
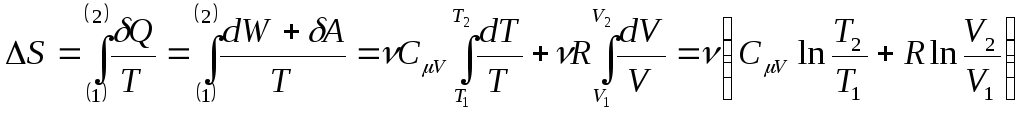 .
.
С точностью до постоянной
![]() энтропия идеального газа равна:
энтропия идеального газа равна:
![]() ,
,
так как
![]() .
.
Энтропия пропорциональна числу молей
газа
![]() ,
т.е. является величиной аддитивной.
,
т.е. является величиной аддитивной.
В большинстве случаев, при решении термодинамических задач знание абсолютного значения энтропии не требуется. Термодинамические процессы определяются изменением энтропии. Поэтому выбор начала отсчёта энтропии может быть произвольным.
Рассмотрим частные случаи изменения энтропии идеального газа:
1)
![]() ,
,
![]() ;
;
2)
![]() ,
,
![]() ;
;
3)
![]() ,
,
![]() ;
;
4) Адиабатный процесс,
![]() ;
;
5) Политропный процесс,
![]() ,
где
,
где
![]() .
.
Изменение энтропии при обратимом нагреве (охлаждении) жидких и твёрдых тел.
Для жидких и твёрдых тел
![]() .
Поэтому при обратимом теплообмене
теплота равна:
.
Поэтому при обратимом теплообмене
теплота равна:
![]() .
.
Изменение энтропии:
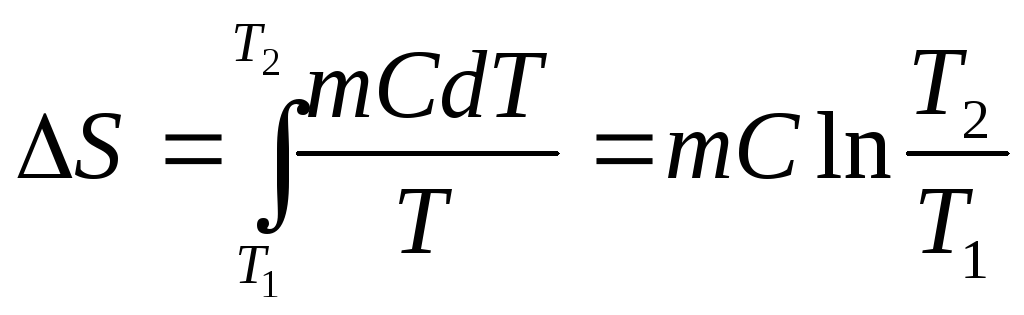 ,
,
если можно пренебречь зависимостью
![]() от
от
![]() .
.
При
![]() (нагрев)
(нагрев)
![]() ,
при
,
при
![]() (охлаждение)
(охлаждение)
![]() .
.
Изменение энтропии при фазовых превращениях.
Фазовые превращения протекают при фиксированной температуре, значение которой зависит от давления.
При плавлении твёрдых тел или отвердевании жидкости поглощается или выделяется теплота, равная:
![]() ,
,
где
![]() - называется удельной теплотой плавления
твёрдого тела или удельной теплотой
отвердевания жидкости,
- называется удельной теплотой плавления
твёрдого тела или удельной теплотой
отвердевания жидкости,
![]() - масса тела.
- масса тела.
При плавлении температура растёт:
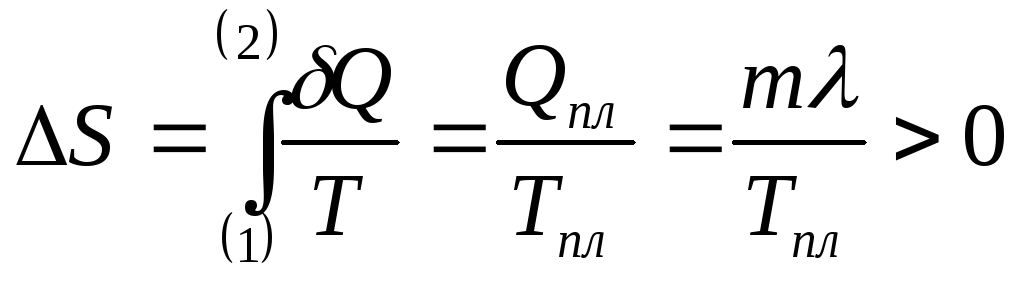 ,
,
где
![]() - температура плавления.
- температура плавления.
При отвердевании энтропия уменьшается.
Кипение жидкости протекает при постоянной температуре, величина которой зависит от давления, и сопровождается процессом парообразования. При этом тепло поглощается:
![]() ,
,
где
![]() - называется удельной теплотой
парообразования,
- называется удельной теплотой
парообразования,
![]() - масса жидкости.
- масса жидкости.
Процесс парообразования сопровождается ростом энтропии:
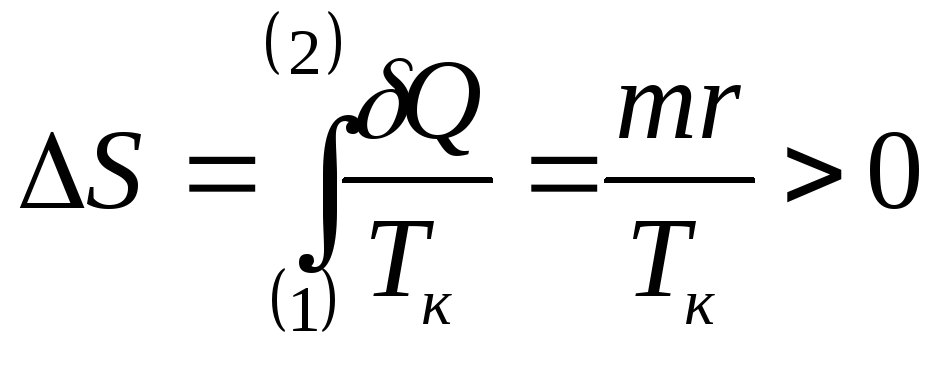 ,
,
где
![]() - температура кипения жидкости.
- температура кипения жидкости.
При конденсации теплота выделяется и энтропия уменьшается.
В процессах фазовых превращений твёрдого тела в жидкость, жидкости в газ энтропия растёт:
![]() .
.
С точки зрения МКТ газу соответствует наибольший беспорядок, чем жидкости и твёрдому телу. В этом смысле энтропию можно представить как меру беспорядка.
