
- •И.С. Колпащикова, е.Р. Кофанов, е.М. Алов углеводороды. Галогенпроизводные углеводородов
- •1. Алканы
- •1.1. Гомологический ряд, изомеры
- •Гомологический ряд алканов. Число структурных изомеров
- •1.2. Строение метана
- •1.3. Строение этана
- •1.4. Вращение вокруг простой углерод-углеродной связи. Конформации
- •1.5. Физические свойства
- •1.6. Химические свойства
- •1.6.1. Хлорирование и бромирование метана. Механизм реакции
- •1.6.2. Строение метильного радикала
- •1.6.3. Расчет изменения энергии в ходе реакции
- •1.6.4. Энергетическая диаграмма реакции. Связь энергии
- •Хлорирования метана
- •Бромирования метана
- •1.6.5. Причина различной реакционной способности галогенов
- •Зависимость реакционной способности галогенов от энергии связи h–Hal
- •1.6.6. Галогенирование высших алканов. Механизм
- •1.6.7. Медленная стадия. Энергетическая диаграмма
- •1.6.8. Причина различной устойчивости радикалов
- •1.6.9. Зависимость скорости образования радикалов
- •1.6.10. Расчет реакционной способности различных связей
- •1.6.11. Селективность в реакциях хлорирования
- •Малореакционного Br• с пропаном
- •1.6.12. Нитрование
- •1.6.13. Сульфоокисление и сульфохлорирование
- •1.6.14. Окисление
- •1.6.15. Термическое разложение алканов, крекинг
- •1.6.16. Ионные реакции алканов
- •1.7. Методы синтеза алканов
- •1.7.1. Гидрирование алкенов и алкинов
- •1.7.2. Реакция Вюрца
- •2.2. Плоскополяризованный свет. Оптическая активность
- •2.3. Строение молекул и оптическая активность
- •2.4. Обозначение конфигураций
- •2.5. Соединения с несколькими хиральными центрами.
- •2.6. Методы разделения энантиомеров
- •3. Циклоалканы
- •3.1 Номенклатура. Изомерия
- •3.2. Физические свойства
- •3.3. Строение
- •Теплоты сгорания и энергии напряжения циклоалканов
- •3.4. Химические свойства
- •3.5. Способы получения
- •4.2. Строение этена
- •4.3. Физические свойства
- •Физические свойства алкенов
- •4.4. Химические свойства
- •4.4.1. Гидрирование. Теплота гидрирования
- •4.4.2. Теплота гидрирования и устойчивость алкенов
- •4.4.3. Присоединение галогенов
- •4.4.3.1. Механизм реакции
- •4.4.3.2. Реакционная способность галогенов в реакции АdЕ
- •4.4.4. Присоединение галогеноводородов
- •4.4.4.1. Механизм реакции
- •4.4.4.2. Направление электрофильного присоединения
- •К пропену
- •4.4.4.3. Реакционная способность и селективность
- •4.4.4.4. Перегруппировка
- •Механизм реакции
- •4.4.5. Присоединение бромистого водорода в присутствии
- •1. Инициирование:
- •2. Рост цепи:
- •3. Обрыв цепи:
- •4.4.6. Присоединение серной кислоты
- •4.4.7. Гидратация алкенов. Присоединение спиртов
- •4.4.8. Гидроборирование алкенов
- •4.4.9. Алкилирование алкенов
- •4.4.10. Полимеризация алкенов
- •4.4.11. Окисление
- •4.4.12. Реакция аллильного замещения. Галогенирование
- •Характеристики химических связей в молекуле алкинов
- •Характеристики связей с-н в алканах, алкенах и алкинах
- •5.2. Физические свойства
- •5.3. Химические свойства
- •5.3.1. Реакции присоединеня
- •5.3.1.1. Каталитическое гидрирование и восстановление
- •5.3.1.2. Реакции электрофильного присоединения Галогенирование
- •Гидрогалогенирование
- •Гидратация
- •5.3.1.3. Нуклеофильное присоединение
- •5.3.2. Кислотность алкинов
- •Константы кислотности некоторых соединений
- •5.3.3. Взаимодействие алкинов с карбонильными соединениями
- •5.3.4. Окисление алкинов
- •5.3.5. Радикальное присоединение бромоводорода
- •5.4. Способы получения
- •6. Диены
- •6.1. Устойчивость сопряженных диенов
- •Теплоты гидрирования алкенов и диенов
- •Гибридизация атомов углерода и длины простых углерод-углеродных связей
- •6.2. Химические свойства
- •6.2.1. Электрофильное присоединение
- •6.2.3. Диеновый синтез. Реакция Дильса-Альдера
- •6.2.4. Полимеризация
- •6.3. Способы получения
- •7. Арены
- •7.1. Сравнение свойств бензола со свойствами алкенов
- •Сравнение химических свойств циклогексена и бензола
- •7.2. Теплота гидрирования. Энергия резонанса
- •7.3. Строение бензола
- •7.4. Ароматичность
- •7.5. Физические свойства
- •Физические свойства аренов
- •7.6. Химические свойства
- •7.6.1. Электрофильное замещение
- •7.6.1.1. Нитрование
- •Превращения -комплекса
- •1.6.1.2. Галогенирование
- •7.6.1.3. Сульфирование
- •7.6.1.3. Алкилирование по Фриделю-Крафтсу
- •7.6.1.4. Ацилирование
- •7.6.1.5. Хлорметилирование
- •7.6.1.6. Формилирование
- •7.6.2. Свободнорадикальное замещение в боковой цепи аренов
- •7.6.3. Реакции окисления
- •7.7. Методы синтеза
- •8. Электрофильное замещение в производных
- •8.1. Влияние заместителей на реакционную способность
- •8.2. Механизм ориентации - влияние заместителей на выбор
- •Классификация заместителей. Электронные эффекты
- •9. Многоядерные ароматические соединения
- •9.1. Нафталин
- •9.1.1. Строение нафталина
- •9.1.2. Химические свойства
- •9.1.2.1. Реакции электрофильного замещения
- •9.1.2.2. Ориентация в реакциях электрофильного замещения
- •9.1.2.3. Восстановление и окисление нафталина
- •9.2. Антрацен и фенантрен
- •10. Гетероциклические соединения
- •10.1. Пятичленные гетероциклы
- •10.1.1. Строение
- •10.1.2. Химические свойства
- •10.1.3. Способы получения
- •10.2. Пиридин
- •10.2.1. Строение пиридина
- •10.2.2. Химические свойства
- •10.3. Хинолин
- •11. Галогеналканы
- •11.1. Нуклеофильное замещение
- •Реакции нуклеофильного замещения
- •11.1.1. Бимолекулярное нуклеофильное замещение
- •Бимолекулярного нуклеофильного замещения, sn2 - процесс согласованный одностадийный:
- •11.1.2. Мономолекулярное нуклеофильное замещение
- •Мономолекулярного нуклеофильного замещения. Sn1-двухстадийный процесс
- •Мономолекулярного нуклеофильного замещения
- •11.1.3. Сравнение реакций sn 1 и sn 2
- •Влияние условий реакции на относительное значение двух механизмов
- •11.1.4. Амбидентные ионы
- •11.2. Реакции отщепления (элиминирование)
- •11.2.1. Бимолекулярное отщепление е2
- •Состав продуктов е2-реакции 2-замещенных пентанов (под действием c2h5oөk)
- •Состав продуктов реакции трет-пентилбромида с алкоголятами калия roөk (70-75о с)
- •5.2.2. Мономолекулярное отщепление е1
- •11.2.3. Сравнение реакций нуклеофильного замещения и элиминирования
- •12.2. Нуклеофильное замещение, протекающее через стадию образования дегидробензола. Отщепление – присоединение
- •12.3. Бимолекулярное нуклеофильное замещение путем
- •12.4. Ориентация при нуклеофильном замещении
- •13. Магнийорганические соединения
- •13.1. Получение и строение магнийорганических соединений
- •13.2. Синтез спиртов и кислот
- •Оглавление
- •Углеводороды. Галогенпроизводные углеводородов
- •150023, Ярославль, Московский пр., 88
- •150000, Ярославль, ул. Советская, 14а
- •И.С. Колпащикова, е.Р.Кофанов, е.М.Алов
- •Углеводороды.
- •Галогенпроизводные углеводородов
13.2. Синтез спиртов и кислот
Магнийорганические соединения присоединяются к карбонильным соединениям по двойной связи углерод - кислород.
Для синтеза первичных спиртов используют в качестве карбонильного соединения муравьиный альдегид.
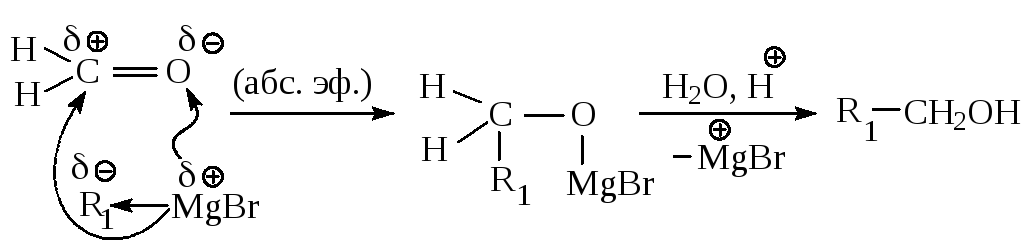
Для получения первичных спиртов, содержащих на два атома углерода больше, чем в магнийорганическом исходном соединении, используют окись этилена.
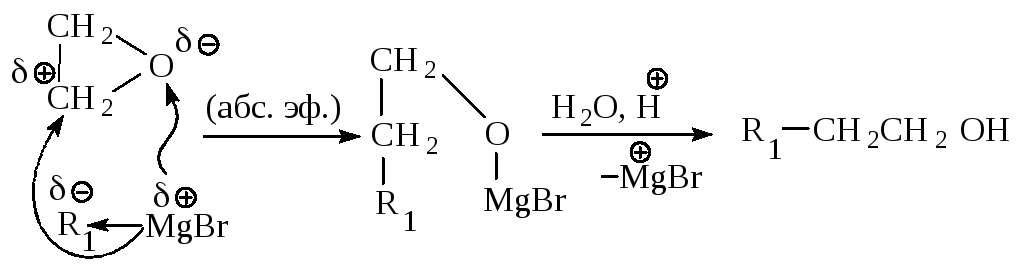
Для получения вторичных спиртов в качестве карбонильного соединения используют соответствующий альдегид.
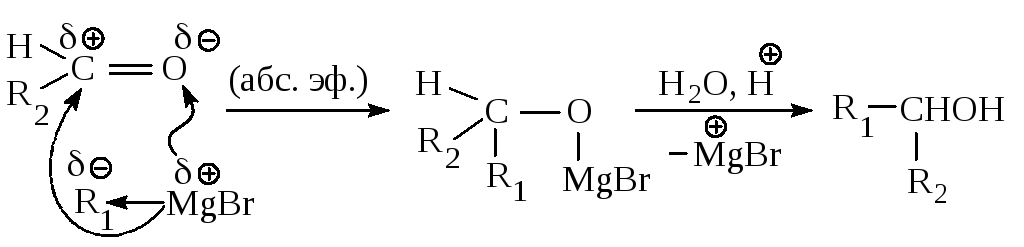
В случае синтеза третичных спиртов исходное карбонильное соединение - кетон.
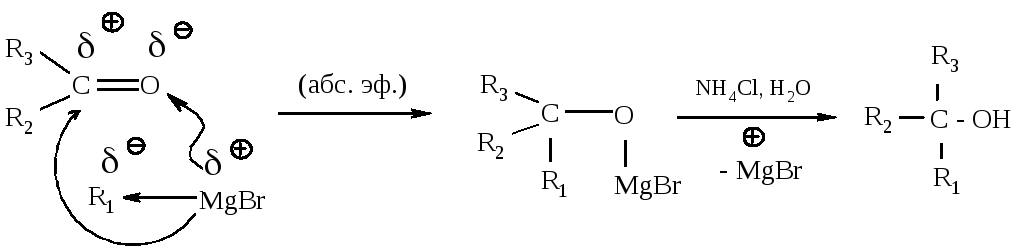
Как выбрать карбонильное соединение для синтеза определенного спирта? Предположим, необходимо получить 2-фенил-2-бутанол. Мысленно расщепляем молекулу спирта около углерода, несущего спиртовую группу. Та часть молекулы, которая содержит кислород, входила в исходное карбонильное соединение, другая - в реактив Гриньяра.
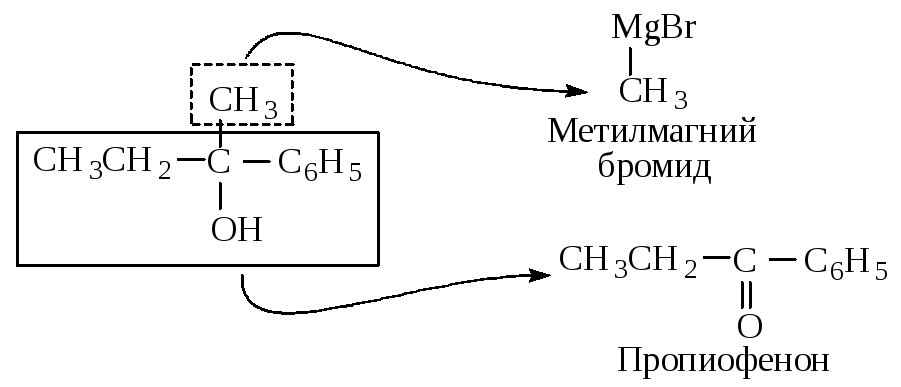
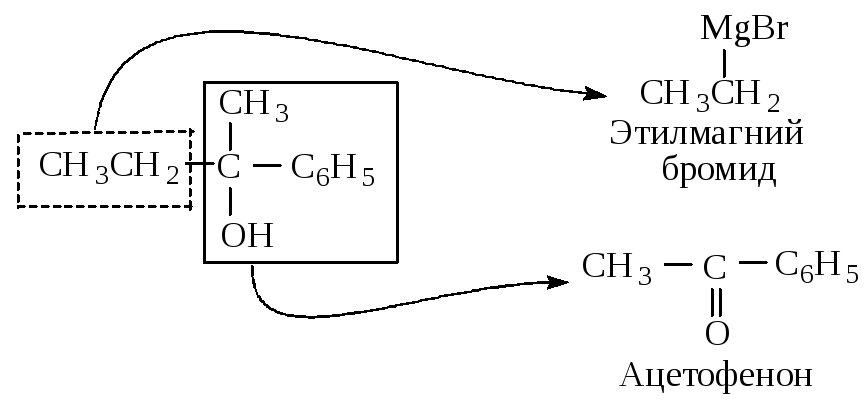
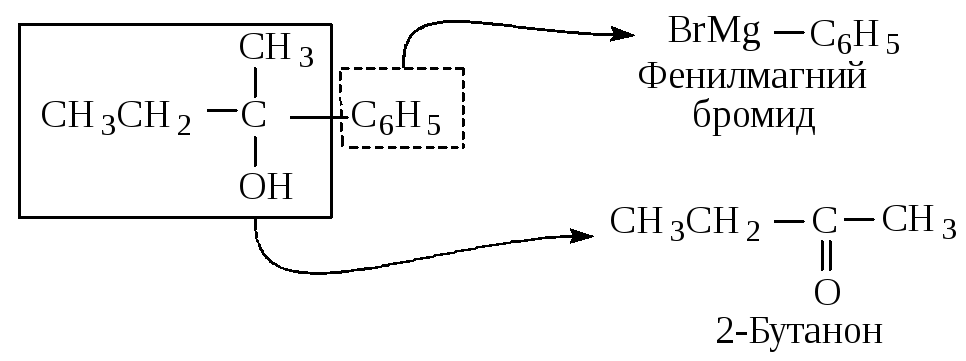
Таким образом, для синтеза указанного спирта можно выбрать три пары соединений.
Получение карбоновых кислот. При взаимодействии реактива Гриньяра с углекислым газом происходит присоединение его по двойной связи, как и в реакции с карбонильными соединениями, в результате образуется соль, из которой карбоновую кислоту выделяют действием разбавленного раствора минеральной кислоты.
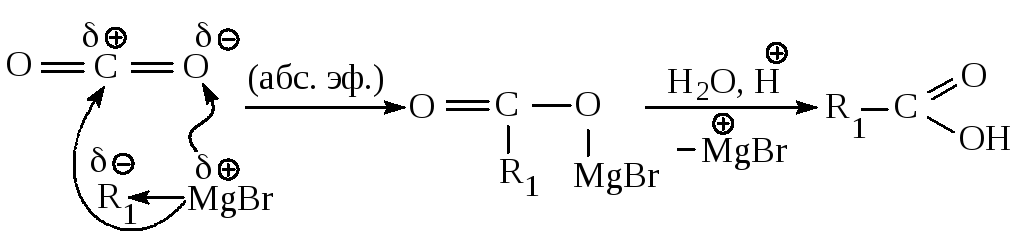
Библиографический список
-
Моррисон, Р. Органическая химия. – М. : Мир, 1974. – 1132 с.
-
Терней, А. Современная органическая химия : 2 т. – М. : Мир, 1991. – Т. 1. – 670 с.; Т. 2. – 615 с.
-
Робертс, Дж. Основы органической химии : в 2 т. / Дж. Моррисон, М. Кассерио. – 2-е изд. – М. : Мир, 1978. – Т. 1. – 842 с.; Т. 2. – 888 с.
-
Шабаров, Ю. С. Органическая химия : в 2 кн. – М. : Химия, 1994. – 848 с.
-
Травень, В. Ф. Органическая химия : 2 т. – М. : ИКЦ Академкнига, 2004. – Т. 1. – 727 с.; Т. 2. – 582 с.
Оглавление
|
1.АЛКАНЫ…………………………………………………….. |
3 |
|
3 |
|
4 |
|
6 |
|
1.4. Вращение вокруг простой углерод-углеродной связи. Конформации………………………………………………… |
6 |
|
1.5. Физические свойства …………………………………………. |
8 |
|
10 |
|
31 |
|
2. СТЕРЕОИЗОМЕРИЯ. ЭНАНТИОМЕРИЯ …………....... |
34 |
|
34 |
|
38 |
|
40 |
|
40 |
|
2.5. Соединения с несколькими хиральными центрами. Диастереомеры. Рацемат. Мезо-формы ……………………... |
43 |
|
2.6. Методы разделения энантиомеров …………………………... |
46 |
|
3. ЦИКЛОАЛКАНЫ ………………………………………………. |
46 |
|
3.1. Номенклатура. Изомерия ……………………………………... |
46 |
|
47 |
|
48 |
|
54 |
|
55 |
|
4. АЛКЕНЫ …………………………………………………... |
56 |
|
56 |
|
58 |
|
61 |
|
63 |
|
92 |
|
5.АЛКИНЫ ………………………………………………….. |
93 |
|
5.1. Строение ацетилена …………..……………………………. |
94 |
|
5.2. Физические свойства ……………………………………….. |
97 |
|
5.3. Химические свойства ..…………………………………….. |
97 |
|
5.4. Способы получения ………..………………………………. |
108 |
|
6. ДИЕНЫ ……………………………………………………… |
109 |
|
6.1. Устойчивость сопряженных диенов ……………………….. |
110 |
|
6.2. Химические свойства ……………………………………….. |
112 |
|
6.3. Способы получения ………...………………………………. |
122 |
|
7. АРЕНЫ ………………………………………………………… |
123 |
|
7.1. Сравнение свойств бензола со свойствами алкенов ……… |
123 |
|
7.2. Теплота гидрирования. Энергия резонанса ……………….. |
124 |
|
7.3. Строение бензола ………..…………………………………. |
125 |
|
7.4. Ароматичность ………………..……………………………. |
127 |
|
7.5. Физические свойства ……………………………………….. |
127 |
|
7.6. Химические свойства ……………………………………….. |
130 |
|
7.7. Методы синтеза ………………………..…………………… |
150 |
|
8. ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ В ПРОИЗВОДНЫХ БЕНЗОЛА …………………………………………………… |
150 |
|
8.1. Влияние заместителей на реакционную способность бензольного кольца ……………………………………………… |
154 |
|
8.2. Механизм ориентации - влияние заместителей на выбор места электрофильной атаки |
157 |
|
9. МНОГОЯДЕРНЫЕ АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ |
165 |
|
9.1. Нафталин …………………………………………………….. |
165 |
|
9.2. Антрацен и фенантрен ……………………………………… |
171 |
|
10. ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ ….………….. |
173 |
|
10.1. Пятичленные гетероциклы ……..………………………… |
173 |
|
10.2. Пиридин ……..…………………………………………….. |
178 |
|
10.3 Хинолин …………………………………………………….. |
183 |
|
11. ГАЛОГЕНАЛКАНЫ ……………………………………… |
185 |
|
11.1. Нуклеофильное замещение …………..…………………… |
186 |
|
11.2. Реакции отщепления (элиминирование) ………..……….. |
202 |
|
11.3. Методы синтеза галогеналканов ………………………….. |
211 |
|
12. ГАЛОГЕНАРЕНЫ …………………...……………………… |
211 |
|
12.1 Причина низкой реакционной способности галогенаренов |
212 |
|
12.2. Нуклеофильное замещение, протекающее через стадию образования дегидробензола. Отщепление - присоединение |
212 |
|
12.3. Бимолекулярное нуклеофильное замещение путем присоединения - отщепления ……………………………….… |
213 |
|
12.4. Ориентация при нуклеофильном замещении в ароматическом кольце ……………………………………………… |
217 |
|
13. МАГНИЙОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ ………….. |
218 |
|
13.1. Получение и строение магнийорганических соединений . |
218 |
|
13.2. Синтез спиртов и кислот …………..……………………... |
219 |
|
БИБЛИОГРАФИЧЕСКИЙ СПИСОК ..……………………… |
222 |
Учебное издание
