
- •Лабораторная работа технология мазей. Определение in vitro биологической доступности Лекарственных Веществ из мазей.
- •1. Цели занятия:
- •1. Информационный материал
- •1.1. Биологическая доступность (бд) лекарственных веществ (лв).
- •1.2. Характеристика мазей как лекарственной формы
- •Растворимость некоторых лв, используемых в технологии мягких лс
- •1.3. Технология суспензионных мазей в лабораторных условиях:
- •1.4. Высвобождение лекарственных веществ из суспензионных мазей.
- •2. Методические указания к Самостоятельной работе
- •2.1. Приготовьте мазь салициловую 5% на различных мазевых основах в количестве 20 г.
- •2.2. Составьте материальный баланс.
- •2.4. Изучите влияние природы мазеобразующих вспомогательных веществ (мазевых основ) на процесс высвобождения лв из мазей
2.2. Составьте материальный баланс.
Рассчитайте выход, трату и общий расходный коэффициент (см. лекционный материал). Составьте рабочую пропись на 1 кг мази с учетом расходного коэффициента.
2.3. Определите показатели качества изготовленной мази и ее тип по дисперсологической классификации (мазь-раствор, мазь-суспензия или мазь-эмульсия).
Определите и запишите в протокол:
- для суспензионной мази – дисперсность ЛВ (размер частиц ЛВ);
- для эмульсионной мази – тип эмульсии.
Методика определения дисперсности (размера частиц ЛВ) в мази.
Размер частиц лекарственного вещества определяют микроскопически (ГФ РБ).
Если концентрация лекарственных веществ в мазях превышает 10%, то их разбавляют основой соответственно до содержания около 10% и перемешивают.
Навеску мази ≈ 0,05 г помещают на предметное стекло или камеру Горяева. Предметное стекло помещают на водяную баню до расплавления основы. К расплавленной на предметном стекле мази прибавляют:
- 1каплю 0,1 % раствора судана III - для жировых, углеводородных и эмульсионных основ типа в/м; или
- 1 каплю 0,15 % раствора метиленового синего - для гидрофильных и эмульсионных основ типа м/в.
Мазь и краситель перемешивают. Пробу накрывают покровным стеклом (24 х 24 мм), фиксируют путем слабого надавливания пинцетом и просматривают в 4 полях зрения. Определяют размер частиц. Максимальный размер частиц заносят в протокол. Делают вывод о соответствии требованиям ФС.
В поле зрения микроскопа должны отсутствовать частицы, размер которых превышает нормы, указанные в частных статьях. Если таких указаний нет, то размер частиц не должен превышать 50 мкм для дерматологических и 10 мкм для глазных мазей.
2.4. Изучите влияние природы мазеобразующих вспомогательных веществ (мазевых основ) на процесс высвобождения лв из мазей
Пробы приготовленных мазей аккуратно с помощью шпателя наносят равномерным слоем на диффузионную среду, вытесняя воздух и не допуская образования воздушных зазоров между средой и слоем мази. Все образцы мазей наносятся одновременно на поверхность агарового геля в пробирках. Пробирки маркируются для идентификации мазевых основ.
Диффузионная среда для испытаний – это 2% агаровый гель, в котором растворен железа (Ш) хлорид. По мере диффузии салициловой кислоты из мази в агаровый гель, последний будет окрашиваться ввиду образования комплекса железа с салициловой кислотой:
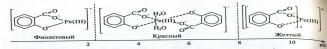
Области устойчивости салицилатов железа при различных значениях рН
Отмечают время и наблюдают за скоростью и полнотой диффузии ЛВ в агаровый гель. Скорость и полноту диффузии салициловой кислоты в агаровый гель определяют по изменению окраски геля. Через 15, 30 и 45 минут определяют величину зоны диффузии в миллиметрах. Заносят в дневник наблюдений.
По результатам работы постройте диаграммы (графики) зависимости величины зоны диффузии высвободившегося ЛВ от времени. На оси абсцисс откладывают время измерения величины зоны диффузии; на оси ординат – величину зоны диффузии в мм.
Приведите данные для трех видов мазей - на гидрофобной основе, на гидрофильной основе, на дифильной основе (в т.ч. полученные другими студентами) - и сравните их между собой. На основании сравнения и анализа полученных результатов сделайте выводы о биологической доступности салициловой кислоты из мазей, приготовленных на различных мазевых основах.
2.5. Оформите протокол, включающий разделы:
-
назначение основных и вспомогательных веществ;
-
обоснование и расчет состава по основным и вспомогательным веществам;
-
технологическая и аппаратурная схемы процесса;
-
изложение технологического процесса по стадиям и операциям;
-
материальный баланс и рабочая пропись на 1 кг продукта
-
результаты определения типа изготовленной мази по дисперсологической классификации.
-
Результаты определения размера частиц ЛВ и типа эмульсии
-
сравнительные результаты высвобождения салициловой кислоты из мазей на различных основах
Контрольные вопросы
-
Дайте определение биодоступности ЛВ в соответствии с ГФ РБ
-
Дайте определение абсолютной и относительной биодоступности ЛС
-
Перечислите методы определения биодоступности ЛС и области их применения
-
Дайте характеристику мазям как лекарственной форме. Какие ингредиенты входят в состав мазей?
-
Какова роль основы в составе мази?
-
Классификация мазей как дисперсных систем.
-
Что такое мази-растворы и суспензионные мази?
-
Факторы, влияющие на биодоступность суспензионных мазей?
-
Перечислите основные стадии технологии мазей растворов и суспензионных мазей.
-
Какое оборудование используется для изготовления суспензионных мазей в промышленных условиях?
-
Как определяется размер частиц лекарственных веществ в суспензионных мазях?
-
Мазевые основы. Классификация. Примеры
-
Перечислите требования, предъявляемые к мазям.
-
В каких случаях в технологическую схему следует включать стадию приготовления концентрата?
-
Что понимают под однородностью мази?
-
Подготовка мазевой основы к введению ЛВ
-
Подготовка ЛВ к введению в мазевые основы
Литература
1. ГФ РБ, 2006, т.1, раздел 5.8. «Биодоступность и биоэквивалентность генерических ЛС», с. 580-597.
2. А.И.Тихонов, Т.Г.Ярных и др. Биофармация // учебник для студентов фармацевтических вузов. Харьков, изд. НФаУ, 2003 г.
3. Технология лекарственных форм / под ред. Л.А.Ивановой. Т. 2. — М.: Медицина, 1991. С. 503-509.
4. Чуешов В.И. Промышленная технология лекарств // Учебник в 2-х томах. Харьков. НФАУ. 2002. Т.2, с. 428-443
5. Муравьев И. А. Технология лекарств. Т. 2. — М.: Медицина, 1980. С. 484-524.
6. Тенцова А.И., Грецкий В.М. Современные аспекты исследования и производства мазей. — М.: Медицина, 1980.
