
- •Патофизиология эндокринной системы. Нарушение функций гипофиза, надпочечников. Патофизиология щитовидной, паращитовидных, половых желез.
- •Патофизиология эндокринной системы. Нарушение функций гипофиза, надпочечников. Патофизиология щитовидной, паращитовидных, половых желез.
- •Основные учебные вопросы:
- •Функциональные пробы
- •Контрольные вопросы по теме:
- •Литература:
(для внутрикафедрального пользования)
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РЕСПУБЛИКИ БЕЛАРУСЬ
УО «ГОМЕЛЬСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ»
Кафедра патологической
физиологии
Утверждено на заседании кафедры
протокол № 7 от 31.08.2010
Зав. кафедрой патофизиологии, к.м.н.
доцент_____________Т.С. Угольник
Патофизиология эндокринной системы. Нарушение функций гипофиза, надпочечников. Патофизиология щитовидной, паращитовидных, половых желез.
Учебно-методическая разработка для студентов
лечебного факультета
Гомель 2011
Патофизиология эндокринной системы. Нарушение функций гипофиза, надпочечников. Патофизиология щитовидной, паращитовидных, половых желез.
Автор-составитель: Чубуков Ж.А.
Актуальность темы: Эндокринная система, совместно с нервной, участвует в регуляции основных физиологических процессов в организме. Нарушение центральных механизмов регуляции функциональной активности эндокринных желез, патологические процессы в самих железах или нарушение периферического механизма действия гормонов приводят к нарушению метаболизма, роста, развития и размножения организма. Неспецифическая резистентность организма и ее нарушения также связаны с функционированием эндокринных желез: гипофиза и надпочечных желез. Участие гормональных факторов в патогенезе не только эндокринных, но и неэндокринных заболеваний обуславливает необходимость изучения патологии эндокринной системы.
Цель занятия: изучить этиологию и патогенез нарушений эндокринной системы
Задачи занятия:
-
Знать основные механизмы нарушения функциональной активности эндокринных желез.
-
Уметь объяснить нарушения центральной регуляции функционирования эндокринных желез, роль механизма "обратной связи" в патогенезе эндокринных расстройств.
-
Знать первичные нарушения синтеза гормонов в периферических эндокринных железах, генетически обусловленные дефекты биосинтеза гормонов.
-
Знать периферические формы эндокринных расстройств.
-
Усвоить основные типы эндокринных расстройств, принципы классификации, общую характеристику.
-
Охарактеризовать патологию гипоталамо-гипофизарной системы.
-
Назвать этиологические факторы, вызывающие нарушение функции надпочечников, объяснить патогенез, морфофункциональные проявления, уметь охарактеризовать "скрытые" формы недостаточности надпочечников.
-
Знать значение ГГНСА для неспецифической резистентности организма и ее нарушений.
-
Знать этиологические факторы, вызывающие нарушения функции щитовидной железы.
-
Уметь охарактеризовать основные проявления гипер- и гипотиреозов.
-
Объяснить механизмы развития гипер- и гипотиреозов и их основные проявления.
-
Уметь раскрыть роль аутоиммунных механизмов в развитии эндокринных нарушений.
-
Назвать этиологические факторы и основные клинические проявления нарушения функции околощитовидных желез.
-
Объяснить механизмы развития гипо- и гипергонадизма у женщин и мужчин.
-
Знать общие принципы диагностики и терапии эндокринных расстройств.
-
Уметь объяснить механизмы развития ятрогенных эндокринопатий.
Основные учебные вопросы:
-
Общая этиология и патогенез эндокринных расстройств. Нарушение центральной регуляции желез внутренней секреции. Избыток, недостаток и нарушение баланса рилизинг- и ингибирующих факторов межуточного мозга (либеринов и статинов).
-
Нарушение обратных связей и механизмов саморегуляции в нейроэндокринной системе, транс-, параадено-гипофизарные механизмы регуляторных расстройств.
-
Первичные нарушения синтеза гормонов в периферических эндокринных железах как следствие патологических процессов в ткани железы, истощения на почве длительной гиперфункции, дефицита субстратов для синтеза гормонов; генетических дефекты биосинтеза гормонов.
-
Психогенные эндокринопатии. Ятрогенные эндокринопатии.
-
Периферические механизмы нарушения реализации эффектов гормонов: нарушение связывания и «освобождения» гормонов белками крови, блокады, чрезмерное разрушение и нарушение метаболизма в тканях, отсутствие или изменение свойств гормональных рецепторов в клетках-мишенях.
-
Основные типы эндокринных расстройств: принципы классификации, общая характеристика.
-
Патология гипоталамо-гипофизарной системы. Гипер- и гипофункция передней и задней доли гипофиза. Тотальная недостаточность гипофиза.
-
Патофизиология надпочечников. Типовые формы патологии (гипо- и гиперфункциональные состояния) механизмы развития, проявления.
-
Патофизиология щитовидной железы. Этиология, патогенез, клинические проявления гипо- и гипертиреозов, тиреотоксикоз.
-
Этиология, патогенез клинические проявления гипертиреозов. Тиреотоксикоз.
-
Патофизиология околощитовидных желез: гипопаратиреоз, гиперпаратиреоз.
-
Патофизиология половых желез: гипо- и гипергонадизм у женщин и мужчин.
-
Нарушение эндокринной функции поджелудочной железы.
-
Дисгормональные расстройства материнского организма, их значение в развитии эндокринопатий плода.
-
Общая характеристика методов обнаружения и принципов терапии эндокринных расстройств. Роль эндокринных расстройств в этиологии и патогенезе неэндокринных заболеваний.
Эндокринная система — это совокупность анатомически, гистологически, цитологически дифференцированных структур, вырабатывающих гормоны.
Гормоны — это органические сигнальные молекулы, секретируемые клетками во внутреннюю среду, связывающиеся с рецепторами клеток-мишеней и изменяющие режим их функционирования.
Гипофиз и гипоталамус представляют собой единую регуляторную систему, «центральное звено» в гормональной регуляции, которое следует воспринимать как единый нейрогуморальных комплекс - гипоталамо-гипофизарный нейросекреторный аппарат.
Аденогипофиз является ключевым регулятором эндокринной системы. Секретируемые им гормоны (ЛГ, ФСГ, ТТГ, АКТГ) регулируют функцию периферических эндокринных желез. Другие гормоны (ГР, пролактин) оказывают прямое воздействие на органы и ткани-мишени. Аденогипофиз находится в структурной и функциональной связи с гипоталамусом, которая реализуется через портальную систему – первичную капиллярную сеть, контактирующую с терминалями аксонов ядер гипоталамуса.
Гормоны гипоталамуса подразделяют на усиливающие (релизинг-гормоны, либерины) и тормозящие (статины) выделение соответствующих тропных гормонов. Каждый из либеринов/статинов может оказывать стимулирующее/тормозящее действие на несколько гормонов гипофиза.
Сам процесс регуляции продукции осуществляется по принципу обратной связи: регулируемый параметр оказывает влияние на продукцию гормона. Системы обратной связи и ЦНС регулируют секрецию гормонов гипоталамуса и аденогипофиза. Обратная связь может быть отрицательной и положительной. Наиболее изученным является механизм отрицательной обратной связи.
Механизм отрицательной обратной связи реализуется четырьмя способами:
-
Длинная петля обратной связи: концентрация гормона периферической железы снижает продукцию тропного гормона.
-
Короткая петля обратной связи: концентрация тропного гормона снижает продукцию релизинг-фактора.
-
Ультракороткая петля обратной связи: концентрация тропного гормона и/или релизинг-фактора снижают собственную продукцию.
-
Конечная сигнальная молекула (гормон, метаболит, либо любая иная молекула) снижает продукцию тропного гормона/релизинг-фактора.
По аналогии с механизмом отрицательной обратной связи существует механизм положительной обратной связи, когда продукция одних сигнальных молекул увеличивается в ответ на возрастание концентрации других.
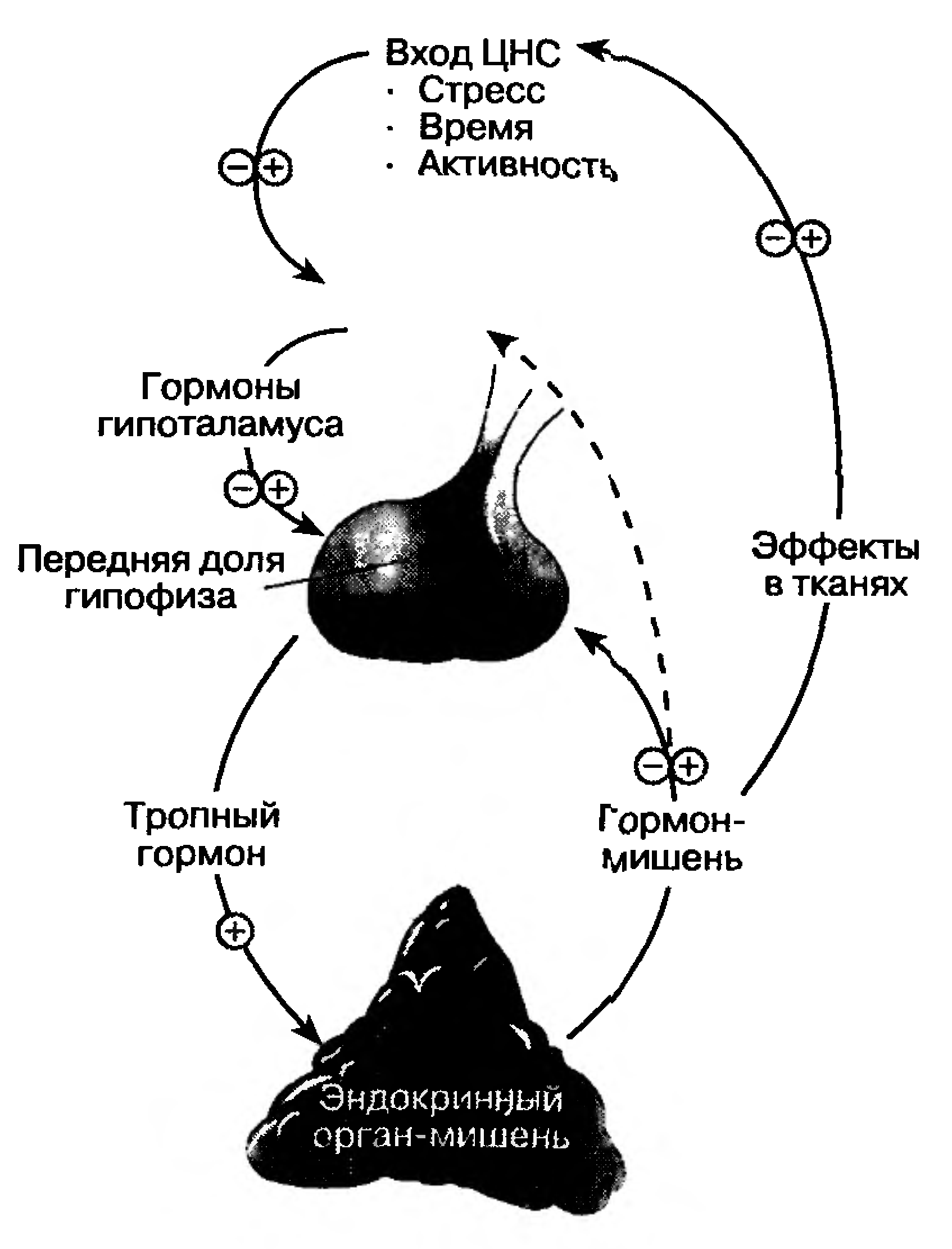 Рисунок
1. Пример регуляции по механизму обратной
связи. Система «гипоталамус-гипофиз-щитовидная
железа» (Кэттайл, 2001).
Рисунок
1. Пример регуляции по механизму обратной
связи. Система «гипоталамус-гипофиз-щитовидная
железа» (Кэттайл, 2001).
Большинство гормонов синтезируются в форме прогормонов. Прогормоны проходят биохимическую модификацию и превращаются в конечную сигнальную гормональную молекулу. Конечные сигнальные молекулы реализуют свой сигнал в несколько этапов. Сначала происходит транспортировка гормона к клетке-мишени, которая имеет мембранные или внутриклеточные рецепторы, комплементарные молекуле гормона. Специфичность этих рецепторов достаточно высока, но не абсолютна поэтому молекулы имеющие сходство в строении могут вызывать сходные эффекты. Сигнал с рецепторов передается молекулам-мессенджерам, которые инициируют сложные каскады биохимических реакций и перестройку метаболизма клеток-мишеней.
Связывание с мембранными рецепторами запускает «раннюю волну» эффектов гормона (2-4 часа), эндоцитоз комплекса рецептор/гормон и дальнейшее связывание гормона с ядерными рецепторами обусловливает «позднюю волну» эффектов. Эти два механизма являются синергичными и протекают одновременно. Ранние эффекты преимущественно реализуются засчет активации имеющихся резервов клетки и перестройки метаболизма, поздние — засчет синтеза de novo внутриклеточных и внутриядерных высокоактивных белковых регуляторов, изменения экспрессии генов. Поздние эффекты проявляются в виде морфогенетического действия гормонов и изменения пролиферативной активности.
Общие механизмы возможных нарушений функции эндокринной системы
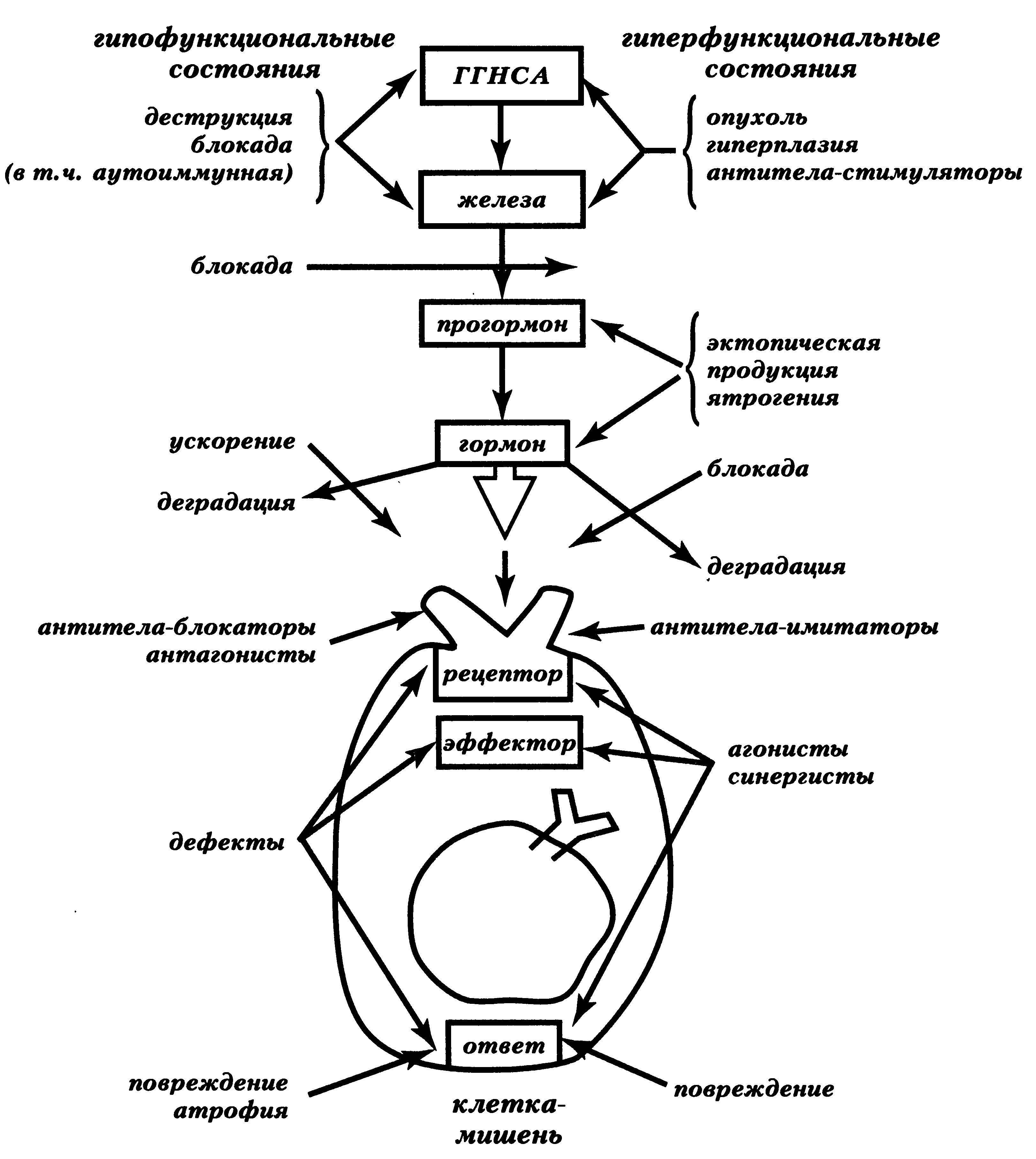 Рисунок
2. Наиболее общие механизмы возможных
нарушений эндокринной системы. (Зайчик,
2007) ГГНСА – гипоталамо-гипофизарный
нейросекреторный аппарат.
Рисунок
2. Наиболее общие механизмы возможных
нарушений эндокринной системы. (Зайчик,
2007) ГГНСА – гипоталамо-гипофизарный
нейросекреторный аппарат.
В норме эндокринная система представляет собой сложную систему, которая динамически регулируется соотношением положительных и отрицательных воздействий. Информация поступающая и исходящая из системы может представлять собой химическое вещество или электрический импульс. Эндокринопатии всегда сопровождаются избыточным или недостаточным эффектом какого-либо гормона на те или иные мишени, либо нарушением генерации/передачи электрических импульсов, что и порождает клиническую картину. Следует отметить, что синтез химических сигнальных молекул так же имеет циклический, «импульсный» характер. Гормональный «импульс» – это реакция «все или ничего» на пороговый стимул, для формирования которого требуется строго определенное время. Нарушение частоты возникновения, «амплитуды» (количество сигнальных молекул) и продолжительности «химических импульсов» приводит к нарушениям нормальной работы системы. Известны исключения, когда гомеостаз может поддерживаться засчет компенсаторных механизмов, пребывая в состоянии неустойчивого равновесия.
Классификация эндокринопатий
|
По происхождению:
|
По уровню продукции гормона:
|
По объему поражения:
|
Эндокринопатии – это патологические состояния, сопровождающиеся первичными или вторичными нарушениями инкреторной функции компонентов ГГНСА.
Гормональная недостаточность – эндокринопатия, имеющая причиной функциональную несостоятельность одного из компонентов ГГНСА .
Типовые причины гормональной недостаточности:
-
Нарушение поставки гормона в кровь (негормонообразующие опухоли, альтерация железы, неинфекционное воспаление, острое нарушение кровообращения)
-
Генетический дефект синтеза гормона
-
Дефицит пластических компонентов
-
Блокада рецепторов к гормону/релизинг-фактору
-
Недостаточный переход прогормона в гормон
-
Наличие циркулирующих антагонистов гормона
-
Усиление связывания с белком-переносчиком
-
Ускоренная деградация гормона
-
Периферическая резистентность (дефект внутриклеточных/мембранных рецепторов, аутоиммунная блокада рецепторов, подавление экспрессии генов рецепторов, снижение количества мессенджеров)
-
Повреждение, гибель или отсутствие клеток-мишеней
Гормональная гиперфункция – эндокринопатия, имеющая причиной избыточность функции одного из компонентов ГГНСА.
Типовые причины гормональной гиперфункции:
-
Функциональная несостоятельность отрицательных обратных связей
-
Избыток стимуляторов секреции, не имеющих отрицательных обратных связей
-
Утечка гормона в результате повреждения железы
-
Нерегулируемая гиперпродукция
-
Метаболический блок с избытком функционально активного прогормона
-
Синдром избыточной эффективности:
- Эктопическая автономная продукция в новообразованиях
- Эктопическая автономная продукция в неопухолевых тканях
- Ятрогенный избыток гормонов
- Наличие АТ к гормональным рецепторам, имитирующих действие гормонов
- Тканевая гиперчувствительность
- Избыток внежелезистого гормона, связанный с особенностями транспорта и катаболизма
Так как эндокринная система представляет собой достаточно устойчивую логическую систему, то суть типовых нарушений регуляции может быть представлена в виде однозначной логической схемы (Таблица 1).
|
Регулирующий гормон
|
Высокая |
Недостаточность железы-мишени |
Автономная выработка регулирующего гормона |
|
|
Нормальная |
Нарушение высвобождения регулирующего гормона |
Норма |
||
|
Низкая |
Автономное функционирование системы или железы-мишени |
|||
|
Концентрация |
Низкая |
Нормальная |
Высокая |
|
|
Регулируемый параметр или гормон |
||||
Таблица 1. Взаимоотношения между регулирующим гормоном и регулируемым параметром (Кэттайл, 2001)
Психогенные эндокринопатии
Нарушения центральных механизмов регуляции эндокринных функций на уровне нейронов коры головного мозга могут быть обусловлены как органическими причинами (опухоли, ОНМК, инфекции), так и функциональными нарушениями деятельности клеток головного мозга. Эмоциональное состояние и функционирование эндокринной системы являются взаимосвязанными и взаимообусловленными, что затрудняет установление причинно-следственных связей. В основе развития психогенных эндокринопатий лежит прекращение или искажение активирующих импульсов от ЦНС. Алкоголизм, голодание, психические травмы, длительные стрессорные воздействия, психозы, неврозы могут приводить к нарушениям со стороны клеток секретирующих гипоталамические гормоны и дисфункции аденогипофиза. Ряд эндокринопатий ассоциирован с продолжительным стрессорным воздействием на психику: сахарный диабет, Базедова болезнь, дисфункция половых желез, несахарный диабет. Кроме того, могут развиваться полигландулярные поражения, обусловленные психогенным повреждением гипоталамуса: гипоталамическая дисфункция и диэнцефальный синдром. Эндокринопатии часто сопровождаются изменениями психоэмоционального состояния пациентов (например, повышенная возбудимость при гиперфункции щитовидной железы, эмоциональная скудность и вялость при гипотирозах). Выявлены ассоциации изменений концентрации гормонов и психических заболеваний (например, снижение пролактина ассоциированно с аутизмом).
Гипоталамические гормоны
Гипоталамус является высшим центром, регулирующим функции вегетативной НС, он поддерживает оптимальный уровень всех видов обмена веществ, энергии, регулирует температуру тела, деятельность внутренних органов, эндокринной системы. Регуляция функции передней доли гипофиза осуществляется посредством выделения гипоталамических нейрогормонов, поступающих в гипофиз через портальную систему сосудов. В гипоталамусе синтезируются 7 стимулирующих (либерины) и 3 ингибирующих (статины) нейрогормона, регулирующих секрецию тропных гормонов гипофиза.
|
К либеринам относятся:
|
К статинам относятся:
|
К гипоталамическим гормонам также относятся вазопрессин (антидиуретический гормон, АДГ) и окситоцин, которые продуцируются клетками крупноклеточных ядер гипоталамуса и поступают в заднюю долю гипофиза.
Гипофизарные гормоны и их эффекты
Гипофиз располагается в гипофизарной ямке турецкого седла клиновидной кости и через ножку анатомически и функционально связан с мозгом. Гипофиз подразделяется на доли: переднюю (аденогипофиз), промежуточную и заднюю (нейрогипофиз).
Гормоны аденогипофиза:
-
АКТГ (кортикотропин) стимулирует пучковую (синтез глюкокортикоидов) и сетчатую (продукция половых гормонов) зоны коры надпочечников;
-
ТТГ (тиреотропин) стимулирует синтез гормонов щитовидной железой;
-
СТГ (соматотропин) стимулирует синтез соматомединов в печени и через них – рост эпифизарного хряща, рост тела в длину, рост соединительной ткани, мышц, внутренних органов, стимулирует синтез белка, оказывает двухфазное влияние на обмен жиров: после кратковременной стимуляции липогенеза происходит увеличение липолиза, повышается уровень СЖК, оказывает кратковременное инсулиноподобное действие, стимулирует секрецию глюкагона;
-
ФСГ (фоллитропин) стимулирует сперматогенный эпителий и образование сперматозоидов и мужчин, у женщин участвует в развитии фолликула и стимулирует образование эстрогенов;
-
ЛГ (лютропин) стимулирует интерстициальные клетки Лейдига и синтез тестостерона у мужчин, у женщин участвует в развитии фолликула, стимулирует функцию желтого тела и образование прогестерона;
-
Пролактин у женщин стимулирует рост молочных желез и образование молока в них, поддерживает существование желтого тела и синтез им прогестерона, стимулирует секрецию надпочечниковых андрогенов, обусловливает сложные инстинктивные реакции («материнский инстинкт»), способствует росту сальных желез и внутренних органов; у мужчин – потенциирует действие ЛГ и ФСГ на поддержание сперматогенеза, усиливает метаболизм в яичках (↑массы), усиливает метаболизм в сперматозоидах (↑подвижность, ↑сперматогенез), стимулирует синтез тестостерона клетками Лейдига; метаболические эффекты – стимулирует анаболизм, жиромобилизующий эффект, ↑ синтеза хондроитинсульфата, ↑ синтеза соматомедина в печени, стимулирует β1-адренорецепторы миокарда, оказывает иммуномодулирующее действие, участвует в осмотической регуляции состава и количества амниотической жидкости, иммуномодулятор в системе мать-плод;
-
β- и γ-липотропные гормоны (литропины) оказывают липолитическое действие, β-литропин оказывает меланоцитстимулируюющее, кортикотропинстимулирующее, гипокальциемическое и инсулиноподобное действие.
Гормоны промежуточной доли и нейрогипофиза:
-
Меланоцитстимулирующий (меланоформный), синтезируется в промежуточной доле гипофиза стимулирует синтез меланина ;
-
АДГ (вазопрессин), содержится в нейрогипофизе, регулирует осмолярность жидкостей организма, оказывает сосудосуживающее действие, ↑ гликогенолиз, ↑ глюконеогенез, усиливает и мобилизует долговременную память;
-
Окситоцин, содержится в нейрогипофизе, стимулирует гладкую мускулатуру матки и миометрий, вызывает сокращение миоэпителиальных клеток протоков молочной железы, обладает слабым вазопрессиноподобным действием, регулирует психоэмоциональное состояние и сложные инстинкты (внутригрупповое социальное поведение).
Типовые формы патологии аденогипофиза
Нормальная функция гипофиза зависит от поступления гипоталамических релизинг-факторов и релизинг-ингибирующих факторов. Для секреции всех гормонов передней доли гипофиза (за исключением пролактина), необходима стимуляция гипоталамическими релизинг-факторами. Синтез пролактина дополнительно находится под ингибирующим контролем гипоталамического допамина. Синдромы избытка гипофизарных гормонов развиваются из-за нарушения связи гипофиз-гипоталамус или из-за автономно секретирующих групп клеток (как правило, опухоли). Синдромы гормональной недостаточности возникают в результате гипофункции гипоталамических релизинг-факторов или локальных повреждений в области sella turcica и ножки гипофиза.
 Рисунок
3. Классификация типовых форм патологии
аденогипофиза (Литвицкий, 2003).
Рисунок
3. Классификация типовых форм патологии
аденогипофиза (Литвицкий, 2003).
Гиперфункция передней доли гипофиза
Гиперпитуитаризм – это избыток содержания и/или эффектов одного либо нескольких гормонов аденогипофиза. В большинстве случаев гиперпитуитаризм – это первичное парциальное поражение гипофиза, реже – патология, связанная с нарушением гипоталамо-гипофизарных функциональных взаимосвязей.
 Гипофизарный
гигантизм и акромегалия
Гипофизарный
гигантизм и акромегалия
Гигантизм – эндокринопатия, характеризующаяся гиперфункцией СТГ-РГ и/или СТГ, пропорциональным ростом конечностей и туловища. Объективных признаков патологии, кроме пропорционального увеличенных органов, не выявляется. Редко: нарушение зрения, снижение способности к обучению. Проявления преимущественно субъективны: утомляемость, головная боль, мышечные боли. При продолжающейся гиперпродукции СТГ-РГ и/или СТГ после созревания скелета формируется акромегалия.
Акромегалия – эндокринопатия, характеризующаяся гиперфункцией СТГ-РГ и/или СТГ, диспропрорциональным ростом скелета, мягких тканей и внутренних органов.
Этиология: опухоли аденогипофиза (эозинофильная аденома, соматотропинома, смешанные опухоли), опухоли гипоталамуса (гамартрома, ганглионевринома), эктопические опухоли продуцирующие СТГ или СТГ-РГ, нейроинфекции, интоксикации, черепно-мозговые травмы.
Стадии:
-
Преакромегалия — стадия ранних трудно диагностируемых проявлений.
-
Гипертрофическая стадия – типичная для акромегалии гипертрофия и гиперплазия.
-
Опухолевая стадия – преобладание опухолевой симптоматики
-
Кахектическая стадия – исход забоваления
Патогенеческие механизмы: первичная или вторичная парциальная гиперфункция ГГНСА (↑СТГ-РГ, ↑СТГ); первичная или вторичная парциальная гипофункция гипоталамуса (↓соматостатин); эктопический синтез СТГ-РГ и/или СТГ; избыточная стимуляция рецепторов органов-мишеней; анатомо-физиологическая диссоциация гипофиза и гипоталамуса. Хронический избыточный синтез СТГ-РГ и/или СТГ приводит к чрезмерной активации анаболических процессов в органах и тканях, способных к интенсивному росту на данном этапе онтогенеза. Это значительно увеличивает пластические и энергетические потребности организма в молодом возрасте. Ткани-мишени в разные периоды онтогенеза имеют различную чувствительность к СТГ, что вызывает акромегалию у взрослых. Из-за избыточного разрастания соединительной ткани наступают дегенеративные изменения миофибрилл, что приводит к быстрой утомляемости. Так как ведущей причиной являются опухоли ЦНС, на фоне их экспансивного роста может происходить формирование сопутствующей неврологической симптоматики и нарушений зрения. Увеличение продукции СТГ приводит к потенциированию синтеза гормонов ЩЖ, что может сопровождаться тиреоидной патологией. Соматотропин обладает выраженным контринсулярным эффектом, что может приводить к развитию нарушений углеводного обмена. Абсолютная и относительная недостаточность синтеза и/или эффектов половых гормонов на фоне избытка СТГ приводит к гипогинетализму и нарушениям полового развития. Систематическое стрессорное воздействие (боли, половая дисфункция, ощущение снижения работоспособности), гипертиреоз, поражение нейронов коры и подкорки в сочетании с нарушениями минерального, углеводного и липидного обменов могут приводить к раннему формированию АГ, сопровождающейся нарушением функции сердца. Отставание увеличения спланхов от роста тела вцелом может сопровождаться недостаточностью функции органов (печень, сердце).
Клиника: увеличены надбровные дуги, скулы, ушные раковины, нос, губы, язык, кисти рук и стопы, нижняя челюсть выступает вперед, увеличиваются промежутки между зубами, кожа утолщена, с грубыми складками, грудная клетка увеличена в объеме с широкими межреберьями. Гипертрофия ЛЖ, артериальная гипертензия. Гипертрофия внутренних органов без нарушения функции. Полинейропатии, миопатии, возможны эпилептоидные приступы. В 50% случаев диффузный или узловой зоб. Возможно развитие СД. При выраженном росте опухоли может происходить сдавление хиазмы, что сопровождается снижением остроты и ограничением полей зрения. Часто встречаются эректильная дисфункция, нарушения менструального цикла.
Диагностика:
-
ОАК: возможны анемия, лейкопения, эозинофилия
-
ОАМ: возможна глюкозурия при развитии СД
-
Биохимический анализ крови: возможно повышение общего белка, неэстерифицированных ЖК, гипергликемия при СД, гиперфосфатемия, гипокальциемия
-
Глюкозотолерантный тест: возможно наличие нарушения толерантности к глюкозе
-
Гликозилированный гемоглобин: может быть повышен при развитии СД
-
Концентрация гормонов: СТГ > 10 нг/мл, среднесуточный уровень СТГ > 4.9 нг/мл, резкое повышение СТГ во всех пробах при суточном мониторинге
-
Мониторинг АД: возможно наличие АГ
-
ЭКГ: возможно наличие гипертрофии ЛЖ
-
УЗИ: увеличение размеров внутренних органов, структурные изменения в щитовидной железе, гипертрофия ЛЖ
-
Рентгенография черепа и области турецкого седла: гиперостоз внутренней пластинки, остеопороз костей черепа, изменения контуров в области sella turcica.
-
КТ, МРТ: выявление неоплазий в головном мозге и внутренних органах
-
ИФА, PCR: определение опухолевых антигенов и антител к ним, неспецифических опухолевых маркеров
-
Офтальмологическое исследование: снижение остроты зрения без выраженных органических изменений, ограничение полей зрения, возможны застойные явления в области сосочков зрительных нервов
-
Неврологический статус: снижение чувствительности, сухожильно-периостальных рефлексов
-
ЭЭГ: выявление изменений характерных для эпилептоидных состояний
Функциональные тесты:
Тесты на подавление секреции СТГ:
-
Пероральный ГТТ: в норме гипергликемия значительно снижает секрецию СТГ. При гиперсекреции СТГ, его концентрация в крови превышает 2 нг/мл через 2.5-3 ч после перорального приема 75 г глюкозы
-
Тест с парлоделом: в норме парлодел повышает содержание СТГ. При гиперсекреции СТГ, через 4 часа после перорального приема концентрация СТГ снижается более чем на 50%.
Тесты со стимуляцией секреции СТГ:
-
Проба с инсулином: в норме гипогликемия повышает концентрацию СТГ. При гиперсекреции СТГ, его концентрация не изменяется (незначительно изменяется), либо снижается через 30-60 мин после внутривенного введения инсулина в дозе 0.15-0.20 ЕД/кг при уровне глюкозы < 2 ммоль/л.
-
Проба с тиреолиберином: опухолевые клетки способны реагировать на неспецифические стимуляторы (в данном случае тиреолиберин). При наличии секретирующей СТГ опухоли, концентрация его увеличивается на 50-100% через 1-2 ч после внутривенного введения 500 мкг тиреолиберина.
-
Проба с СТГ-РГ: по своему смыслу аналогична пробе с тиреолиберином. Внутривенно вводят 100 мкг соматолиберина. Оценку производят так же как и при пробе с тиреолиберином.
Гипофизарный гиперкортицизм (болезнь Иценко-Кушинга)
Болезнь Иценко-Кушинга – гипоталамо-гипофизарное заболевание, характеризующееся избыточной секрецией кортикотропина и последующей двусторонней гиперплазией надпочечников и их гиперфункцией (гиперкортицизм).
Этиология: окончательно неустановлена. В большинстве случаев при гипофизарном гиперкортицизме выявляется базофильная аденома гипофиза (микро-, макроаденома), иногда – гиперплазия базофильных клеток аденогипофиза. ЧМТ, энцефалиты, арахноидиты, роды и беременность могут выступать в роли предрасполагающих факторов.
Гиперкортицизм – является клиническим синдромом, который проявляется гиперфункцией надпочечников. Следует различать понятия «болезнь Иценко-Кушинга» и «синдром Иценко-Кушинга», они используются для обозначения разных патологий (см. таблицу 2).
|
Эндогенный гиперкортицизм |
Экзогенный гиперкортицизм |
Функциональный гиперкортицизм |
|
Болезнь Иценко-Кушинга (опухоль гипофиза)
Синдром Иценко-Кушинга (опухоль коры надпочечников)
АКТГ-эктопированный синдром (эктопическая опухоль вне гипофиза и надпочечников) |
Ятрогенный: длительное введение синтетических кортикостероидов |
Юношеский гипоталамический синдром
Гипоталамический синдром
Беременность
Ожирение
Сахарный диабет
Алкоголизм
Заболевания печени |
Таблица 2. Классификация гиперкортицизма (Марова, 1992)
Степени тяжести гипофизарного гиперкортицизма:
-
Легкая: наблюдается сочетание 3-4 и более характерных для гиперкортицизма синдромов
-
Средняя: развиваются почти все проявления, но без осложнений со стороны ССС, костной, иммунной систем
-
Тяжелая: выражены все проявления, развитие осложнений, декомпенсация
Патогенез: первичная парциальная гиперфункция базофильных клеток аденогипофиза, нерегулируемая гиперпродукция АКТГ, функциональная несостоятельность обратных связей гипофиз/гипоталамус (снижение ингибирующего эффекта гипоталамического допамина) сопровождаются напочечниковыми и вненадпочечниковыми эффектами. В надпочечниках повышается концентрация глюкокортикоидов и гликогена, в меньшей степени – минералкортикоидов. Вненадпочечниковые эффекты проявляются гиперпигментацией и нарушениями психики. Увеличивается катаболизм белков и углеводов, что приводит к атрофическим изменениям мышц (в том числе сердечной мышцы), инсулинрезистентности, усилению глюконеогенеза в печени с последующим развитием стероидного диабета. Усиленный катаболизм белков способствует подавлению специфического иммунитета, в результате чего развивается вторичных иммунодефицит. Ускорение анаболизма жиров приводит к ожирению. Увеличение продукции минералкортикоидов приводит с одной стороны на нарушениям реабсорбции кальция в кишечнике, с другой – к ускоренной деградации костных структур, что приводит к остеопорозу. Под действием минералкортикоидов происходит активация РААС, что приводит к развитию гипокалиемии и АГ. Гиперсекреция андрогенов приводит к снижению синтеза гонадотропинов гипофиза и увеличению синтеза пролактина. В результате комплексных изменений обмена веществ снижается синтез ТТГ и СТГ. Повышена секреция СТГ-РГ, эндорфинов, меланоцитстимулирующего гормона.
Клиника: диспластическое ожирение, трофические нарушения кожи, гиперпигментация, стрии, гнойные поражения, миопатия, системный остеопороз, симптомы нарушения белкового обмена, АГ, вторичная кардиомиопатия, энцефалопатия, симптоматический СД, вторичный иммунодефицит, нарушения половой функции, эмоциональная лабильность.
Диагностика:
-
ОАК: ↑Hb, эритроцитоз, нейтрофильный лейкоцитоз с дегенративно-регенеративным сдвигом влево, лимфопения, эозинопения, ↑СОЭ
-
ОАМ: щелочная реакция, глюкозурия, протеинурия, лейкоцитурия, фосфаты
-
Биохимический анализ крови: гипокалиемия, гипернатриемия, гиперфосфатемия, гиперхолестеринемия, гиперкальциемия, снижение общего белка, ↑АлАТ, ↑АсАТ, ↑ЩФ, ↑триглицеридов, ↑β-липопротеидов, ↑ПТИ
-
ГТТ: нарушение толерантности к глюкозе
-
Гликозилированный гемоглобин: повышен
-
Протеинограмма: ↓IgM, ↓IgG
-
Концентрация гормонов: ↑АКТГ, ↑андрогенов, ↑пролактина, ↑СТГ-РГ, ↑эндорфинов, ↑меланоцит-стимулирующего гормона, ↑паратгормон, ↓кальцитонин, ↓СТГ, ↓ТТГ, ↓гонадотропинов, извращение суточного ритма синтеза ГК.
-
Иммунологические исследования: ↓фагоцитарной активности нейтрофилов, ↓абсолютного числа T-лимфоцитов, ↓сывороточного и лейкоцитарного интерферонов
-
ИФА, PCR: определение опухолевых антигенов и антител к ним, неспецифических опухолевых маркеров
-
Мониторинг АД: АГ
-
ЭКГ: гипокалиемия, гипертрофия ЛЖ
-
УЗИ: увеличение надпочечников, хр. пиелонефрит, жировой гепатоз, панкреолипоматоз, конкременты в почках
-
Рентгенография: остеопороз скелета, асептический некроз головок бедренных костей, компрессионные переломы тел позвонков
-
КТ, МРТ: гиперплазия надпочечников, остеопороз костей черепа, изменения в области турецкого седла (аденома), признаки повышения ВЧД, признаки энцефалопатии
-
Радиоиммунное сканирование: двустороннее повышение поглощения надпочечниками йод-холестерола
-
Денситометрия: ранние признаки остеопороза
-
Офтальмологическое исследование: сужение полей зрения, ангиопатия, застойные изменения глазного дна
Функциональные тесты:
-
«Большая» проба с дексаметазоном: при болезни Иценко-Кушинга (опухоль гипофиза) принцип обратной связи сохранен, при синдроме Иценко-Кушинга (опухоль надпочечников) – нарушен. При гипофизарном гиперкортицизме после приема дексаметазона в суточной дозе 8 мг, экскреция кортизола и 17-ОКС в моче снижается более чем на 50%, при кортикостероме – не снижается.
-
Проба с синактеном-депо: в норме и при гипофизарном гиперкортицизме принцип обратной связи сохранен, поэтому через 30-60 после введения 250 мг синактена-депо (аналог АКТГ) концентрация кортизола и 17-ОКС в крови увеличивает в 2 и более раза, при коритикостероме – не увеличивается.
Гиперпролактинемия
Гиперпролактинемия – это клинический симптомокомплекс, который развивается при повышении концентрации пролактина в крови > 20 нг/мл.
Может быть физиологической и патологической. Физиологическая гиперпролактинемия может встречаться у женщин во время беременности и после родов до окончания кормления грудью. Патологическая гиперпролактинемия встречается у мужчин и женщин. Следует отметить, что пролактин синтезируется не только в аденогипофизе. Внегипофизарными источниками пролактина являются эндометрий и клетки иммунной системы (практически все, но преимущественно Т-лимфоциты).
Этиология: синдром гиперпролактинемии может возникать и развиваться как первичное самостоятельное заболевание и вторично на фоне имеющейся патологии. Классификацию этиологических факторов см. в таблице 3.
|
Первичная гиперпролактинемия |
Вторичная гиперпролактинемия |
|
Синдром ГП как самостоятельное заболевание: – идиопатические гипоталамические нарушения – аденомы гипофиза – синдром ГП на фоне хронической внутричерепной гипертензии и синдрома «пустого турецкого седла»
Синдром ГП в сочетании с другими заболеваниями гипоталамо-гипофизарной зоны: – акромегалия – болезнь Иценко-Кушинга – гормонально неактивные образования, повреждение ножки гипофиза |
При поражении периферических эндокринных желез: – первичный гипотиреоз – эстрогенпродуцирующие опухоли – склерокистоз яичников – врожденная дисфункция коры надпочечников
Ятрогенные формы, обусловленные приемом медицинских препаратов
Нейрогенные нарушения Печеночная и почечная недостаточность
Внегипофизарные опухоли, продуцирующие пролактин
Хронический простатит Эндометриоз, мастопатии |
Таблица 3. Классификация синдрома гиперпролактинемии (Окороков, 2010, сокращенная)
Патогенез: первичная, вторичная или третичная парциальная гиперфункция лактофоров аденогипофиза, нерегулируемая гиперпродукция пролактина, функциональная несостоятельность обратных связей гипофиз/гипоталамус (снижение ингибирующего эффекта гипоталамического допамина); эктопическая секреция пролактина внегипофизарными опухолями и пролактинсекретирующими спланхами; стимуляция синтеза пролактина гормонами, препаратами, экспансивно растущей опухолью. Хроническая гиперпролактинемия нарушает циклическое выделение гонадотропинов, уменьшает частоту и амплитуду пиков секреции ЛГ, ингибирует действие гонадотропинов на половые железы, что приводит к гипогонадизму, формированию синдрома галакторрея+аменоррея, импотенции, фригидности, аноргазмии, снижению либидо, бесплодию, гинекомастии, гипоплазии матки. Непосрдественное воздействие пролактина на липидный обмен приводит к изменениям липидного спектра, развивается ожирение. Нарушение процессов синтеза, связанных с концентрацией гонадотропинов по механизму обратной связи вызывает гормональный дисбаланс других тропных гормонов. Если гиперпролактинемия развивается на фоне экспансивно растущей опухоли ГГНСА, то с увеличением ее размеров проявляется неврологическая симптоматика, появляются офтальмологические нарушения, повышается ВЧД. К высокомолекулярным формам пролактина при их поступлении в кровь вырабатываются антитела, которые связывают пролактин. В связанном виде пролактин медленнее выводится из организма и выключается из механизма регуляции по принципу обратной связи. В таком случае развивается гиперпролактинемия без клинических проявлений.
Клиника: различается для мужчин и женщин.
У мужчин: снижение полового влечения, отсутствие спонтанных утренних эрекций, головные боли, гипогонадизм, аноргазмия, ожирение по женскому типу, бесплодие, истинная гинекомастия, галакторея.
У женщин: отсутствие менархе, недостаточность функции желтого тела, укорочение лютеиновой фазы, ановуляторные циклы, опсоменорея, олигоменорея, аменорея, менометроррагия, бесплодие, галакторея, мигрени, ограничение полей зрения, фригидность, ожирение, избыточный рост волос, отсутствие симптомов «зрачка» и «натяжения слизи» при гинекологическом осмотре.
Диагностика:
– ОАК,ОАМ: без изменений
– Биохимический анализ: может быть повышен уровень глюкозы, ЖК
– Содержание гормонов: пролактин у женщин > 20 нг/мл, у мужчин >15 нг/мл
– ИФА и PCR: опухолевые антигены, антитела к ним, антитела к компонентам ГГНСА
– Рентгенография черепа: признаки повышения ВЧД, изменение формы и размеров турецкого седла
– КТ и МРТ: изменения размеров и плотности гипофиза, отклонение ножки гипофиза, выбухание дифрагмы турецкого седла, проявления синдрома «пустого седла».
– Офтальмологическое исследование: может выявляться сужение полей зрения, застойные явления в области сосочка зрительного нерва.
Функциональные пробы
-
Проба с тиреолиберином: в норме после в/в введения 200-500 мкг тиреолиберина наблюдается повышение секреции пролактина через 15-30 мин в 4-10 раз. При гиперпролактинемии неопухолевого генеза пик в норме или снижен, опухолевого генез – резко снижен или отсутствует
-
Проба с метоклопрамидом: в норме метоклопрамид стимулирует секрецию пролактина. После в/в введения 2 мл (10 мг) метоклопрамида в течение 4-х часов концентрация пролактина в крови увеличивается в 10-15 раз. При пролактиноме – не увеличивается.
Гипофункция аденогипофиза
Парциальный гипопитуитаризм
Гипофизарный нанизм – недостаточность функции СТГ, заболевание, основным проявлением которого является отставание в росте.
Этиология и патогенез:
1) абсолютный или относительный дефицитом СТГ в связи с патологией самого гипофиза
2) нарушение гипоталамической (церебральной) регуляции.
3) нарушение тканевой чувствительности к СТГ.
Пангипопитуитарная карликовость наследуется преимущественно по рецессивному типу. Предполагают, что имеется 2 типа передачи этой формы патологии- аутосомным путем и через Х- хромосому. При этой форме нанизма наряду с дефектом секреции СТГ чаще всего расстраивается секреция гонадотропинов и тиреотропного гормона. Секреция АКТГ нарушается в меньшей степени. У большинства больных имеется патология на уровне гипоталамуса.
Этиотропная классификация (В.А. Петеркова, 1995 в сокращении):
