
- •Термодинамические свойства воздуха
- •Иваново 2001
- •Введение
- •Принцип построения таблиц термодинамических свойств газов
- •Примеры расчета процессов по таблицам термодинамических свойств газов
- •2.2. Изобарный процесс
- •2.3. Изохорный процесс
- •2.4. Изотермический процесс
- •Библиографический список
- •Содержание Введение ……………………………………………………….……………… 3
- •Термодинамические свойства воздуха
- •Составитель чухин Иван Михайлович
Министерство образования Российской Федерации
Ивановский государственный энергетический университет
Кафедра теоретических основ теплотехники
Термодинамические свойства воздуха
Справочные материалы и методические указания для определения термодинамических свойств воздуха с учетом влияния температуры на их изобарную и изохорную теплоемкость
Иваново 2001
Составитель И.М. ЧУХИН
Редактор А.А. ВАРЕНЦОВ
Данные материалы предназначены для студентов специальностей: 100500, 100600, 100700, 100800, 101000, 210200, 330100, 060800, изучающих курс технической термодинамики, а также для аспирантов и преподавателей теплоэнергетических направлений. Они включают таблицы термодинамических свойств воздуха с учетом влияния температуры на их изобарную и изохорную теплоемкости, а также основные методические положения по их определению в различных процессах.
Методические указания утверждены цикловой методической комиссией ТЭФ
Рецензент
кафедра теоретических основ теплотехники Ивановского государственного энергетического университета
Введение
Термодинамические свойства идеального воздуха при учете влияния температуры на их изобарную и изохорную теплоемкость близки к реальным энергетическим (калорическим) параметрам в большом диапазоне давлений и температур [1]. Так, при давлениях до 30 МПа и температурах от –50 °С до 1500 °С эти энергетические параметры имеют погрешность по сравнению с аналогичными параметрами, полученными на основании экспериментальных данных, не более 0,5 %. В этом диапазоне давлений и температур находятся большинство процессов воздуха, проходящих в промышленных и энергетических установках. Поэтому, используя уравнение состояния идеального газа Pv=RT и рассчитанные энергетические параметры (h, u, s) с учетом влияния температуры на изохорную и изобарную теплоемкость, любой процесс воздуха рассчитывается по уравнениям идеального газа. Это очень удобно и не требует привлечения величин, полученных экспериментальным путем.
Единственная сложность при выполнении таких расчетов связана с определением функциональной зависимости изобарной или изохорной теплоемкости воздуха в зависимости от температуры СР=f1(T), СV=f2(T). Затруднения, вызванные при расчете этих теплоемкостей, обусловлены привлечением целого ряда физических констант, которые определяются экспериментально и сами являются функциями температуры. В результате этого расчетные формулы для СР или СV получают в два этапа: сперва на основании расчетов, выполненных для СР по квантовой теории теплоемкостей, строят графическую зависимость СР=f1(T), а затем путем ее аппроксимации получают выражение степенного полинома и значения его констант. Эти сложности привели к необходимости создания специальных таблиц термодинамических свойств газов [1]. В этих таблицах приведены численные значения теплоемкостей СР и СV, энергетических параметров: h, u, sо как функции от температуры. Подробная методика расчета энергетических параметров газов и примеры расчета некоторых процессов газов по этим таблицам приведены в [2].
Принцип построения таблиц термодинамических свойств газов
В табл. 1 термодинамических свойств воздуха приведены значения истинных изобарных и изохорных теплоемкостей воздуха и коэффициента Пуассона К=СР/СV. Все эти величины есть функции от температуры.
В табл. 2 приведены значения энтальпий h, внутренних энергий u, величин относительных давлений πо=P/Po и относительных объемов Θо=v/vo, величин so. Все эти величины – функции температуры, которая приведена в крайнем левом столбце таблицы.
Из
табл. 1 видно, что коэффициент Пуассона
- величина переменная, он зависит от
температуры. Поэтому расчет адиабатного
процесса с использованием К в уравнениях
типа PvК=const
весьма затруднителен. В связи с этим, в
табл. 2 расчет энергетических параметров
совмещен с расчетом обратимого адиабатного
процесса s=const. Для адиабатного процесса
(и только для него) в табл. 2 приведены
величины πо=P/Po
и Θо=v/vo.
Эти величины позволяют перейти от одной
точки адиабатного процесса к другой
при определении термических параметров
без коэффициента Пуассона. Расчет всех
величин, приведенных в табл.2, выполнен
при То=0
К по следующим уравнениям:![]()
![]()
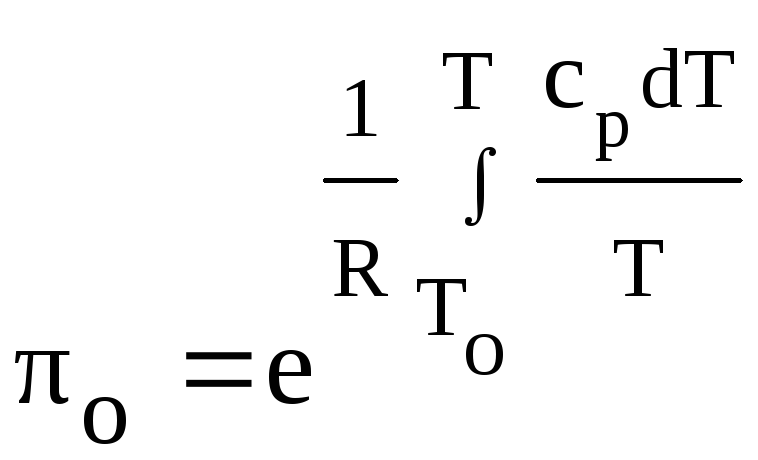 , (1)
, (1)
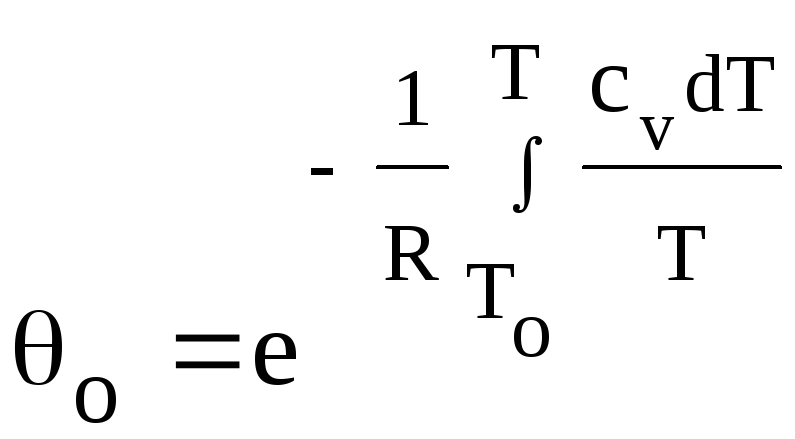 , (2)
, (2)
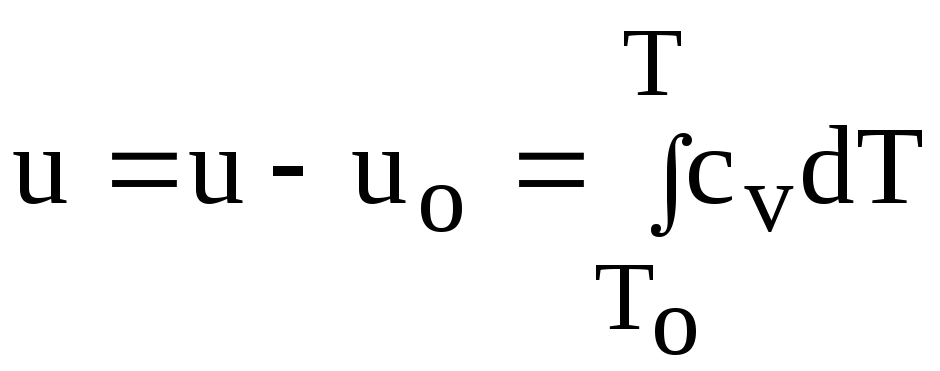 , (3)
, (3)
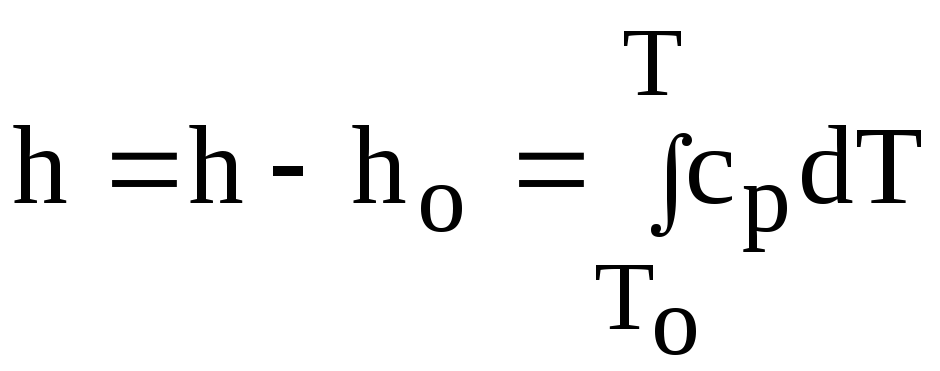 , (4)
, (4)
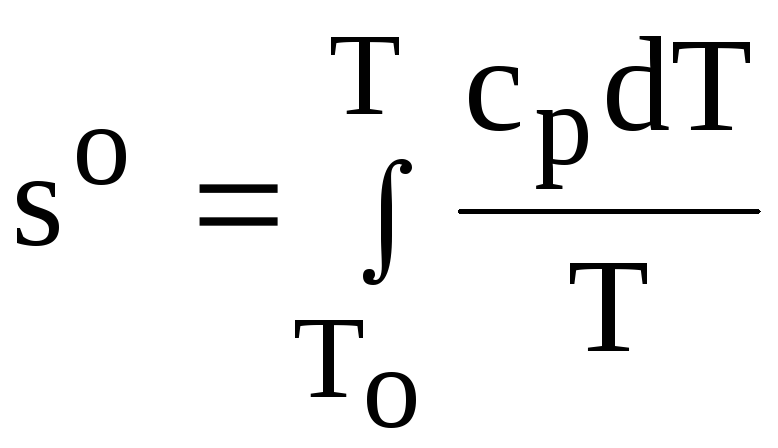 . (5)
. (5)
В уравнениях (3) и (4) начало отсчета внутренней энергии uo=0 и энтальпии ho=0 приняты при То=0 К. В уравнении (5) величина so является составляющей абсолютного значения энтропии, рассчитываемого по формуле
![]() , (6)
, (6)
где значение Ро выбирается произвольно, но при расчете одного и того же процесса должно быть одним и тем же.
