
Лабораторная работа №2.
Влияние температуры и катализатора на скорость химических реакций.
Теория.
1. Влияние температуры на скорость химических реакций.
 (1)
(1)
Уравнение в интегральном виде (1) носит название уравнения Аррениуса. Оно устанавливает зависимость константы скорости химической реакции «k» от температуры. Величину Е называют энергией молекул при данной температуре, которым должны обладать молекулы, чтобы они могли вступить в химическую реакцию. Из уравнения (1) следует, что чем больше энергия активации, тем меньше константа скорости и, следовательно, скорость химической реакции.
Связь энергии активации с теплотой реакции можно проиллюстрировать с помощью представления об энергетическом барьере (см. рисунок):

Химическую
реакцию можно представить как переход
из состояния 1 со средней энергией
исходных веществ
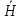 (исх.)
в состояние 2 со средней энергией
продуктов реакции
(исх.)
в состояние 2 со средней энергией
продуктов реакции
 (прод.).
Разность средних энергий – это теплота
реакции:
(прод.).
Разность средних энергий – это теплота
реакции:
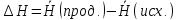
Из рис. также следует, что теплота реакции связана с энергиями активации прямой и обратной реакций:
 (2)
(2)
Для того, чтобы осуществился элементарный акт химической реакции, молекулам исходных веществ, обладающих достаточной энергией, необходимо образовать так называемый активированный комплекс – промежуточные соединения с повышенной энергией (см. рис.4: вершина энергетического барьера).
Достигнув переходного состояния, система может перейти в конечное состояние – продукты реакции или вернуться в исходное состояние. Соотношение вероятностей этих переходов учитывает множитель А в уравнении Аррениуса.
2. Каталитические реакции.
Катализом называют явление ускорения химических реакций в присутствии веществ, не участвующих стехиометрически в суммарном процессе. Эти вещества получили название катализаторов.
Катализ бывает гомогенным, когда катализатор и реагирующие вещества находятся в одной фазе (газе или жидкости) и гетерогенным, когда катализатор находится в иной фазе. Например, некаталитическое взаимодействие оксида серы (IV) с кислородом происходит чрезвычайно медленно (константа скорости k1→0):
 (3)
(3)
Если добавить в газовую смесь оксида азота (2), то вместо медленной реакции (3) пойдут две быстрые:
 ,
k2>>k1
(4)
,
k2>>k1
(4)
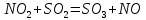 ,
k3>>k1
,
k3>>k1
причем NO будет постоянно регенерироваться в ходе реакции гомогенного катализа.
Скорость реакции можно значительно увеличить, используя гетерогенный катализ и проводя реакцию (3) на платиновом катализаторе.
 ,
k4>>k1
(5)
,
k4>>k1
(5)
Действие катализатора сводится к уменьшению энергии активации реакции, иногда – к увеличению предэкспоненциального множителя «А» в уравнении Аррениуса. В остальных случаях катализатор направляет реакцию по другому, более «быстрому» пути.
Каталитические реакции обладают рядом особенностей:
1. Для катализа необходимо небольшое количество катализатора, так как он или не расходуется, или регенерируется в ходе реакции.
2. Каталитические реакции, как правило, обладают селективностью (избирательностью) – направляют реакцию по определенному пути.
3. Не входя в стехиометрическое уравнение химической реакции, катализатор не смещает химическое равновесие, то есть он в равной степени увеличивает скорости прямой т обратной реакций.
3. Экспериментальное определение энергии активации.
Для экспериментального определения энергии активации химической реакции можно воспользоваться уравнением Аррениуса (1) после его логарифмирования:
 ,
(6)
,
(6)
Проводят реакцию при нескольких температурах (например, Т1, Т2 и Т3) и методом, описанным в лабораторной работе №1 «Кинетика химических реакций», определяют соответствующие константы скоростей реакции при этих температурах (k1, k2 и k3).
Далее строят график в координатах ln k от 1/Т. Согласно уравнению (6), на графиках в этих координатах должна получиться прямая линия, тангенс угла наклона прямой линии будет равен tg=-(E/R) (или tgβ=E/R):

Значение константы А можно получить из уравнения (1), взятого при Т, например, равной Т1:
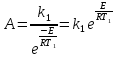 (7)
(7)
Экспериментальная часть.
Цель работы. Изучить влияние температуры на скорость химической реакции, определить энергию активации химической реакции. Изучить влияние катализатора на кинетику химических реакций.
