
лекции / ОФ_Фармакодинамика
.pdf
11
Иногда размер частиц или вид лекарственной формы являются определяющими факторами для реализации фармакологического эффекта лекарства. Например, абсорбция гризеофульвина или солей лития возможна только в том случае, если они имеют вид мельчайших частиц, поэтому все лекарственные формы этих средств представляют собой микрокристаллические суспензии, таблетки или порошки.
Пути введения. Путь введения также определяет скорость поступления лекарства в системный кровоток. В ряду внутривенное > внутримышечное > подкожное введение скорость поступления лекарства в организм уменьшается и время развития эффекта лекарства замедляется. Иногда путь введения может определять характер действия лекарства. Например, раствор сульфата магнезии при пероральном введении оказывает послабляющее действие, при введении в мышцу он оказывает гипотензивный эффект, а при внутривенном введении – наркотическое действие.
Проблема биоэквивалентности лекарственных средств
Выше уже упоминалось о том, что каждое лекарство может быть представлено на рынке как в брендовой, так и в генерической форме, причем генерические средства могут иметь несколько вариантов торговых названий. Например, транквилизатор диазепам представлен на рынке 10 генерическими препаратами, противовоспалительное средство диклофенак – 14. Все это многообразие лекарственных средств отличается часто не только внешним видом, но и стоимостью (причем, разница в цене иногда может быть довольно ощутимой).
Естественно, что врач и пациент предполагают, что все это многообразие лекарств должно обеспечить равное по эффективности лечение болезни. Т.е. они исходят из предположения об эквивалентности различных препаратов одного и того же лекарственного средства, произведенного разными фирмами.
Различают 3 вида эквивалентности:
Химическая (фармацевтическая) эквивалентность – означает, что 2 лекарственных препарата содержат одно и то же лекарственное вещество в равных количествах и в соответствии с действующими стандартами (фармакопейными статьями). При этом неактивные ингридиенты лекарственных препаратов могут различаться. Например, таблетки ренитека и энама по 10 мг являются химически эквивалентными, т.к. содержат по 10 мг эналаприла малеата (ингибитора АПФ).
Биоэквивалентность – означает, что два химически эквивалентных лекарственных препарата различных производителей при введении в организм человека в равных дозах и по одинаковой схеме всасываются и поступают в системный кровоток в равной степени, т.е. обладают сопоставимыми показателями биодоступности. Доказательство биоэквивалентности генерического лекарственного препарата его брендовому аналогу – необходимое условие регистрации любого генерического препарата.
Основным критерием биоэквивалентности является отношение площадей под фармакокинетической кривой для двух изучаемых лекарственных средств, а также отношение максимальных концентраций этих лекарств в крови пациента:
f " = |
Cmax,T |
и f ' = |
AUCT |
|
Cmax,R |
AUCR |
|||
|
|
Считают, что допустимыми колебаниями этих параметров является диапазон 0,8-1,2 (т.е. биодоступность двух сравниваемых лекарств не должна различаться более чем на 20%). Если генерический лекарственный препарат является небиоэквивалентным его брендовому аналогу то данное лекарство не может быть зарегистрировано и разрешено к применению. Показателен пример с препаратами пиридинолкарбамата. Это средство было представлено на рынке в виде таблеток пармидин (Россия), продектин (Венгрия) и ангинин (Япония)2. Разница показателей биодоступности между пармидином и ангинином составляла 7,1%, тогда как та же разница для продектина и ангинина была 46,4%. Неудивитель-
2 Описываемая ситуация имела место еще до того, как было принято законодательство о необходимости представления доказательств биоэквивалентности лекарств разных производителей.
12
но, что доза продектина должна была быть в 2 раза больше дозы ангинина, чтобы оказать сопоставимое терапевтическое действие.
Доказательств биоэквивалентности не требуется для отдельных лекарственных препаратов: дигоксина, фенитоина, оральных контрацептивов. Это связано с тем, что обеспечить равную биодоступность для этих средств сложно даже в пределах одного производителя
– иногда разные серии препарата, изготовленные на одном заводе могут иметь значимые колебания показателей биодоступности.
Следует помнить, что биоэквивалентность лекарств еще ничего не говорит об их терапевтической эквивалентности. Ниже приведен пример подобной ситуации. Терапевтическая эквивалентность. Данное понятие означает, что 2 лекарственных препарата, содержащих одно и то же лекарственное средство, которые применяют в равных дозах и по одинаковой схеме вызывают сопоставимый терапевтический эффект. Терапевтическая эквивалентность не зависит от биоэквивалентности лекарственных препаратов. Два препарата могут быть биологически эквивалентны, но при этом иметь разную терапевтическую эквивалентность. Примером может служить ситуация, которая сложилась после выхода на рынок лекарств 2 препаратов коллоидного висмута субцитрата – брендового препарата «Де-нол» (Yamanouchi Europe B.V., Нидерланды) и «Трибимол» (Torrent House, Индия), которые были биоэквивалентны. Однако, изучение их антигеликобактерной активности показало, что незначительное изменение фирмой Torrent технологии производства практически лишило трибимол активности в отношении H. pylori. Следует отдать должное сотрудникам фирмы – они исправили допущенную ошибку (хотя репутация фирмы при этом несколько пострадала).
Возможна иная ситуация, когда два биологически неэквивалентных препарата оказываются терапевтически эквивалентными. В частности, два оральных контрацептива - новинет (Gedeon Richter) и мерсилон (Organon) содержат по 150 мг дезогестрела и 20 мкг этинилэстрадиола. Несмотря на одинаковый состав, они являются бионеэквивалентными, но при этом равноэффективно предупреждают беременность.
Взаимодействие лекарственных средств
Взаимодействием лекарственных средств называют изменение эффекта одного лекарства под влиянием другого лекарственного средства, которое применяется совместно с ним. В настоящее время можно привести примеры монотерапии – т.е. лечения заболевания путем назначения всего одного средства. Однако, в большинстве случаев амбулаторные пациенты получают 2-3, а стационарные – 4-6 лекарственных средств. Даже если бы врач ограничился прописыванием лекарств исключительно из перечня основных лекарственных средств ВОЗ, то при условии назначения 4 лекарств одновременно число возможных комбинаций составило бы 64.000.000. Запомнить все возможные взаимодействия, которые возникали бы при этом невозможно. Однако, следует знать общие принципы и закономерности взаимодействия лекарств.
При взаимодействии лекарств возможно развитие следующих состояний: Усиление эффектов комбинации лекарств; Ослабление эффектов комбинации лекарств; Лекарственная несовместимость.
Усиление эффектов комбинации лекарств
Данный вид взаимодействия может быть реализован в 3 вариантах:
• Суммирование эффектов или аддитивное взаимодействие (от лат. additio – добавление) – вид лекарственного взаимодействия при котором эффект комбинации равен простой сумме эффектов каждого из лекарственных средств в отдельности. Т.е. 1+1=2. Данный вид взаимодействия характерен для лекарств из одной фармакологической группы, которые имеют общую мишень действия. Например, кислотонейтрализующая активность комбинации гидроокиси алюминия и магния равна сумме их кислотонейтрализующих способностей в отдельности.
13
•Синергизм (от греч. synergos – действующий вместе) – вид взаимодействия при котором эффект комбинации превышает сумму эффектов каждого из веществ взятых по отдельности. Т.е. 1+1=3. В основе синергизма могут лежать фармакокинетические и фармакодинамические механизмы, которые будут рассмотрены ниже.
Синергизм может касаться как желаемых (терапевтических), так и нежелательных эффектов лекарств. Так, например, сочетанное введение тиазидного диуретика дихлотиазида и ингибитора ангиотензинпревращающего фермента эналаприла приводит к усилению гипотензивного действия каждого из средств и данная комбинация с успехом применяется при лечении гипертонической болезни. Напротив, одновременное назначение аминогликозидных антибиотиков (гентамицина) и петлевого диуретика фуросемида вызывает резкое возрастание риска ототоксического действия и развития глухоты.
•Потенцирование – вид лекарственного взаимодействия, при котором одно из лекарственных средств, которое само по себе не оказывает данного эффекта, может приводить к резкому усилению действия другого лекарственного средства. Т.е. 1+0=3. Например, клавулановая кислота не обладает противомикробным действием, но способна усиливать эф-
фект β-лактамного антибиотика амоксициллина за счет того, что она блокирует β- лактамазу (фермент бактерий, который разрушает амоксициллин). Адреналин не оказывает местноанестезирующего действия, но при добавлении к раствору ультракаина он резко удлиняет его анестезирующий эффект (за счет замедления всасывания анестетика из места инъекции).
Ослабление эффектов комбинации лекарств
Ослабление эффектов лекарственных средств при их совместном применении называют антагонизмом. Различают несколько видов антагонизма:
•Химический антагонизм или антидотизм – химическое взаимодействие веществ между собой с образованием неактивных продуктов. Например, химическим антагонистом ионов железа является дефероксамин, который связывает их в неактивные комплексы. Протамина сульфат (молекула, имеющая избыточный положительный заряд) является химическим антагонистом гепарина (молекула которого имеет избыточный отрицательный заряд). Протамин образует с гепарином в крови неактивные комплексы. Химический антагонизм лежит в основе действия антидотов (противоядий).
•Фармакологический (прямой) антагонизм – антагонизм, вызванный разнонаправленным действием 2 лекарственных веществ на одни и те же рецепторы в тканях. Фармакологический антагонизм может быть конкурентным (обратимым) и неконкурентным (необратимым). Рассмотрим их несколько подробнее:
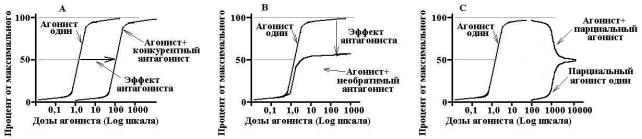
Конкурентный антагонизм. Конкурентный антагонист обратимо связывается с активным центром рецептора, т.е. экранирует его от действия агониста. Из курса биохимии известно, что степень связывания вещества с рецептором пропорциональна концентрации этого вещества. Поэтому, действие конкурентного антагониста можно преодолеть если увеличить концентрацию агониста. Он будет вытеснять антагонист из активного центра рецептора и вызовет ответную реакцию ткани в полном объеме. Т.о. конкурентный антагонист не изменяет максимальный эффект агониста, но для взаимодействия агониста с рецептором требуется его более высокая концентрация. Данная ситуация показана на схеме 9А. Нетрудно заметить, что конкурентный антагонист сдвигает кривую «доза-эффект» для агониста вправо относительно исходных значений и увеличивает ЕС50 для агониста, не влияя на величину Еmax.
Вмедицинской практике достаточно часто используют конкурентный антагонизм. Поскольку эффект конкурентного антагониста может быть преодолен, если его концентрация упадет ниже уровня агониста, при лечении конкурентными антагонистами необходимо постоянно поддерживать его уровень достаточно высоким. Иными словами, клинический эффект конкурентного антагониста будет зависеть от периода его полуэлиминации и концентрации полного агониста.
14
Неконкурентный антагонизм. Неконкурентный антагонист связывается практически необратимо с активным центром рецептора или же взаимодействует вообще с его аллостерическим центром. Поэтому, как бы ни повышалась концентрация агониста – он не в состоянии вытеснить антагонист из связи с рецептором. Поскольку, часть рецепторов, которая связана с неконкурентным антагонистом уже не способна активироваться, значение Еmax понижается. Напротив, сродство рецептора к агонисту не изменяется, поэтому значение ЕС50 остается прежним. На кривой зависимости «дозаэффект» действие неконкурентного антагониста проявляется в виде сжатия кривой относительно вертикальной оси без ее смещения вправо.
Схема 9. Виды антагонизма.
А – конкурентный антагонист смещает кривую «доза-эффект» вправо, т.е. снижает чувствительность ткани к агонисту, не изменяя его эффект.
В – неконкурентный антагонист снижает величину ответа ткани (эффект), но не влияет на ее чувствительность к агонисту.
С – вариант применения парциального агониста на фоне полного агониста. По мере повышения концентрации парциальный агонист вытесняет полный из рецепторов и в итоге ответ ткани снижается от максимального ответа на полный агонист, до максимального ответа на агонист парциальный.
Неконкурентные антагонисты применяются в медицинской практике реже. С одной стороны они имеют несомненное преимущество, т.к. действие их не может быть преодолено после связывания с рецептором, а значит не зависит ни от периода полуэлиминации антагониста, ни от уровня агониста в организме. Эффект неконкурентного антагониста будет определяться лишь скоростью синтеза новых рецепторов. Но с другой стороны, если происходит передозировка данного лекарства, устранить его эффект будет чрезвычайно сложно.
Таблица2. Сравнительнаяхарактеристикаконкурентногоинеконкурентногоантагонистов
|
Конкурентный антагонист |
|
Неконкурентный антагонист |
1. |
Похож по строению на агонист. |
1. |
По строению отличается от агониста. |
2. |
Связывается с активным центром рецеп- |
2. |
Связывается с аллостерическим участ- |
|
тора. |
|
ком рецептора. |
3. |
Смещает кривую «доза-эффект» вправо. |
3. |
Смещает кривую «доза-эффект» по вер- |
|
|
|
тикали. |
4. |
Антагонист снижает чувствительность |
4. Антагонист не изменяет чувствитель- |
|
|
ткани к агонисту (ЕС50), но не влияет на |
|
ность ткани к агонисту (ЕС50), но умень- |
|
максимальный эффект (Еmax), который |
|
шает внутреннюю активность агониста и |
|
может быть достигнут при более высокой |
|
максимальную реакцию ткани на него |
5. |
концентрации. |
5. |
(Еmax). |
Действие антагониста может быть устра- |
Действие антагониста не может быть |
||
|
нено высокой дозой агониста. |
|
устранено высокой дозой агониста. |
6. |
Эффект антагониста зависит от соотно- |
6. |
Эффект антагониста зависит только от |
|
шения доз агониста и антагониста |
|
его дозы. |
Конкурентным антагонистом в отношении АТ1-рецепторов ангиотензина является лозартан, он нарушает взаимодействие ангиотензина II с рецепторами и способствует снижению артериального давления. Действие лозартана можно преодолеть, если ввести высокую дозу ангиотензина II. Неконкурентным антагонистом в отношении этих
15
же АТ1-рецепторов является валсартан. Его действие нельзя преодолеть даже при введении высоких доз ангиотензина II.
Интересным является взаимодействие, которое имеет место между полным и парциальным агонистами рецепторов. Если концентрация полного агониста превышает уровень парциального, то в ткани наблюдается максимальный ответ. Если уровень парциального агониста начинает повышаться, он вытесняет полный агонист из связи с рецептором и ответ ткани начинает уменьшаться от максимального для полного агониста, до максимального для парциального агониста (т.е. такого уровня, при котором он займет все рецепторы). Данная ситуация представлена на схеме 9С.
• Физиологический (непрямой) антагонизм – антагонизм, связанный с влиянием 2 лекарственных веществ на различные рецепторы (мишени) в тканях, что приводит к взаимному ослаблению их эффекта. Например, физиологический антагонизм наблюдается между инсулином и адреналином. Инсулин активирует инсулиновые рецепторы в результате чего увеличивается транспорт глюкозы в клетку и уровень гликемии понижается. Адреналин активирует β2-адренорецепторы печени, скелетных мышц и стимулирует распад гликогена, что в итоге приводит к повышению уровня глюкозы. Данный вид антагонизма часто используется при оказании неотложной помощи пациентам с передозировкой инсулина, которая привела к гипогликемической коме.
Лекарственная несовместимость
Лекарственной несовместимостью называют взаимодействие между лекарственными средствами, которое приводит к нейтрализации их полезного терапевтического действия, усилению токсических эффектов и является недопустимым с клинической точки зрения. Фактически понятие лекарственной несовместимости более широкое и включает как усиление, так и ослабление эффектов лекарств при совместном применении, но при этом лекарственная несовместимость затрагивает только отрицательные стороны такого взаимодействия (тогда как антагонизм, синергизм, потенцирование часто применяются с фармакотерапевтическими целями).
Механизмы взаимодействия лекарств
Различают следующие механизмы взаимодействия лекарств:
•Фармацевтическое взаимодействие – вид взаимодействия, связанный с физикохимической реакцией между лекарственными средствами в процессе изготовления лекарственного препарата, еще до введения этих средств в организм человека. Например, допамин нельзя вводить в инфузионную систему, которая содержит щелочные растворы (гидрокарбонат натрия, раствор Рингера), т.к. при этом он подвергается преципитации.
•Фармакологическое взаимодействие – взаимодействие лекарств, которое проявляется только в организме человека после их совместного применения. По своей природе фармакологическое взаимодействие подразделяют на фармакокинетическое и фармакодинамическое.
Фармакокинетическое взаимодействие связано с изменениями фармакокинетики взаимодействующих веществ. Данный вид взаимодействия может быть связан с изменением фазы абсорбции, распределения, метаболизма или элиминации лекарств.
Взаимодействие в фазе абсорбции может быть обусловлено способностью одного лекарства связывать другое с образованием неактивного комплекса. Например, активированный уголь, холестирамин, сукральфат способны адсорбировать другие лекарства и замедлять их всасывание. Данный вид взаимодействия наблюдается в том случае, если одно из лекарственных средств снижает моторику ЖКТ и замедляет эвакуацию лекарства из желудка. Например, совместное применение атропина с другими лекарствами приводит к снижению скорости их всасывания, т.к. атропин замедляет опорожнение желудка.
Взаимодействие в фазе распределения. Может быть связано с вытеснением одного лекарственного средства из связи с белком под влиянием других лекарств. Данная ситуация уже обсуждалась выше в разделе, посвященном фармакокинетике лекарст-
16
венных средств. Результатом вытеснения из связи с белком одного лекарства другим будет возрастание свободной (активной) фракции первого лекарства в крови. При этом легко может возникнуть ситуация, когда уровень свободной фракции лекарства превысит токсический порог. Например, нестероидные противосовпалительные средства (ацетилсалициловая кислота, индометацин) могут вытеснять противоопухолевое средство метотрексат из связи с белком и одновременно понижать скорость его почечной экскреции. В результате у пациента может развиться интоксикация метотрексатом даже при использовании стандартных терапевтических доз.
Взаимодействие в фазе метаболизма. Проявляется в том случае, если одно из лекарственных средств выступает в роли индуктора или ингибитора ферментов метаболизма другого лекарства. В случае использования индукторов метаболизма эффект этого лекарства будет ослабляться, а в случае ингибиторов – усиливаться. Например, антибиотик рифампицин индуцирует ферменты метаболизма стероидных гормонов, поэтому контрацепция при помощи гормональных лекарственных препаратов в обычных дозах может быть несостоятельной у пациенток, которые его принимают.
Взаимодействие в фазе экскреции. Данный вид взаимодействия связан прежде всего с влиянием лекарственных средств на процесс образования мочи или системы активной секреции лекарств в мочу или желчь. Наиболее показателен пример взаимодействия мочегонного средства фуросемида с другими лекарственными средствами. Фуросемид усиливает процессы образования мочи, поэтому он ускоряет элиминацию других лекарств и значительно сокращает продолжительность их действия. Единственным исключением является литий, выведение которого при назначении фуросемида резко понижается. Поэтому, если обычно на фоне фуросемида дозу других лекарственных средств несколько повышают, доза солей лития должна быть снижена. Фармакодинамическое взаимодействие – это взаимодействие лекарств, связанное с изменением фармакодинамики одного из них, под влиянием другого. Как правило, фармакодинамическое взаимодействие реализуется на уровне рецепторов, ферментов и других биологических субстратов действия лекарств. Например, под влиянием тиреоидных гормонов усиливается синтез β-адренорецепторов в миокарде и усиливается влияние адреналина на миокард.
Данные механизмы взаимодействия лекарств обеспечивают фактически все его виды, рассмотренные выше – как позитивные, так и негативные в клиническом плане.
Нежелательное действие лекарств
Мироздание объективно, оно не подвластно желаниям и чаяниям человека. Стремление человека избавить себя от страданий, продлить свою жизнь заставляет его искать средства для реализации этой мечты. Еще в средние века появилась легенда о философском камне, который мог превращать неблагородные металлы в золото, был панацеей от всех болезней и даровал вечную жизнь. Философский камень, наверное, был единственным лекарственным средством в истории человечества, которое не обладало нежелательными эффектами.
К сожалению, до настоящего времени попытки отыскать лекарственное средство, которое обладало бы сколько-нибудь заметным фармакологическим эффектом и, при этом, было бы лишено нежелательного действия – не увенчались успехом. Мнение Парацельса (14931541 гг) о том, что «… всякое лекарство есть яд, только доза определяет что есть яд и что не является им» до настоящего времени незыблемо и находит все новые и новые подтверждения. Поэтому, естественным является и то, что, разбирая положительные аспекты действия лекарств, мы не должны забывать и об обратной стороне медали.
По определению ВОЗ нежелательными эффектами называют «любые не желаемые или непредвиденные последствия проведения лекарственного лечения». Данное определение весьма обширно и фактически охватывает весь спектр реакций – от незначительных до летальных. Для четкого и ясного описания нежелательных эффектов следует определить их в более узком смысле.
17
Нежелательные эффекты – любые нежелательные изменения, которые как предполагают, обусловлены приемом данного лекарства, возникают при использовании этого лекарства в обычных терапевтических дозах и требуют для своего устранения специального лечения, снижения дозы лекарства или особого внимания при назначении этого лекарства в последующем. Заметим, что такое определение исключает из рассмотрения как незначимые клинически реакции, так и токсическое действие лекарства.
Единой классификации нежелательных эффектов не существует, наиболее рациональной является попытка разделить нежелательные эффекты по патогенетическому принципу:
ТИП А. Предсказуемые или прогнозируемые реакции. Эти реакции представляют собой количественно усиленные эффекты, которые входят в спектр фармакологической активности данного лекарственного средства. Такие реакции встречаются достаточно часто и являются дозозависимыми (т.е. чем выше используемая доза лекарства, тем выше вероятность развития этой реакции). К данному типу относят побочные реакции, вторичные эффекты лекарства.
ТИП В. Непредсказуемые или непрогнозируемые реакции. Это атипичные, т.е. качественно измененные реакции на лекарственное средство, которые не входят в спектр фармакологической активности лекарства. Данная группа нежелательных эффектов не может быть спрогнозирована без специальных тестов. Механизм развития реакций данного типа не всегда ясен. К этой группе относят аллергические реакции, идиосинкразию.
ТИП С. Реакции, связанные с длительным применением лекарственных средств. В эту группу включают кумуляцию, привыкание (толерантность), лекарственную зависимость. ТИП D. Отдаленные реакции, проявляющиеся через несколько лет или поколений. В данную группу включают тератогенное, канцерогенное и мутагенное действие лекарств. ТИП E. Реакции, возникающие в связи с прекращением приема лекарственных средств. Сюда относят синдромы рикошета и отмены.
Рассмотрим все эти эффекты подробнее.
РЕАКЦИИ ТИПА А.
Побочные эффекты – это фармакологические эффекты лекарства, которые не являются терапевтически ценными при лечении конкретного заболевания. Причина их развития – недостаточная селективность действия лекарственных средств. Различают 3 механизма возникновения побочных эффектов:
•Побочные эффекты являются продолжением терапевтически ценного (значимого) фармакологического эффекта лекарства. Например, терапевтическим эффектом инсулина является снижение уровня глюкозы в крови. Но если пациент, страдающий сахарным диабетом, введет инсулин натощак возможно чрезмерное снижение уровняглюкозы и развитие гипогликемической комы.
•Побочные эффекты имеют тот же механизм, что и терапевтически ценные эффекты, но связаны с воздействием на иные органы или ткани. Например, атропин применяют для лечения брадиаритмий. Он блокирует М-холинорецепторы миокарда и усиливает влияние на него симпатической системы, в результате ЧСС и проведение импульсов в миокарде нормализуется. Одновременно атропин блокирует М-холинорецепторы в слюнной железе и снижает выработку слюны. В итоге развивается сухость во рту, появляется охриплость голоса.
•Побочные эффекты имеют иной механизм реализации, чем терапевтически значимые эффекты. Например, антибиотик имипенем блокирует фермент транспептидазу у бактерий и вызывает их гибель (противомикробное действие). В то же самое время в ЦНС
имипенем блокирует ГАМКА-рецепторы и может вызывать судороги.
Вторичные эффекты – это непрямые последствия основного действия лекарственных веществ. Например, антибиотики, подавляя нормальную микрофлору, могут привести к развитию суперинфекции. Глюкокортикостероиды вызывают повышение внутриглазного давления, которое способствует развитию глаукомы.
18
Интолерантность (непереносимость, гиперреактивность) – это состояние при кото-
ром пациент имеет низкий порог чувствительности к лекарству и даже его минимальные дозы позволяют вызвать значительный эффект, а обычные средние дозы вызывают у таких лиц токсическую реакцию. При построении квантовой кривой «доза-эффект» упоминалось, что большинство людей отвечает на средние дозы лекарства, но имеется небольшая группа лиц, которая занимает левую часть кривой – область низких доз. Эта часть популяции пациентов и является группой с интолерантностью к лекарству. Например, в литературе описан случай, который возник у профессора медицинской школы св. Мартина в Лондоне R.L. Smith после приема 40 мг симпатолитика дебризохина. Обычно такая доза лекарства вызывала у пациентов лишь незначительное кратковременное понижение АД. У R.L. Smith после приема дебризохина развился ортостатический коллапс, который продолжался 4 часа, а сама гипотензия сохранялась 2 суток. Причиной интолерантности в данном случае послужила низкая скорость метаболизма дебризохина.
РЕАКЦИИ ТИПА В
Аллергические реакции (реакции гиперчувствительности). Это группа реакций,
связанная с гиперактивацией иммунной системы. Они не зависят от вида лекарственного вещества и величины принятой дозы, протекают стереотипно (т.е. имеют универсальные проявления не зависимо от вызвавшего их лекарственного средства). У чувствительных лиц аллергическую реакцию могут вызвать ничтожные дозы лекарства (запах пенициллина в процедурном кабинете может привести к развитию анафилактического шока у пациента с аллергией к нему), тогда как у лиц без аллергической сенсибилизации введение даже значительных доз лекарства не способно вызвать такую реакцию.
Для проявления аллергической реакции необходима предварительная сенсибилизация организма, поэтому после первого контакта организма с лекарством-аллергеном латентный период может продолжаться по меньшей мере 1-2 недели (за это время иммунные клетки синтезируют антитела). Только вторичный контакт с аллергеном вызовет развитие аллергической реакции.
В роли антигенов, вызывающих аллергию могут выступать лекарства-белки (стрептокиназа, инсулин). Большинство же лекарств является гаптенами (неполными антигенами). Они приобретают антигенные свойства лишь после того, как соединяться с белком (например, белком плазмы крови). Для развития аллергической реакции совсем не обязательно наличие антител к данному лекарству. Химически родственные лекарственные средства могут вызывать перекрестные аллергические реакции.
Выделяют 4 типа аллергических реакций:
Тип I – аллергические реакции немедленного типа, анафилактические реакции. Связаны с образованием реагиновых антител (IgE), которые фиксируются на поверхности тучных клеток. При повторном воздействии лекарства оно активирует антитела и вызывает выброс из тучных клеток биологически активных веществ – гистамина, серотонина, лейкотриенов и простагландинов. Аллергическая реакция проявляется через несколько минут и продолжается 1-2 часа. Примерами реакций такого типа является анафилактический шок, ангионевротический отек Квинке, крапивница, бронхиальная астма.
Тип II – цитолитические реакции. Антигенное лекарство образует комплекс с белками на поверхности клеток. К этому комплексу вырабатываются антитела. Антитела связывают комплексы белок-лекарство и активируют систему комплемента, который повреждает мембрану клеток и вызывает их гибель. Примерами реакций этого типа является тромбоцитопения, агранулоцитоз и гемолитическая анемия после приема некоторых лекарств.
Тип III – иммунокомплексные реакции. Лекарство-антиген и антитело образуют циркулирующие иммунные комплексы. Эти крупномолекулярные комплексы могут фиксироваться к стенкам мельчайших капилляров легких, почек, кожи и привлекать к ним фагоциты. Фагоциты, поглощая комплексы вырабатывают ряд ферментов, повреждающих ткань. Примерами реакций такого типа является развитие сыпей, сывороточной болезни (лихорадка, артралгии, лимфаденопатии), васкулитов и нефритов после приема лекарства.
19
Тип IV – клеточно-опосредованная реакция замедленного типа. Связана с появлением на Т-лимфоцитах антиген-специфических рецепторов. Такие лимфоциты называются сенсибилизированными. При поступлении антигена (лекарства) Т-лимфоциты выделяют лимфокины, которые привлекают в очаг фагоциты, лимфоциты и запускают воспалительную реакцию. Примерами реакций этого типа являются контактный дерматит и фотосенсибилизация при приеме лекарства.
Идиосинкразия – качественно измененная необычная реакция на лекарственное средство, обусловленная, как правило, генетическими аномалиями. Наиболее ярким примером идиосинкразии является злокачественная гипертермия, которая возникает после применения галота (средство для наркоза) или сукцинилхолина (миорелаксант) у 1 человека из каждых 20.000. Реакция связана с аутосомно-доминантным дефектом строения саркоплазматического ретикулума в мышцах. При введении указанных выше лекарств у пациента происходит массивный выброс ионов кальция из депо в цитоплазму мышечного волокна, развиваются клонические судороги и повышается температура тела (за счет усиления термогенеза).
РЕАКЦИИ ТИПА С
Кумуляция (от лат. cumulatio – увеличение, скопление) – повышение интенсивности ответной реакции организма на повторное введение лекарства. Различают 2 вида кумуляции:
Материальная кумуляция – связана с накоплением в организме молекул лекарства, если оно вводится со скоростью большей, чем скорость элиминации этого лекарства. Наиболее характерен этот вид кумуляции для высоколипофильных веществ, которые имеют низкую скорость элиминации (сердечные гликозиды, барбитуровые препараты, амиодарон). Материальная кумуляция имеет как свои положительные, так и отрицательные стороны. Лекарственные средства, способные к кумуляции имеют длительное действие, поэтому их можно применять нечасто и это удобно для пациента. Однако, за счет кумуляциилекарства достаточно высок риск развития интоксикации, если уровень лекарства в организме превысит токсический порог.
Функциональная кумуляция – связана с тем, что фармакологический эффект лекарства сохраняется в организме больший период времени, чем само это лекарство. При повторном введении такого лекарства суммируются не его количества в организме, а эффекты этого лекарства. Функциональная кумуляция характерна для лекарственных средств, которые оказывают необратимое воздействие на субстрат. Например, тиклопидин быстро инактивируется в воротной вене кишечника, но при этом он успевает необратимо изменить мембрану эритроцитов, которые находятся в крови этой вены. При повторных введениях тиклопидина его эффекты суммируются, т.е. все большее и большее число эритроцитов подвергается необратимой модификации и реологические свойства крови улучшаются.
Толерантность (привыкание). Толерантность представляет собой эффект обратный кумуляции. Под толерантностью понимают снижение ответной реакции организма на повторные введения лекарственного средства. Для того, чтобы восстановить реакцию на лекарство его приходится вводить во все бóльших и бóльших дозах. Так, например, обычная доза диазепама для лечения фобий (тревожных неврозов) составляет 5-10 мг/сут, на фоне развития толерантности при длительном приеме она может составлять до 1000 мг/сут. Различают 2 вида толерантности:
Истинная толерантность – наблюдается как при энтеральном, так и при парентеральном введении лекарства, она не зависит от степени его всасывания в кровоток. В основе истинной толерантности лежат, как правило, фармакодинамические механизмы привыкания:
Десенситизация – снижение чувствительности рецептора к лекарственному средству. Например, β-адреномиметики при длительном применении приводят к фосфорилированию β-адренорецепторов и фосфорилированные рецепторы не способны ответить на β-адреномиметики.
20
Down-регуляция – снижение числа рецепторов к лекарственному средству. Например, при повторных введениях наркотических анальгетиков количество опиоидных рецепторов снижается и требуются все бóльшие и бóльшие дозы лекарства, чтобы вызвать желаемый ответ. Если лекарственное средство блокирует рецепторы, то механизм толерантности к нему может быть связан с up-регуляцией – увеличением числа рецепторов к лекарственному средству. Например, при длительном приеме β- адреноблокаторов число β-адренорецепторов на поверхности клеток начинает компенсаторно увеличиваться за счет синтеза новых молекул и требуются все более высокие дозы лекарства, чтобы блокировать новые рецепторы.
Включение компенсаторных механизмов регуляции. Например, при первом введении гипотензивного средства нифедипина у пациента может развиться ортостатический коллапс (резкое падение артериального давления). Однако, при последующих введениях барорефлексы адаптируются к способности лекарства расширять сосуды и не допускают падения артериального давления нижеуровня, необходимого для кровоснабжения мозга.
Истинная толерантность может носить не только приобретенный, но и врожденный характер. Так, например, афро-американцы обладают врожденной толерантностью к β- адреноблокаторамиингибиторамАПФ, аевропейцы– кα-адреноблокирующимсредствам.
Относительная толерантность (псевдотолерантность). Этот вид толерантности развивается только при введении лекарства внутрь и связан со снижением скорости и полноты всасывания лекарства. Данный вид толерантности искусственно вырабатывали в древние века лица, которые боялись быть отравленными. Наиболее показателен пример Митридата Великого (ок. 132-63 гг до н.э.) царя Понта Эвксийского. Отравив свою мать он достиг вершины власти, но при этом сам стал панически бояться быть отравленным соперниками. В течение многих лет он принимал внутрь в небольших дозах различные яды и наконец, потерял к ним восприимчивость. Когда Понт был завоеван Цезарем Митридат, чтобы избежать позорного пленения пытался покончить с собой и просил вначале сына, а затем жену дать ему яд. Но его организм не воспринимал яд и, наконец, царю пришлось просить раба, чтобы тот заколол его. Данный пример толерантности связан с тем, что яд не абсорбировался в кишечнике Митридата, но если бы ему была введена даже ничтожная доля яда парентерально, он, несомненно бы, погиб.
Тахифилаксия (от греч. tachys – быстрый, phylaxis – бдительность, охрана) – состояние при котором часто введение лекарственного средства вызывает развитие толерантности уже через несколько часов, но при достаточно редких введениях лекарства его эффект сохраняется в полной мере. Развитие толерантности связано обычно с истощением эффекторных систем. Например, действие симпатомиметика эфедрина связано с вытеснением норадреналина из окончаний симпатических нервов. Если эфедрин вводят слишком часто, то запас норадреналина в окончаниях не успевает возобновиться и тахифилаксия развивается уже через 3-5 введений эфедрина.
Лекарственная зависимость. «То, что человечество в целом будет когда-либо обходиться без искусственного рая, маловероятно. Большинство мужчин и женщин ведут такую тягостную жизнь, которая в лучшем случае так монотонна, убога и ограничена, что желание «уйти» от нее, отключиться хотя бы на несколько мгновений, есть и всегда было одним из основных желаний души». Эта мысль была высказана A. Huxley в его работе «The Doors of Perception» и до сих пор именно она выражает всю суть существования проблемы лекарственной зависимости.
Лекарственная зависимость – состояние психики и/или физическое состояние, которое является следствием воздействия на организм лекарственного средства и характеризуется специфическими поведенческими реакциями, трудно преодолимым стремлением повторно принимать лекарство, чтобы добиться особого психического эффекта или избежать дискомфорта при отсутствии лекарства в организме.
Лекарственная зависимость характеризуется:
