
лекции / ИО_Кровь
.pdfЛЕКАРСТВЕННЫЕ СРЕДСТВА, ВЛИЯЮЩИЕ НА СИСТЕМУ КРОВИ.
Когда я спал в саду, Как то обычно делал пополудни,
Мой мирный час твой дядя подстерег С проклятым соком белены в сосудце И тихо мне в преддверия ушей
Влил прокажающий настой, чье свойство Так глубоко враждебно нашей крови, Что, быстрый, словно ртуть, он проникает В природные врата и ходы тела И свертывает круто и внезапно, Как если кислым капнуть в молоко, Живую кровь…
В. Шекспир Гамлет, акт I, сцена 5.
Средства, влияющие на систему гемостаза.
Гемостаз – способность крови циркулировать по сосудистому руслу, оставаясь в жидком состоянии и образовывать плотные сгустки (тромбы) при нарушении его целостности. В более узком смысле – гемостаз это способность крови переходить из жидкого состояния в состояние сгустка (тромба). Гемостаз обеспечивает тонко сбалансированный ансамбль ряда взаимосвязанных компонентов. В гемостазе выделяют:
1.Сосудисто-тромбоцитарное звено (первичный гемостаз), которое образует:
a.Эндотелий сосудов;
b.Тромбоциты циркулирующей крови, которые, подвергаясь агрегации-дезаг- регации, способны образовывать тромбоцитарные сгустки.
2.Плазмено-коагуляционное звено (вторичный гемостаз), которое включает:
a.Свертывающую систему крови;
b.Противосвертывающую систему крови;
c.Фибринолитическую систему.
СРЕДСТВА, ВЛИЯЮЩИЕ НА СОСУДИСТО-ТРОМБОЦИТАРНОЕ ЗВЕНО ГЕМОСТАЗА.
Сосудисто-тромбоцитарное звено гемостаза активируется при повреждении мелких сосудов. Основная функция его – обеспечение процессов агрегации-дезагрегации форменных элементов крови. Агрегация – это способность форменных элементов склеиваться между собой и образовывать конгломераты (агрегаты частиц). Процесс агрегации заканчивается формированием тромба. Первоначально формируется белый – тромбоцитарный тромб, а затем за счет присоединения эритроцитов он трансформируется в красный. Дезагрегация – обратный процесс перехода форменных элементов из агрегата во взвешенное состояние и способность находиться в этом состоянии неопределенно долго. Средства, которые ускоряют агрегацию называются проагрегантами, средства, которые препятствуют агрегации называют дезагрегантами.
Физиология сосудисто-тромбоцитарного гемостаза.
Сосудисто-тромбоцитарное звено гемостаза представлено эндотелием и тромбоцитами. Форменные элементы поддерживаются в дезагрегированном состоянии во многом благодаря активности эндотелия. Эндотелий – слой клеток, который выстилает поверхность сосудов изнутри. Поверхность эндотелия имеет избыточный отрицательный заряд, который обеспечивают сульфатные группы молекул гепарина, гепарана и дерматана сульфата, покрывающих эндотелий непрерывным слоем. Благодаря этому слою форменные элементы крови не способны длительно удерживаться на поверхности эндотелия или прилипать к ней. Кроме того, на внешней мембране эндотелия экспрессирована АДФ-аза – фермент, который разрушает АДФ до АМФ. АМФ блокирует Р2Y-пуриновые рецепторы на поверхности тромбоцитов и тормозит тем самым их агрегацию. Благодаря активности цитозольных ферментов эндотелий выделяет в кровь ряд эндогенных антиагрегантов – простациклин (PgI2), оксид азота
(NO) и проагрегантов – эндотелины.

Узловым компонентом сосудисто-тромбоцитарного звена гемостаза являются тромбоциты. Тромбоциты – это безъядерные обломки (фрагменты) мегакариоцитов – клеток красного костного мозга. В 1 литре крови в норме находится 240.000-320.000×109 этих клеток. Средняя длительность жизни тромбоцита составляет 7-10 сут. Агрегация тромбоцитов протекает в 2 этапа: 1) обратимая агрегация тромбоцитов, которая завершается сборкой интегриновых рецепторов на поверхности тромбоцита и 2) необратимая агрегация – завершается формированием тромбоцитарного тромба.
Схема 1. Основные этапы агрегации тромбоцитов. ФЛ – фосфолипиды (фосфатидилхолин), ФлА2 – фосфолипаза А2, АхК – арахидоновая кислота, ЦОГ – циклооксигеназа, PgG2 – простагландин G2, PgH2 – простагландин H2, PgI2 – простациклин, ТхА2 – тромбоксан А2, АТФ – аденозинтрифосфорная кислота, АДФ – аденозиндифосфорная кислота, АМФ – аденозинмонофосфорная кислота, АС – аденилатциклаза, ФДЭ – фосфодиэстераза, цАМФ – циклический 3’5’-аденозинмомнофосфат, ФлС – фосфолипаза С, PIP2 – фосфатидил инозитол бифосфат, IP3 – инозитол трифосфат, IIb/IIIa – интегриновыйрецептор, ФАТ– факторактивациитромбоцитов.
Обратимая агрегация тромбоцитов протекает по трем путям:
•Циклооксигеназо-зависимый
•ФАТ (фактор активации тромбоцитов)-зависимый
•АДФ-зависимый.
Циклооксигеназо-зависимый путь. При травме сосуда происходит нарушение целостности эндотелиальной выстилки и исчезновение избыточного отрицательного заряда на поверхности клеток. Прекращается электростатическое отталкивание форменных элементов от стенок сосуда, обнажаются адгезивные белки коллагенового субэндотелиального слоя – фибронектин, ламинин, витронектин и фактор Виллебранда. Эти белки являются центрами притяжения тромбоцитов. На поверхности тромбоцитов экспресированы интегриновые рецепторы – гликопротеины Ia и Ib, которые распознают адгезивные молекулы и связываются с ними. Связь тромбоцитов с адгезинами повышает активность фосфолипазы А2, которая расщепляет фосфатидилхолин мембран до арахидоновой кислоты и лизоФАТ. Арахидоновая кислота циклооксигеназой окисляется до нестабильных эндоперекисей – PgH2, PgG2, которые в свою очередь под влиянием тромбоксан-синтазы конвертируются в тромбоксан А2 (ТхА2) – один из мощнейших проагрегантов. Связываясь с тромбоксановыми рецепторами на

поверхности тромбоцитов, ТхА2 повышает активность связанной с рецептором фосфолипазы С, которая гидролизует фосфатидил инозитол бифосфат (PIP2) до инозитол трифосфата (IP3) и диацилглицерола. IP3 воздействует на рецепторы плотной тубулярной системы (ПТС), которая представляет сосбой сеть внутриклеточных канальцев и трубочек, хранящих запасы ионов кальция. Активация IP3-рецепторов открывает рН-чувствительные Са2+-каналы и уро-
вень ионов кальция в цитоплазме возрастает. Ко-фактором активации канала является АТФ, которая при этом подвергается гидролизу до АДФ. Повышение внутриклеточной концентрации Са2+ активирует транспорт и встраивание компонентов интегринового рецептора – IIb и IIIа в клеточную мембрану тромбоцитов, там происходит сборка рецептора IIb/IIIa, который распознает на поверхности α-цепей фибриногена так называе-
мые RDG-участки (-arg-gly-asp-). Эти RDG-участки выступают в роли лигандов интегриновых рецепторов и тромбоциты прочно фиксируются на поверхности фибриногена, формируя при этом конгломерат.
В эндотелии сосудов также присутствует циклооксигеназная система. Однако, в отличие от тромбоцитов, здесь эндоперекисные соединения PgH2 и PgG2 простациклинсинтазой преобразуются в простациклин (PgI2) – мощный антиагрегант. Взаимодействуя с простациклиновыми рецепторами на поверхности тромбоцита, простациклин повышает активность связанной с ним аденилатциклазы и в клетке происходит интенсивный синтез цАМФ. При этом цАМФ-зависимые протеинкиназы фосфорилируют белки, обеспечивающие процессы элиминации кальция из цитоплазмы (Na+/Ca2+-обменник мембраны и Са2+/Мg2+-АТФ-азу плотной тубулярной системы). Фосфорилированная форма этих белков является активной, транспорт кальция из цитоплазмы возрастает и внутриклеточное содержание ионизированного кальция понижается. При снижении уровня ионизированного кальция прекращается процесс транспорта и сборки интегриновых рецепторов IIb/Ша, а уже собранные комплексы подвергаются диссоциации и агрегация тромбоцитов нарушается.
ФАТ-зависимый путь. ЛизоФАТ, который образуется в результате действия фосфолипазы А2 на предыдущем этапе, подвергается конверсии в ФАТ (см. схему 1) ферментом ацетил-трансферазой. ФАТ является лигандом PAF-рецепторов 2 типов – PAF1 и PAF2, которые характеризуются соответственно высоким и низким аффинитетом к ФАТ. РАF2-рецепторы локализованы, главным образом, на макрофагах и их активация приводит к повышению ак-
тивности пентозофосфатного цикла и индукции кислородного взрыва в макрофагах, усиливает экспрессию антигенов HLA-II, рецепторов IL-2, стимулирует синтез ФНО, IL-1,6 и колониестимулирующих факторов. PAF1-рецепторы локализованы, главным образом, на тромбоцитах и их активация вызывает повышение ферментативной активности фофолипазы С, что в конечном итоге (см. выше) приводит к сборке интегриновых рецепторов Пb/IIIа и запускает агрегацию тромбоцитов. ФАТ-зависимый путь не имеет супрессивного контроля со стороны эндотелия.
АДФ-зависимый путь. АДФ-зависимый путь связан с активностью пуриновых рецепторов тромбоцитов.
В настоящее время описаны 2 семейства пуринорецепторов: P1 и Р2-типа. P1- пуринорецепторы сопряжены с G-белками и агонизм к этим рецепторам в ряду аденозин>АМФ>АДФ>АТФ ослабевает. Данный тип рецепторов разделяют на 4 семейства – А1- А4 рецепторы. Антагонистами А1 и А2-рецепторов являются метилксантины, тогда как А3 и
А4-рецепторы не блокируются этими соединениями. А1-рецепторы, расположенные в гладкомышечных клетках, миокарде и скелетных мышечных волокнах, напрямую активируют калиевые каналы мембраны клетки, блокируют ее аденилатциклазную систему. Открытие калиевых каналов и выход калия из клетки сопровождается гиперполяризацией ее мембраны, что приводит к нарушению процесса возбудимости и сократимости мышечной ткани (проявляется отрицательное инотропное действие на миокард). А1-рецепторы, расположенные в тромбоцитах сопряжены с Gi-белком, который угнетает активность мембранной аденилатциклазы и Gs-белком, который стимулирует фосфолипазу С. В конечном итоге это приводит к понижению образования в клетке цАМФ и увеличению содержания в ней ино- зитол-трифосфата. В условиях избытка IP3 стимулируется поступление кальция внутрь клетки, а из-за недостатка цАМФ – удаление ионов кальция из клетки затруднено. Т.о. активация А1-рецепторов сопровождается повышением уровня ионов Са2+ в тромбоцитах и сборкой под влиянием этих ионов интегринового рецепторного комплекса.
А2-рецепторы располагаются в мембранах тромбоцитов, лимфоцитов и клетках коры головного мозга. Стимуляция этих рецепторов приводит к повышению уровня активности аденилатциклазы (через Gs-белок) и содержания в клетке цАМФ. Под влиянием цАМФ происходит фосфорилирование белков переносчиков Са2+ и он начинает активно удаляться из клетки. Недостаток кальция в клетке приводит к затруднению синаптической передачи в нервной системе, нарушениюкооперации иммунокомпетентных клетокиагрегации тромбоцитов.
Функция А3 и А4 рецепторов остается невыясненой.
Р2-пуринорецепторы обладают иной чувствительностью к агонистам, среди производных аденозина агонизм нарастает в ряду АТФ>АДФ>АМФ>аденозин. В этой группе рецепторов также выделяют 2 семейства Р2X-рецепторы, сопряженные с ионными каналами и Р2Y- рецепторы, которые связаны с G-белками. Функции этих рецепторов изучены крайне слабо, однако установлено, что в агрегации тромбоцитов весьма существенную роль играют имен-
но Р2Y-рецепторы.
При активации ЦОГили ФАТ-зависимого путей агрегации тромбоцитов, выброс кальция из внутриклеточного депо сопряжен с гидролизом АТФ до АДФ (см. выше). АДФ, которая образуется в ходе этого процесса, является агонистом пуриновых Рау-рецепторов, которые непосредственно стимулируют процессы транспорта и сборки интегриновых IIb/IIIa рецепторов на поверхности тромбоцитов. В обычных условиях эндотелий экспресирует на своей мембране АДФ-азу – фермент, который гидролизует АДФ до АМФ. АМФ – антагонист Р2Y-рецепторов, который препятствует стимулирующему влиянию АДФ на процессы сборки интегринов и индукции агрегации тромбоцитов.
АНТИАГРЕГАНТНЫЕ СРЕДСТВА
Показания и критерии оценки при проведении антиагрегантной терапии.
Показания к антиагрегантной терапии:
1.С профилактической и лечебной целью при стабильной и нестабильной форме стенокардии, инфаркте миокарда;
2.Для профилактики тромбоэмболических осложнений у лиц с протезами сосудов и клапанов сердца;
3.Для профилактики тромбоэмболических осложнений у пациентов с постоянной формой мерцательной аритмии, поскольку при этой форме аритмии формируются внутрипредсердные тромбы (особенно, если размеры левого предсердия превышают 10 см по данным УЗИ сердца).
4.Диабетическая и другие формы микроангиопатии и ретинопатии.
Абсолютные противопоказания к проведению антиагрегантной терапии:
1.Геморрагические диатезы любой этиологии, гемофилия;
2.Язвенное поражение желудочно-кишечного тракта (язвенная болезнь желудка и двенадцатиперстной кишики, неспецифический язвенный колит) до ликвидации язвенных дефектов;
3.Неконтролируемая артериальная гипертензия (уровень ДАД более 105 мм. рт. ст.);
4.Ранний послеоперационный период;
5.Беременность.
Критерии оценки эффективности антиагрегантной терапии.
•Время кровотечения по Дьюку. В норме составляет 2-4 минуты. Оптимальным является увеличение этого показателя в 2-2,5 раза;
•Индекс АДФ и коллагениндуцированной агрегации тромбоцитов. В норме составляет 3178% для АДФ и 47-93% для коллагена. Оптимальным считается снижение индекса на ½-
⅓от первоначального уровня.
Критерии оценки безопасности антиагрегантной терапии.
•Подсчет числа тромбоцитов. Нормальный показатель составляет 180-320×109 клеток в литре. В случае снижения этого показателя до 100×109 клеток в литре и менее необходимо немедленно прекратить дезагрегантную терапию;
•Эндотелиальные пробы («щипка», «жгута», «манжетки»). Для постановки пробы щип-
ка врач собирает под ключицей кожу в складку и делает щипок. В норме не возникает никаких изменений ни сразу после щипка, ни 24 часа спустя. Если через 24 часа на коже появляются видимые на глаз петехии, необходимо пересмотреть дозировку дезагрегантных средств. Для постановки пробы жгута на предплечье на 1,5-2 см ниже локтевой ямки очерчивают круг диаметром 2,5 см. На плечо накладывают манжету тонометра и создают давление 80 мм рт. ст., поддерживая его строго на таком уровне в течение 5 минут. Затем в очерченном круге подсчитывают число петехий. В норме наблюдается не более 10 петехий. При увеличении числа петехий необходимо снизить дозу дезагреганта.
•Появление колено-геморрагического синдрома. В норме кожно-геморрагический синдром отсутствует. Возникновение его в любой из моментов дезагрегантной терапии следует трактовать как показание к уменьшению доз лекарственных средств или же их полной отмене.
Классификация средств, обладающих антиагрегантной активностью:
I.Средства, воздействующие на ЦОГ-зависимый путь агрегации тромбоцитов.
A.Средства, понижающие активность тромбоксановой системы.
1.Ингибиторы синтеза тромбоксана А2:
•ингибиторы ЦОГ: ацетилсалициловая кислота, сулъфинпиразон, индобуфен;
•ингибиторы тромбоксансинтазы: дазоксибен, бензидамин, пирмагрел.
2.Блокаторы тромбоксановых рецепторов: ридогрел, вапипрост.
B.Средства, повышающие активность простациклиновой системы.
1.Синтетические аналоги простациклина: илопрост, эпопростенол.
2.Стимуляторы синтеза и выделения простациклина. никотиновая кислота, ксан-
тинола никотинат.
C.Средства, понижающие активность ФДЭ: дипиридамол, пентоксифиллин.
II. Антагонисты Р2Y-пуриновых рецепторов (тиенопиридины): тиклопидин, клопидогрель.
III. Антагонисты PAF-рецепторов: кадсуренон, танакан, кетотифен, алпразолам, триазолам.
IV. Антагонисты интегриновых IIb/IIIa рецепторов.
A.Дезинтегрины или RDG-белки: барбурин, флаворидин, кистрин, алболабрин, эптифибатид
B.Моноклональные химерные антитела: абциксимаб
C.Непептидные антагонисты (фибаны): ламифибан, тирофибан, ксемилофибан, фрадафибан
I. Средства, влияющие на ЦОГ-зависимый путь агрегации тромбоцитов.
Ацетилсалициловая кислота (Acidum acethylsalicylicum, Aspirine). Относится к не-
стероидным противовоспалительным средствам. МД: Ацетилсалициловая кислота (АСК) взаимодействует с активным центром цоклооксигеназы и ацетилирует его по сериновому

остатку (Ser229). В результате этого активность фермента необратимо утрачивается. Угнетение ЦОГ происходит как в тромбоцитах, так и в эндотелии, где прекращается синтез ТхА2 и PgI2. Поскольку в эндотелиальных клетках имеется ядро, то, через несколько часов, за счет синтеза de novo молекул ЦОГ образование PgI2 восстанавливается. В отличие от эндотелия тромбоциты не имеют ядра, поэтому синтез ТхА2 возобновляется только по мере образования
новых тромбоцитов в костном мозге. Кроме того, полагают, что чувствительность ЦОГ тромбоцитов к ацетилсалициловой кислоте в несколько раз выше, чем у ЦОГ эндотелия, поэтому в относительно малых дозах АСК угнетает главным образом тромбоцитарную ЦОГ.
ФЭ: в дозах до 325 мг/сут АСК снижает агрегацию тромбоцитов практически не вызывая жаропонижающего, анальгетического или противовоспалительного эффектов. До настоящего времени АСК является «золотым стандартом» в выборе антиагрегационной терапии, ее эффективность и безопасность по сравнению с другими антиагрегантами подтверждена в ряде клинических испытаний.
РД: Как антиагрегант АСК принимают по 100-325 мг/сут в один прием, как правило, в вечернее время. При плохой переносимости возможно назначение через день в тех же дозах.
НЭ: 1) повышение риска кровотечений у лиц со скрытыми дефектами системы гемостаза или при приеме совместно с другими препаратами, понижающими свертываемость крови; 2) НПВС-гастропатия – язвенное поражение слизистой желудка; 3) острый внутрисосудистый гемолиз у лиц с дефектом глюкозо-6-фосфат дегидрогеназы; 4) при длительном приеме возможно развитие макроцитарной анемии, вызванной дефицитом фолата; 5) тератогенный эффект при использовании у беременных женщин.
ФВ: таблетки по 0,1; 0,325 и 0,5.
Сульфинпиразон (Sulfinpyrazone, Anturan) Фармакологически активный метаболит фенилбутазона. МД: необратимо ингибирует циклооксигеназу тромбоцитов и эндотелия. В эндотелии, за счет синтеза фермента de novo, образование PgI2 восстанавливается через несколько часов, но образование ТхА2 не возобновляется до тех пор, пока не обновится циркулирующий пул тромбоцитов. Кроме того, сульфинпиразон уменьшает выделение АДФ и серотонина из тромбоцитов при их дегрануляции.
ФЭ: В большей степени угнетает адгезию тромбоцитов, чем их агрегацию. Несмотря на то, что он является производным нестероидного противовоспалительного средства, сульфинпиразон лишен анальгетической и жаропонижающей активности. В малых дозах он лишен антиагрегантной активности, но оказывает выраженное урикозурическое действие, что иногда используется при лечении подагры и гиперурикемического синдрома.
РД: Как антиагрегант сульфинпиразон принимают внутрь по 200-400 мг 4 раза в день. НЭ: Возможно обострение язвенной болезни желудка и двенадцатиперстной кишки. ФВ: драже по 0,2; таблетки по 0,1.
Индобуфен (Indobufenum, Ibustrine). Полагают, что механизм действия этого средства связан с обратимым угнетением активности циклооксигеназы. После однократного применения действие лекарства сохраняется в течение 12 часов. Помимо антиагрегантного эффекта оказывает слабое анальгезирующее и противовоспалительное действие.
РД: Применяют внутрь по 100-200 мг 2 раза в день после еды. При нарушении функции почек (клиренс креатинина менее 40
мл/мин) дозу лекарственного средства необходимо уменьшить в 2 раза. НЭ: Кровоточивость, НПВС-гастропатия.
ФВ: таблетки по 0,2.
Дазоксибен (Dazoxyben), Безидамин (Benzydamine), Пирмагрел (Pyrmagrel). Эти соединения выступают в роли конкурентных ингибиторов тромбоксан-синтетазы. Они конкурируют с PgG2 и PgH2 за активный центр этого фермента и, в конечном итоге, скорость

образования ТхА2 резко падает. Однако, как было показано в ряде контролируемых клинических испытаний, эффективность этих средств невысока. Полагают, что одной из причин этого является накопление в клетках предшественников тромбоксана – эндоперекисей PgG2 и PgH2, которые выступают в роли агонистов тромбоксановых рецепторов и способны индуцировать агрегацию тромбоцитов даже в отсутствие ТхА2. В настоящее время в клинической практике эти средства практически не применяются.
Ридогрел (Ridogrel), Вапипрост (Vapiprost). Эти средства оказывают комбинированное воздействие на метаболизм тромбоксана: они понижают активность тромбоксансинтетазы и одновременно выступают в роли антагонистов рецепторов для ТхА2. Т.о. эти средства не только тормозят образование тромбоксана, но и блокируют на уровне рецепторов проагрегантное действие ТхА2 и других циклических эндопероксидов (PgH2, PgG2). В 1994 г. проводилось крупное клиническое исследование ридогрела в сравнении с ацетилсалициловой кислотой. Результаты исследования убедительно показали, что ридогрел не превосходит по клинической эффективности АСК.
Илопрост (Iloprost) - синтетический аналог PgI2. МД: При введении в организм, взаимодействует с простациклиновыми рецепторами на поверхности тромбоцитов и гладкомышечных клеток сосудов, это приводит к активации аденилатциклазного пути регуляции уровня кальция и в итоге, содержание свободных ионов кальция в цитозоле клеток падает.
ФЭ: Снижение свободного кальция в цитоплазме тромбоцитов приводит к антиагрегантному эффекту. В гладкомышечных клетках снижение уровня кальция сопровождается релаксацией клетки, развитием гипотензивного эффекта. В отличие от других аналогов простагландинов илопрост снижает давление в малом круге кровообращения (a. pulmonalis), поэтому иногда применяется при лечении легочной гипертензии. В расчете на вазодилятирующий эффект илопрост применяют также при лечении облитерирующих заболевани сосудов конечностей (синдром Рейно, болезнь Бюргера, облитерирующий эндартериит и др.). Как и природный простациклин илопрост повышает активность лецитин-холин ацилтрансферазы (ЛХАТ) сосудистой стенки, что способствует переводу свободного холестерина в форму эфиров и синтезу ЛПВП, при этом продукция ЛПНП падает (антиатерогенный эффект). Иногда илопрост применяется для профилактики и лечения тромбоцитопении, которая возникает у пациентов, получающих нефракционированный гепарин. Полагают, что это связано со способностью илопроста (как и других аналогов простациклина) увеличивать время жизни тромбоцитов.
РД: Вводят внутривенно медленно капельно в течение 45 мин в дозе 1-3 нг/кг/мин (максимально до 10 мкг на введение). Иногда илопрост применяют внутрь 1 мкг/кг 2-3 раза в день, однако, при пероральном введении его биодоступность не превышает 16%.
НЭ: 1) желудочно-кишечные расстройства – анорексия, тошнота, рвота, диарея; 2) коллапс, ортостатическая гипотензия; 3) кожные сыпи, распирающие боли по ходу вен; 4) достаточно часто отмечается парадоксальное усиление агрегации тромбоцитов после прекращения инфузии илопроста; 5) превышение допустимых доз может привести к развитию тяжелых желудочковых аритмий высоких градаций, которые обусловлены Са2+ перегрузкой миокарда. Нежелательные эффекты илопроста уменьшаются при его совместном применении с АСК (до 300 мг/сут).
Эпопростенол (Aepoprostenolum) – также синтетический аналог простациклина, для которого характерны те же эффекты, что и у илопроста. В отличие от илопроста, эпопростенол обладает более избирательным действием в отношении рецепторов тромбоцитов, поэтому практически не оказывает гипотензивного действия.
Никотиновая кислота (Acidum nicotinicum, Niacine, Vitamine PP) - витамин В3 (РР).
МД: При парентеральном введении никотиновая кислота вызывает выброс из эндотелия большого количества PgI2, гистамина и кининоподобных веществ, что приводит к снижению агрегации тромбоцитов, вазодилятации. Однако, вследствие плохой переносимости препараты никотиновой кислоты не применяют для длительной терапии как антиагрегантные средства.

РД: Курсовое введение никотиновой кислоты чаще всего используют при облитерирующих заболеваниях сосудов нижних конечностей. Лекарство вводят внутривенно в виде 1% раствора по схеме: в 1-ый день 1 мл, во 2-ой – 2 мл, в 3-ий – 3 мл и т.д. до 10 мл в день, после чего дозу понижают на 1 мл/день и вновь доводят до 1 мл.
До настоящего времени не имеется клинически достоверного подтверждения преимуществ терапииникотиновой кислотойпосравнениюсдругими антиагрегантными средствами.
НЭ: Большинство нежелательных эффектов никотиновой кислоты обусловлены выбросом гистамина и активацией кининовой системы. Быстрое введение никотиновой кислоты сопровождаетсягиперемиейкожныхпокровов, уртикарнойсыпью, зудом. Выбросгистамина ибрадикинина приводит к падению артериального давления, что сопровождается выраженным головокружением. Вызванныегистаминомикининамигиперемияиотекслизистыхоболочекжелчевыводящихпутей и мочеиспускательного канала могут привести к развитию симптоматики, напоминающей приступ желчной колики, дизурические расстройства (сильное жжение при мочеиспускании, спастические сокращения мочевого пузыря в конце акта мочеиспускания). При длительном применении никотиновой кислоты возможно развитие осложнений со стороны ЖКТ: анорексия, рвота, диарея, ульцерация слизистой оболочки желудка, нарушения функции печени (резкое повышение уровня трансаминаз в сыворотке крови); возможны гипергликемия и гиперурикемия, которые способны вызватьобострениелатентнопротекающейподагрыилидекомпенсациюсахарногодиабета.
Несмотря на то, что никотинамид лишен большинства нежелательных эффектов никотиновой кислоты, его применение в качестве антитромбоцитарного средства неэффективно.
ФВ: Ампулы 1% раствора по 1 мл.
Ксантинола никотинат (Xantinoli nicotinas, Complamin). Это средство является ком-
бинацией производного теофиллина – ксантина и никотиновой кислоты. МД: содержащаяся в молекуле никотиновая кислота вызывает выброс простациклина из эндотелия, что обеспечивает вазодилятацию и антиагрегантный эффект. Ксантинол – является слабым антагонистом A1-пуриновых рецепторов и, блокируя их, усиливает эффекты никотиновой кислоты: нарушается АДФ-зависимый путь агрегации тром-
боцитов, происходит релаксация гладкомышечных клеток сосудов за счет блокады пуриновых рецепторов на их поверхности.
ФЭ: В расчете на дезагрегантное и слабое сосудорасширяющее действие ксантинола никотинат применяют при лечении облитерирующих заболеваний нижних конечностей, диабетической ангио- и ретинопатии (поражение мелких капилляров сетчатки, почек и др. органов). В целом ксантинола никотинат переносится лучше, чем никотиновая кислота. Подобно пентоксифиллину ксантинола никотинат улучшает реологические свойства крови, за счет повышения деформируемости эритроцитов (см. пентоксифиллин).
РД: Ксантинола никотинат назначают внутрь по 0,15-0,3 г 3 раза в день после еды, курсами по 2 месяца. В тяжелых случаях можно вводить внутримышечно по 300 мг 1-3 раза в день или внутривенно медленно капельно после разведения 1500 мг ксантинола никотината в 500 мл 5% глюкозы (введение должно продолжаться не менее 3-4 часов).
НЭ: К сожалению, вазодилятирующий эффект ксантинола никотината в большей степени проявляется в неповрежденных сосудистых бассейнах, а его выраженность в участках подвергшихся воздействию ишемии значительно меньше. Поэтому, при использовании ксантинола никотината возможно развитие «синдрома обкрадывания» – парадоксальное усиление кровотока в нормально перфузируемых тканях и его резкое уменьшение в зонах ишемии. Наиболее опасен синдром обкрадывания у лиц с ИБС, имеющих субкритический уровень стеноза коронарных артерий.
ФВ: таблетки и драже 0,15; раствор в ампулах 15% по 2 и 10 мл.
Дипиридамол (Dipyridamolum, Curantyl, Persantin). МД: Полагают, что механизм действия дипиридамола связан с несколькими процессами.
•Дипиридамол усиливает в эндотелии образование проста-
циклина (PgI2), который оказывает антиагрегантное действие.
•Дипиридамол снижает активность фосфодиэстеразы цитоплазмы тромбоцитов. Это приводит к прекращению гидролитического разрушения в них цАМФ, который образуется
под влиянием PgI2, и усиливает антиагрегантное действие простациклина.
•Дипиридамол является конкурентным ингибитором аденозиндезаминазы – основного фермента утилизации аденозина в сосудистом русле. Дипиридамол тормозит захват аденозина эндотелием и эритроцитами. В конечном итоге концентрация аденозина в крови
возрастает. Подобно АМФ аденозин способен блокировать Р2Y-рецепторы тромбоцитов и препятствовать их активации под влиянием АДФ, а значит, препятствовать и проагрегантному действию АДФ.
ФЭ: Дипиридамол в большей степени подавляет адгезию, чем агрегацию тромбоцитов,
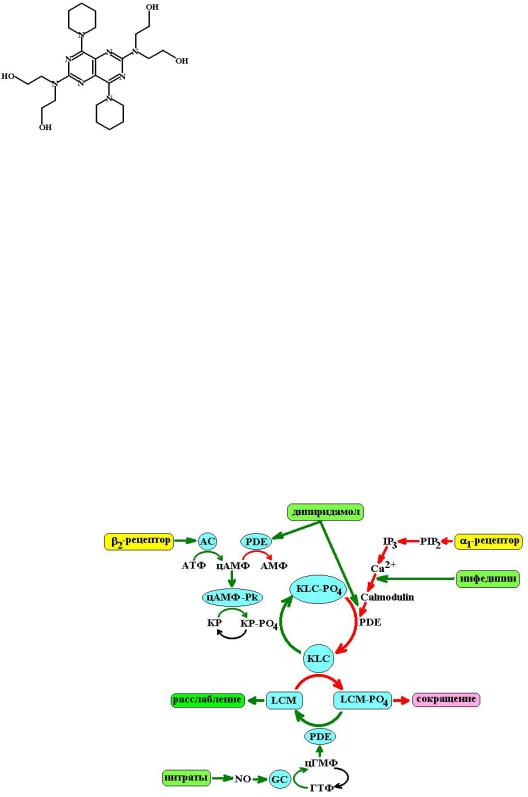
однако, по силе антиагрегантного действия он сопоставим с ацетилсалициловой кислотой. Дипиридамол оказывает вазодилятирующее действие за счет нарушения активности ФДЭ гладких мышц сосудов и повышения в них уровня цАМФ. Расслабление гладких мышц при этом обусловлено 2 процессами: 1) цАМФ активирует белки-переносчики ионов Са2+ в мембране клеток, которые удаляют ионизированный кальций из цитоплазмы и фибриллы миоцита расслабляются; 2) цАМФ-зависимые протеинкиназы фосфорилируют фермент киназу фосфорилазы и переводят ее в активную форму. Киназа фосфорилазы, в свою очередь, фосфорилирует киназу легких цепей миозина и тем самым инактивирует ее. Неактивная киназа легких цепей миозина не способна обеспечить фосфорилирование миозина, необходимое в процессе сокращения гладкой мышцы. В конечном итоге, происходит расслабление гладких миоцитов и развивается вазодилятация со снижением АД. (На схеме 2 регуляция тонуса гладких мышц представлена более подробно.)
Схема 2. Регуляция тонуса гладкамышечных клеток сосудов. АС – аденилатциклаза; РDE – фосфодиэстера-
за; IР3 – инозитолтрифосфат; РIР2 – фосфатидилинозитолбифосфат; цАМФ-Pk – цАМФ-зависимые протеинкиназы; Calmodulin – активный комплекс кальмодулина; КР – киназа фосфорилазы; KLC – киназа легких цепей миозина; LCM – легкие цепи миозина; GC – гуанилатциклаза; NO – оксид азота (эндотелийзависимый релаксирующий фактор). Красные пути обеспечивают повышение тонуса миоцита, зеленые – его снижение.
Для дипиридамола характерно также иммуномодулирующее действие. В ряде клинических исследований было показано, что прием дипиридамола снижает риск развития злокачественных опухолей колоректальной зоны. Полагают, что этот эффект лекарства обусловлен влиянием повышенного уровня цАМФ в клетке на экспрессию ряда проонкогенов в ее ядре.

Дипиридамол обладает слабым кардиотоническим действием, которое связано с увеличением уровня аденозина и усилением синтеза АТФ в миокарде.
РД: Дипиридамол принимают внутрь, натощак по 75 мг 3 раза в день. При хорошей переносимости дозу препарата можно увеличить до 300-450 мг/сут. Возможно внутривенное введение данного лекарства.
НЭ: 1) при быстром внутривенном введении может вызвать гиперемию лица, гипотонию и тахикардию; 2) развитие «синдрома обкрадывания» при внутривенном введении лекарства или применении высоких доз перорально (развитие синдрома обусловлено бóльшим вазодилятирующим эффектом дипиридамола в нормальных сосудах и меньшим – в зоне ишемии); 3) аллергические реакции; 4) при совместном назначении с β-лактамными антибиотиками или тетрациклинами возможнопарадоксальноеусилениеэффектовдипиридамола.
ФВ: таблетки идраже по 0,025 и0,075; растворвампулах0,5%-2 мл.
Пентоксифиллин (Pentoxyphylline, Trental, Agapurin) является производным тео-
бромина. МД: Полагают, что препарат оказывает многогранное воздействие на систему гемостаза:
•Пентоксифиллин выступает в роли слабого антагониста Р2X-рецепторов и, конкурируя с АДФ за связывание с этими рецепторами, снижает проагрегантное воздействие АДФ на пуриновые рецепторы и сборку интегриновых рецепторов.
•Пентоксифиллин снижает синтез фибриногена и усиливает образование тканевого активатора плазминогена (t-PA), что приводит к повышению активности фибринолитической системы.
•Пентоксифиллин повышает активность ферментов гликогенолиза в эритроцитах и повы-
шает тем самым содержание в них дифосфоглицерата. В эритроцитах дифосфоглицерат выполняет не только энергетическую функцию, но и является разобщителем белка цито-скелета эритроцитов спектрина и сократительного белка актина. Нарушение кооперации этих белков придает мембране эритроцита повышенную способность к деформации, поэтому эритроцит (с диаметром около 7 мкм) достаточно легко проходит даже по мельчайшим капиллярам (с
диаметром около 5 мкм). Кроме того, нарушение кооперации спектрина и актина вызывает конформационные изменения белков калиевых каналов и переводит каналы в неактивное состояние. В итоге, снижаются токи «утечки» калия из цитоплазмы эритроцитов и их осмотическая резистентность повышается. Этот механизм действия пентоксифиллина лежит в основе его способности улучшать динамические свойства эритроцитов.
ФЭ: Пентоксифиллин снижает адгезию и агрегацию тромбоцитов, оказывает некоторый вазодилятирующий эффект. Вазодилятация в области капилляров клубочков почек приводит к некоторому усилению диуреза. За счет блокирования ФДЭ III типа в кардиомиоцитах, пентоксифиллин оказывает слабое кардиотоническое действие. Следует отметить, что действие пентоксифиллина развивается медленно: антиагрегантный эффект проявляется только через 1-2 дня, а изменение динамических свойств эритроцитов отмечается только через 2-4 недели регулярного приема препарата. Это связано с тем, что пентоксифиллин влияет не на зрелые эритроциты, а на вновь образуемые в ходе гемопоэза клетки и клинический эффект проявляется только после того, как циркулирующий пул эритроцитов заменится более новыми клетками. Кроме того, пентоксифиллин оказывает тонизирующее действие на дыхательные мышцы (главным образом межреберные и диафрагму), что приводит к улучшению функции внешнего дыхания и дополнительному насыщению крови кислородом. Этот эффект лекарства в большей степени выражен в условиях исходной гипоксии мышц, которая имеет место при хронических неспецифических заболеваниях легких (хр. бронхиты, бронхиальная астма, эмфизема, пневмосклероз и др).
Показано, что регулярный прием пентоксифиллина снижает риск развития рака молочной железы и колоректальной зоны. Механизм этого эффекта до конца не выяснен, но
